Том 102, № 2 (2025)
- Год: 2025
- Выпуск опубликован: 12.05.2025
- Статей: 10
- URL: https://microbiol.crie.ru/jour/issue/view/189
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Исследование безопасности и иммуногенности вакцины для профилактики COVID-19 на основе вирусоподобных частиц в рамках I фазы клинических испытаний
Аннотация
Введение. Одним из перспективных направлений в предупреждении распространения инфекций, в том числе COVID-19, является получение вакцин на основе вирусоподобных частиц (virus like particles, VLP). В НИЦЭМ им. Н.Ф. Гамалеи разработана вакцина на основе VLP против COVID-19.
Цель работы — оценить переносимость, безопасность и иммуногенность новой вакцины для профилактики COVID-19 на основе VLP в сравнении с плацебо на протяжении 21 сут после двукратного внутримышечного введения в рамках I фазы клинических испытаний.
Материалы и методы. Двойное слепое плацебо-контролируемое исследование переносимости, безопасности, и иммуногенности вакцины для профилактики COVID-19 на основе VLP проводили с дозой введения препарата, содержащего 40 и 80 мкг антигена, плацебо — 0,9% NaCl. У 180 добровольцев в возрасте 18–55 лет отмечали наличие или отсутствие нежелательных явлений (НЯ) после вакцинации, оценивали показатели крови, напряжённость гуморального и клеточного иммунитета до и после вакцинации с помощью иммуноферментного анализа, реакции нейтрализации, реакции бласттрансформации лимфоцитов и проточной цитометрии.
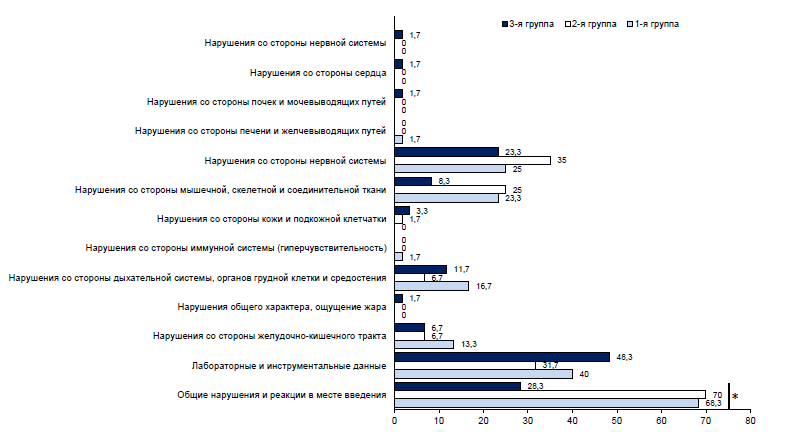
Результаты. Анализ переносимости и безопасности новой вакцины против COVID-19 на основе VLP показал, что большинство НЯ регистрировались в течение первых 10 сут после вакцинации, преимущественно после 1-й вакцинации. В период с 11-х по 21-е сутки после вакцинации НЯ отмечались в единичных случаях. Летальных исходов, серьёзных и иных НЯ не зарегистрировано. Введение исследуемой вакцины добровольцам не оказало негативного влияния на основные жизненные показатели. Сравнительная характеристика показателей иммуногенности у добровольцев показала, что введение вакцины с содержанием антигена как 40, так и 80 мкг приводит к выраженному и достоверному росту уровня специфических иммуноглобулинов, вируснейтрализующих антител и активации клеточно-опосредованного иммунного ответа. В рамках I этапа клинических исследований доза 80 мкг была выбрана как оптимальная.
Заключение. Новая вакцина для профилактики COVID-19 на основе VLP с содержанием антигена 40 и 80 мкг при введении добровольцам внутримышечно не вызывает серьёзных НЯ и индуцирует напряжённый гуморальный и клеточный иммунный ответ.
 135-149
135-149


Молекулярно-биологическая характеристика изолятов Streptococcus pneumoniae, выделенных от больных пневмококковым менингитом
Аннотация
Цель работы — дать ключевые характеристики изолятов Streptococcus pneumoniae, циркулирующих на территории России в 2015–2020 гг. и выделенных от больных пневмококковым менингитом, на основании данных высокопроизводительного секвенирования, включая глобальные кластеры пневмококковых последовательностей, серотипы, факторы вирулентности и генетические детерминанты резистентности, в сравнении с клиническими данными по чувствительности к антимикробным препаратам (АМП).
Материалы и методы. Исследовано 68 инвазивных изолятов S. pneumoniae, выделенных из крови и ликвора пациентов с бактериальным менингитом в разных регионах России в 2015–2020 гг. Видовую идентификацию проводили с учётом морфологии колоний на кровяном агаре, наличия α-гемолиза, отрицательной каталазной реакции, чувствительности к оптохину, положительных результатов латекс-агглютинации. Чувствительность изолятов к АМП определяли методом микроразведений в бульоне, категории чувствительности — на основании пограничных значений минимальных подавляющих концентраций (МПК). Проводили полногеномное секвенирование изолятов S. pneumoniae, анализ изолятов на сигнатуру пенициллинсвязывающих белков, определение глобальных кластеров пневмококковых последовательностей, аллелей MLST, серотипов, сиквенс-типов и генов приобретённой резистентности (mefA, ermB, tetM, folA/P, cat), идентифицировали гены вирулентности.
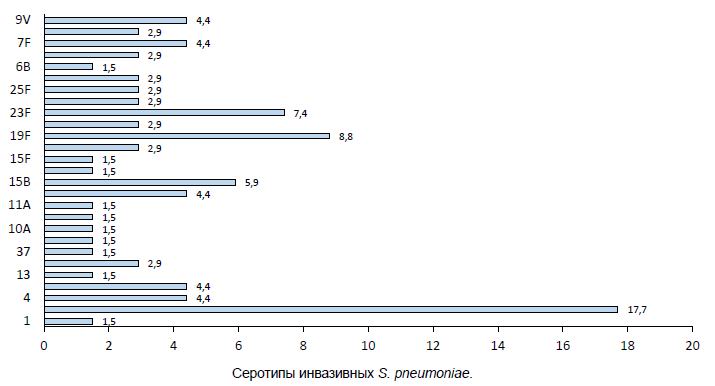
Результаты. Выявлены 28 GPSC, 45 сиквенс-типов и 27 серотипов. Степень охвата ППВ-23 и ПКВ-13 составила 78 и 59% соответственно. Доминировали серотипы 3 (18%), 19F (9%), 23F (7%) и 15В (6%). Преобладала (43%) линия GPSC12 (серотип 3). Линии, экспрессирующие вакцинные серотипы GPSC1(19F), GPSC6(14), GPSC13(6A), GPSC904(14) и GPSC10(19F), обладали множественной антимикробной резистентностью, включая резистентность к пенициллину. Резистентные линии, экспрессирующие невакцинные серотипы, — GPSC230 (13) и GPSC177 (35F). В большинстве случаев установлено соответствие генотипической и фенотипической резистентности к пенициллину (повышенные МПК β-лактамов коррелировали с типами пенициллинсвязывающих белков), эритромицину (ermB, mefA, ermB/mefA), клиндамицину (ermB) и тетрациклину (tetM) и триметоприму-сульфаметоксазолу (folA, folP). У всех изолятов обнаружены гены вирулентности cbpG, lytA, pce/cbpE, pavA, pfbA, ply, hysA, nanA и cps4A. Цинковая металлопротеиназа С обнаружена у 13% изолятов.
Заключение. Выявлено высокое разнообразие серотипов и линий среди изолятов пневмококков, выделенных у больных менингитом. Из 68 изолятов S. pneumoniae, выделенных у пациентов с бактериальным менингитом, более 17% относились к невакцинным серотипам. Результаты сопоставления фенотипической и генотипической антимикробной резистентности характеризовались хорошей конкордантностью, что указывает на необходимость дальнейшего изучения возможности использования полногеномного секвенирования в качестве диагностического инструмента для выявления механизмов резистентности у клинических изолятов пневмококков.
 150-161
150-161


Гуморальный иммунитет к адгезинам и токсинам возбудителя коклюша у мышей, иммунизированных экспериментальными бесклеточными коклюшными вакцинами из биоплёночной и планктонной культур Bordetella pertussis
Аннотация
Введение. Коклюш остаётся актуальной проблемой здравоохранения во всём мире, в том числе в странах с высоким уровнем вакцинации, где начиная с 1990-х гг. отмечается рост заболеваемости коклюшем, увеличение тяжести течения заболевания и летальности. В этой ситуации требуется создание нового поколения бесклеточных коклюшных вакцин (БКВ), способных более эффективно влиять на колонизацию, персистенцию и передачу Bordetella pertussis. Одним из возможных направлений совершенствования вакцинопрофилактики коклюшной инфекции является создание БКВ на основе протективных антигенов, выделенных из биоплёночных культур B. pertussis.
Цель работы — исследование уровня IgG-антител к антигенам возбудителя коклюша: адгезинам — филаментозному гемагглютинину (ФГА), пертактину (ПРН) и токсинам — коклюшному токсину (КТ), липополисахариду (ЛПС) у мышей, иммунизированных экспериментальными БКВ на основе антигенных комплексов, выделенных из биоплёночных и планктонных культур B. pertussis.
Материалы и методы. В опытах использовали экспериментальные БКВ на основе антигенных комплексов, выделенных из среды культивирования биоплёночной (БКВ-Б) и планктонной (БКВ-П) культур штамма B. pertussis № 317 (серовар 1.2.3). Титры IgG-антител к КТ, ФГА, ПРН и ЛПС в сыворотках крови мышей, иммунизированных БКВ-Б и БКВ-П, определяли в иммуноферментном анализе.
Результаты. Титры IgG-антител к адгезинам (ФГА и ПРН) в группе БКВ-Б были выше в 8 и 4 раза соответственно по сравнению с БКВ-П, при отсутствии значимых различий по титрам IgG-антител к КТ и ЛПС.
Заключение. Более высокая, по сравнению с БКВ-П, способность БКВ-Б индуцировать иммунный ответ к адгезинам B. pertussis при отсутствии существенных различий между ними в стимуляции IgG-антител к токсинам, указывает на преимущество использования антигенных комплексов из биоплёночных культур для создания БКВ нового типа.
 162-167
162-167


Динамика ферментативной активности в первичной культуре адгезивных лейкоцитов сирийского хомячка, заражённых SARS-CoV-2 ex vivo
Аннотация
Введение. Сохраняющаяся эпидемическая актуальность SARS-CoV-2 даже после завершения в 2023 г. связанной с ним пандемии COVID-19 определяет необходимость дальнейшего изучения взаимодействия этого вируса с клетками первой линии защиты — нейтрофилами.
Цель работы — определить ферментативную активность лейкоцитов периферической крови сирийских хомячков (Mesocricetus auratus) в динамике SARS-CoV-2-инфекции ex vivo, характеризующую микробицидный потенциал клеток врождённого иммунитета.
Материалы и методы. В работе использовался штамм SARS-CoV-2/Vladivostok/R-8726/2021 в заражающих дозах 3 lg (ТЦД50/мл) и 2 lg (ТЦД50/мл) (ТЦД50 — 50% тканевая цитопатическая доза для линии клеток Vero E6); время контакта заражающей вируссодержащей жидкости с клеточной культурой — 1 ч. Количество жизнеспособных клеток в культуре адгезивных лейкоцитов подсчитывали с помощью инвертированного микроскопа, оснащённого цифровой камерой, и программы MCView. Удельную (в расчёте на 1 жизнеспособную клетку) активности аденозинтрифосфатазы (АТФазы), 5′-нуклеотидазы (аденозинмонофосфатазы, АМФазы), лактатдегидрогеназы (ЛДГ), сукцинатдегидрогеназы (СДГ), миелопероксидазы (МПО) и цитохромоксидазы (ЦХО) определяли спектрофотометрическим методом после инкубации со специфическими субстратами инфицированных и неинфицированных клеточных культур через 1, 16, 24, 48 ч после инокуляции вируса (п.и.в.).
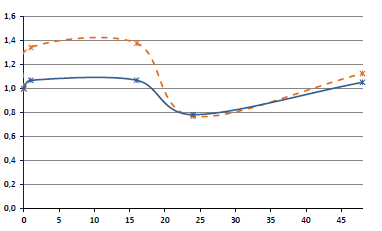
Результаты. Через 1 ч п.и.в. по сравнению с неинфицированными лейкоцитами была снижена удельная активность АТФазы, МПО, повышена активность АМФазы, ЛДГ, СДГ; через 16 ч п.и.в. снижена активность МПО, повышена активность АМФазы, ЛДГ, СДГ, на исходном уровне, т. е. примерно на уровне неинфицированного контроля находится активность АТФазы, ЦХО; через 24 ч п.и.в. снижена активность АМФазы, повышена активность АТФазы, на исходном уровне — активность ЛДГ, СДГ, МПО, ЦХО; через 48 ч п.и.в. повышена активность АТФазы, ЛДГ, СДГ, МПО, ЦХО, на исходном уровне — активность АМФазы. Изменения ферментативной активности зависят от величины заражающей дозы и коррелируют с накоплением вируса в культуральной среде.
Заключение. Выявленная динамика ферментативной активности в первичной культуре адгезивных лейкоцитов, инфицированных SARS-CoV-2 ex vivo, свидетельствует о снижении микробицидного потенциала клеток врождённого иммунитета в процессе этой инфекции.
 168-178
168-178


Прогнозирование заболеваемости иксодовым клещевым боррелиозом с использованием методов математического моделирования (на примере Кировской области)
Аннотация
Введение. Кировская область — эндемичный регион по иксодовому клещевому боррелиозу (ИКБ), что обусловлено климатическими условиями, обилием клещей и их прокормителей. Экономический ущерб от ИКБ включает затраты на лечение больных и ликвидацию природных очагов. Прогнозирование заболеваемости необходимо для планирования профилактических мероприятий (акарицидных обработок, информационно-разъяснительной работы с населением) и энтомологического мониторинга. Эффективность таких мер превышает вышеуказанные затраты, что подчёркивает актуальность исследования.
Цель исследования — изучение влияния различных факторов на заболеваемость ИКБ с использованием методов математического моделирования для дальнейшего эпидемиологического прогнозирования на примере Кировской области.
Материалы и методы. Изучены данные государственных докладов «О состоянии санитарно-эпидемиологического благополучия населения в Кировской области» за 2006–2023 гг. по заболеваемости ИКБ, первому и последнему зарегистрированным случаям присасывания клеща к человеку и объёму акарицидных работ. Гидрометеорологические данные: среднемесячные и среднегодовые значения температуры воздуха, влажности воздуха и объёма осадков. Проводили корреляционный анализ по Спирмену и множественный регрессионный анализ, в качестве критерия статистической значимости был выбран уровень p < 0,05.
Результаты. Интервальный прогноз заболеваемости: к 2024 г. — до 18,67 на 100 тыс. населения, к 2025 г. — 16,51, к 2026 г. — 14,36. Выявлены корреляции между климатическими факторами и заболеваемостью ИКБ, отрицательная достоверная корреляционная связь умеренной тесноты между заболеваемостью ИКБ в Кировской области и объёмом акарицидных работ. Разработаны две модели прогнозирования: на основе сроков первого и последнего зарегистрированных случаев присасывания клещей; на основе гидрометеорологических факторов и объёма акарицидных работ.
Заключение. Заболеваемость ИКБ в Кировской области характеризуется тенденцией к снижению. Предложены математические модели для прогнозирования заболеваемости ИКБ в Кировской области.
 179-189
179-189


Перспектива применения биофлуоресцентных белков на этапе доклинической оценки живых вакцин на примере вакцинного штамма Yersinia pestis EV НИИЭГ pTURBOGFP-B
Аннотация
Введение. Актуальны исследования, направленные на поиск наиболее информативного и оптимизированного метода оценки приживаемости вакцинного штамма чумного микроба в организме животных, привитых против чумы.
Цель работы — оценить целесообразность использования биофлуоресцентных белков на примере вакцинного штамма Yersinia pestis EV НИИЭГ pTurboGFP-B (EVGFP) в схемах сочетанного применения с иммуномодуляторами на этапе доклинической оценки живых вакцин.
Материалы и методы. Морских свинок иммунизировали EVGFP, выращенным при 28°С и 37°С (EVGFP28 и EVGFP37 соответственно), в сочетании с иммуномодуляторами: азоксимера бромидом (АБ) и интерфероном-γ человеческим рекомбинантным (ИЧР).
Результаты. Методом люминесцентной микроскопии выявлено обсеменение (до 600 м.к. в одном поле зрения) клетками EVGFP места введения культуры во всех опытных группах на 1-е сутки. Методом проточной цитометрии in vivo установлено, что на 1-е сутки во всех опытных группах фагоцитарный индекс (ФИ) составлял в среднем 94,5% с последующим снижением к 4-м суткам в среднем в 4,4 раза (на 21,2%). На 4-е сутки исследования в группе EVGFP37+АБ ФИ превосходил в 1,8 раза аналогичный показатель в группе EVGFP37. Напротив, в группе EVGFP28+ИЧР ФИ снижался в 2,2 раза относительно аналогичного показателя в группе EVGFP28. Кроме того, в группах EVGFP37+АБ и EVGFP37+ИЧР на 4-е сутки ФИ в 2 раза превышали показатели в группах EVGFP28+АБ и EVGFP28+ИЧР соответственно. В группе EVGFP37 фагоцитарное число превосходило в среднем в 1,5 раза показатель в группе EVGFP28.
Заключение. Получены данные, подтверждающие зависимость исхода взаимодействия in vivo чумного микроба с фагоцитами селезёнки от температуры выращивания бактерий, а также от присутствия АБ и ИЧР. Применение биофлуоресцентных белков, как показано на примере штамма EVGFP и метода проточной цитометрии, расширяет возможности оценки живых вакцин против чумы на доклиническом этапе.
 190-200
190-200


Опыт применения метода метагеномного секвенирования по фрагментам гена 16S рРНК для детекции и идентификации возбудителей природно-очаговых инфекций
Аннотация
Введение. Метагеномное секвенирование — один из наиболее перспективных методов как для детекции и идентификации возбудителей природно-очаговых инфекций (ПОИ), так и для определения видовой структуры различных бактериальных сообществ.
Цель работы — выполнить детекцию и идентификацию возбудителей ПОИ в образцах полевого и клинического материала методом метагеномного секвенирования фрагментов гена 16S рРНК, проанализировать таксономический состав эндосимбиотических микроорганизмов в образцах.
Материалы и методы. Исследованы образцы полевого (14 проб) и клинического (2 пробы) материала с различной нагрузкой ДНК возбудителей ПОИ, определённой методом полимеразной цепной реакции (Borrelia burgdorferi sеnsu lato, Anaplasma phagocytophilum, Francisella tularensis, Rickettsia spp., Coxiella burnetii). Амплификацию фрагментов гена, кодирующего 16S рРНК, осуществляли с помощью праймеров, фланкирующих вариабельные участки гена.
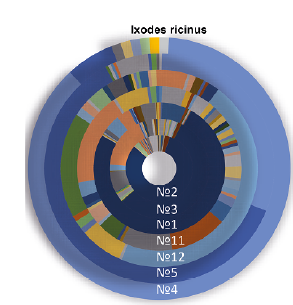
Результаты. В 14 из 16 исследуемых образцов детектированы целевые возбудители ПОИ. До вида идентифицированы R. aeschlimannii (в 57,1% положительных образцов), B. valaisiana (в 16,6%), F. tularensis (в 75%), C. burnetii (в 100%), также в одном образце выявлены боррелии — возбудители возвратных лихорадок (B. turcica, B. hispanica). Исследована таксономическая структура микробиома клещей Ixodes ricinus, Dermacentor reticulatus, Rhipicephalus annulatus, Hyalomma aegyptium, Dermaceptor marginatus, собранных в южных регионах России. Выявлено, что преобладающие микроорганизмы — это представители родов Flavobacterium, Pseudomonas, Serratia, Aeromonas, Pedobacter, Bradyrhizobium, Shingomonas. В пулах иксодовых клещей обнаружены ДНК-маркеры микроорганизмов — эндосимбионтов клещей Candidatus Midichloria mitochondrii, представителей родов Rickettsiella, Coxiella, непатогенных и условно-патогенных для человека видов родов Francisella.
Заключение. Показана эффективность метода метагеномного секвенирования фрагментов гена 16S pРНК для детекции и идентификации возбудителей ПОИ в пробах клинического и полевого материала. Метагеномное секвенирование по участкам гена 16S pРНК может быть рекомендовано в качестве дополнительного метода лабораторного исследования образцов с целью детекции и идентификации возбудителей ПОИ.
 201-212
201-212


Получение и очистка рекомбинантных белков VP2 и VP3 вируса Alongshan группы Jingmenvirus и оценка их иммунохимических свойств
Аннотация
Введение. Вирус Alongshan — представитель неклассифицированной группы Jingmenvirus (Flaviviridae), обнаружен в клещах Ixodes persulcatus, Ixodes ricinus и различных видах комаров в России, Китае, Финляндии и Франции. В отличие от классических ортофлавивирусов, геном вируса Alongshan представлен 4 сегментами РНК положительной полярности. Первый и третий сегменты генома кодируют белки, гомологичные белкам репликативной машинерии ортофлавивирусов, остальные сегменты кодируют предположительно структурные белки, не имеющие известных гомологов: сегмент 2 — VP1a (белок оболочки), VP1b и NuORF; сегмент 4 — VP2 (капсидный) и VP3 (мембранный). Описаны случаи заболевания людей, связанные с вирусом Alongshan.
Цель работы — разработка системы экспрессии и очистки рекомбинантных белков VP2 и гидрофильного участка VP3 для проверки их антигенных свойств.
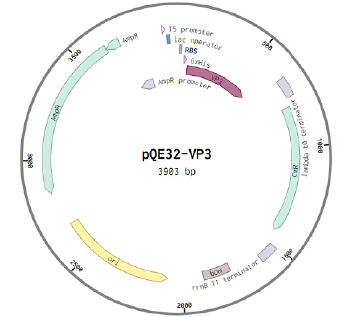
Материалы и методы. Для получения гипериммунных сывороток мышей и рекомбинантных белков в бактериальной системе экспрессии был использован штамм Miass527 вируса Alongshan. Произведены биоинформатический анализ последовательностей, кодирующих целевые белки, генно-инженерное клонирование. Для контроля результатов осуществлены иммуноблотинг и иммуноферментный анализ.
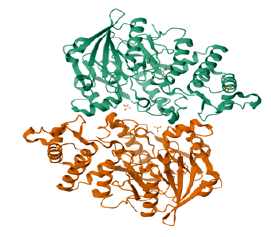
Результаты. Рекомбинантные белки вируса Alongshan использованы в лабораторной диагностической тест-системе для определения наличия антител к вирусу. Полученный рекомбинантный белок VP2 способен выявлять антитела во всех исследованных сыворотках инфицированных мышей, а также антитела в сыворотках людей как в вестерн-блоттинге, так и в иммуноферментном анализе. При этом антитела к рекомбинантному участку белка VP3 в противовирусных иммунных сыворотках выявлялись нерегулярно.
Заключение. Выявление антител к вирусу Alongshan у пациентов подтверждает необходимость дальнейшего исследования данной группы вирусов.
 213-222
213-222


НАУКА И ПРАКТИКА
Эффекторные молекулы стрептококков как перспективные противоопухолевые средства: плюсы и минусы
Аннотация
Онкологические заболевания остаются одной из основных причин инвалидности и смертности населения во всём мире. К наиболее злокачественным типам рака относятся опухоли поджелудочной железы, печени и головного мозга. Современные методы терапии (в том числе химиолучевая, таргетная, иммунная терапия) не позволяют добиться желаемой эффективности у этой группы пациентов. В этой связи необходимы новые подходы для терапии онкологических заболеваний.
Целью обзора явилось обсуждение механизмов противоопухолевого действия Strepococcus pyogenes и других видов стрептококков, а также рассмотрение их опухольстимулирующих эффектов и существующих при этом ограничений.
В обзоре рассмотрено современное состояние проблемы использования бактериальной онкотерапии с участием стрептококков группы А (в частности, S. pyogenes). Обсуждается участие факторов патогенности S. pyogenes: М-белка, экзотоксинов: стрептолизинов S, О, суперантигенов, аргининдеиминазы и др., а также молекулярные механизмы, опосредованные клетками иммунной системы организма-носителя. Собственные данные авторов показывают, что для S. pyogenes обнаружена селективная опосредованная М-белком цитолитическая активность в отношении опухолевых клеток глиомы С6 и аденокарциномы поджелудочной железы и её отсутствие на нормальных фибробластах. Кратко суммируются данные по доклиническому и клиническому применению полученного на основе стрептококков препарата OK-432 для терапии онкологических заболеваний. Обсуждаются и опухоль-ассоциированные свойства стрептококков (индукция секреции цитокинов, пролиферации, миграции и ангиогенеза эпителиальных клеток сосудов, образование внеклеточных ловушек нейтрофилов из микроокружения опухоли), обусловленные их взаимодействием с клетками иммунной системы организма-опухоленосителя.
Заключение. Представленные в обзоре научные данные убедительно показывают, что S. pyogenes могут при участии факторов патогенности непосредственно оказывать противоопухолевое действие на раковые клетки. Однако стрептококковую вакцину следует применять с осторожностью, учитывая индивидуальные особенности иммунной системы пациента, поскольку S. pyogenes могут оказывать и эффекты противоположного характера, требующие дальнейших исследований.
 223-238
223-238


ОБЗОРЫ
Современное состояние разработок в области создания вакцин против респираторно-синцитиального вируса
Аннотация
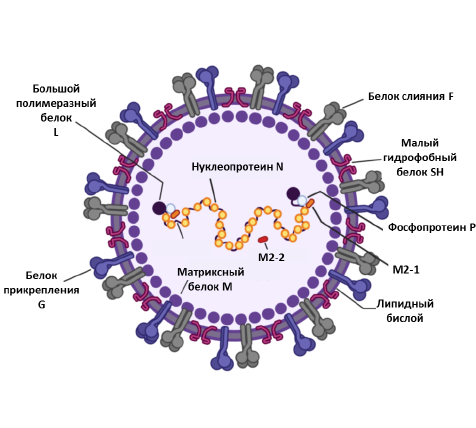
Респираторно-синцитиальный вирус (РСВ) является основной причиной инфекций верхних дыхательных путей у детей и пожилых. В отношении РСВ одобрено единственное специфическое средство лечения — препарат моноклональных антител паливизумаб для пассивной иммунопрофилактики у младенцев из группы высокого риска. Спустя 60 лет с момента обнаружения вируса были лицензированы несколько безопасных вакцинных кандидатов против РСВ. Этому способствовали исследования по выявлению структуры РСВ, изучению основных функций компонентов РСВ, механизмов врождённого и приобретённого иммунного ответов на инфекцию. Был учтён отрицательный опыт клинического испытания формалининактивированной вакцины против РСВ на детях, закончившийся смертью нескольких вакцинированных.
Цель исследования — обобщить данные исследований вакцинных кандидатов против РСВ на лабораторных животных и в клинических испытаниях на различных возрастных группах.
Поиск статей для анализа доклинических и клинических испытаний вакцин против РСВ осуществляли с использованием электронно-поискового ресурса PubMed по ключевым словам «respiratory syncytial virus and vaccine». В качестве критериев отбора указывали, что оригинальные статьи должны содержать сведения о доклинических и клинических исследованиях, причём последние включали в себя I–IV фазы рандомизированных контролируемых испытаний. За 1967–2025 гг. обнаружено 296 статей, обобщающих данные по исследованию вакцинных кандидатов против РСВ, и 1788 статей, в которых суммированы данные об испытаниях вакцинных кандидатов на животных. В обзоре суммированы данные доклинических исследований вакцинных кандидатов с указанием разработчиков, состава вакцинных препаратов, животных моделей, на которых проводились исследования, с кратким описанием основных результатов. Представлены данные о клинических испытаниях вакцинных кандидатов с указанием целевых групп населения, номера клинического исследования и источников, где опубликованы результаты этих исследований.
 239-264
239-264