Том 100, № 4 (2023)
- Год: 2023
- Выпуск опубликован: 21.09.2023
- Статей: 12
- URL: https://microbiol.crie.ru/jour/issue/view/179
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Характеристика эпидемического процесса COVID-19 в Москве и поиск возможных факторов, определяющих тенденции наблюдаемых изменений
Аннотация
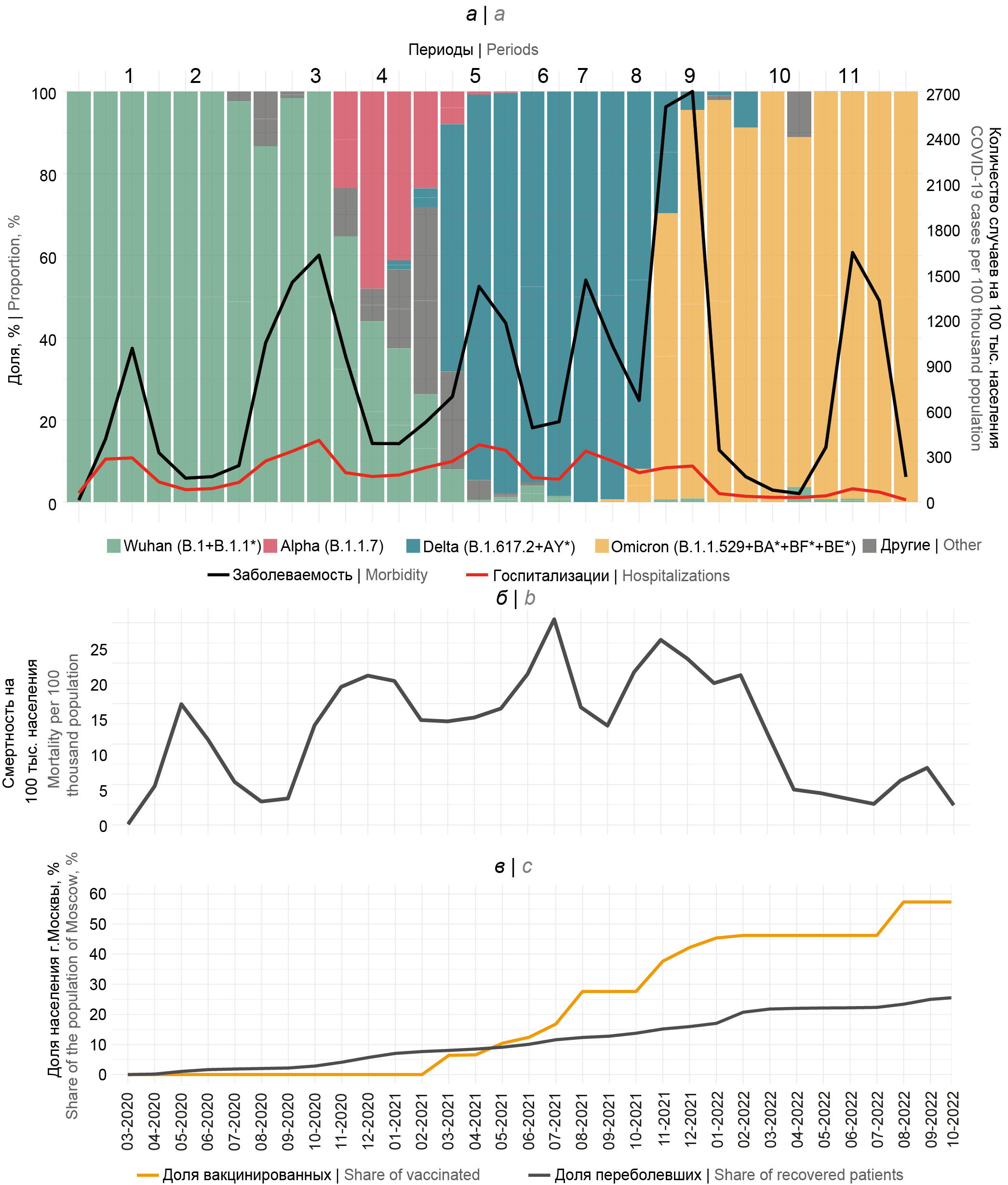
Введение. Постоянная оценка динамики основных характеристик эпидемического процесса является базовой функцией эпидемиологического надзора за инфекционными заболеваниями. Поиск факторов, определяющих изменения характеристик эпидемического процесса, позволяет своевременно вырабатывать управленческие решения и снижать риск увеличения масштабов пандемии. Москва является основным центром притяжения населения других регионов России с наиболее сложной структурой социальных связей и самой высокой плотностью населения.
Цель и задачи исследования — выявить факторы, потенциально определяющие тенденции наблюдаемых изменений, с помощью молекулярно-эпидемиологического анализа основных характеристик эпидемического процесса новой коронавирусной инфекции (COVID-19).
Материалы и методы. Для проведения анализа данные Российской национальной базы геномных последовательностей вируса SARS-CoV-2 (VGARus) были объединены с информацией о заболеваемости и смертности, представленными на официальных интернет-ресурсах стопкоронавирус.рф и Yandex DataLens, о динамике вакцинации, перенесённом заболевании COVID-19 и госпитализации с портала Gogov.ru. Для изучения половой и возрастной структуры госпитализированных пациентов проведено многоцентровое ретроспективное наблюдательное эпидемиологическое исследование. Источником данных для анализа половозрастной структуры послужили истории болезни пациентов с COVID-19, собранные в различные периоды наблюдения на базе учреждений города Москвы (41 561 наблюдение).
Результаты. Выделено 11 периодов, достоверно различающихся по комплексу эпидемиологических характеристик. Выявлено снижение заболеваемости среди молодых людей трудоспособного возраста во время действия ограничительных мероприятий. В 3 из 11 периодов ухудшение эпидемической ситуации совпало с началом циркуляции нового генетического варианта возбудителя COVID-19 (варианты Ухань, Дельта, Омикрон). Отмечено снижение заболеваемости в летний период вне зависимости от циркулирующих генетических вариантов.
Заключение. Существенная часть наблюдаемой динамики характеристик эпидемического процесса в Москве может объясняться свойствами возбудителя, сезонностью и динамикой напряжённости иммунитета. Влияние динамики показателей напряжённости коллективного иммунитета на ход эпидемического процесса предстоит изучить дополнительно.
 267-284
267-284


Спектр и функциональные свойства мутаций гена ERG11 флуконазол-резистентных грибов Candida albicans, выделенных от ВИЧ-инфицированных пациентов
Аннотация
Актуальность. Низкая эффективность терапии кандидозной инфекции азоловыми препаратами, особенно у ВИЧ-инфицированных пациентов, зачастую связана с гиперэкспрессией в грибах Candida spp. гена ERG11, которая обусловливает повышение объёма синтеза эргостерола — мишени данных препаратов. Обнаружены мутации гена ERG11, способные модифицировать эффекты его гиперэкспрессии путём как усиления, так и снижения. Однако сведения, полученные в различных лабораториях и странах, весьма противоречивы.
Цель работы — исследовать спектр и функциональные свойства мутаций гена ERG11 в устойчивых к флуконазолу штаммах Candida albicans, выделенных от ВИЧ-инфицированных пациентов.
Материалы и методы. Исследование выполнено на 10 штаммах грибов C. albicans, выделенных из ротоглотки ВИЧ-инфицированных пациентов и изначально устойчивых к действию флуконазола и вориконазола, из коллекции Московского научно-исследовательского института эпидемиологии и микробиологии им. Г.Н. Габричевского. Штаммы были охарактеризованы по чувствительности к антимикотическим препаратам: анидулафунгину, микафунгину, каспофунгину, позаконазолу, вориконазолу, итраконазолу, флуконазолу, амфотерицину В, 5-флуцитозину. Уровень экспрессии гена ERG11 измеряли с помощью количественной ПЦР. Мутации гена ERG11 выявляли путём его секвенирования по Сэнгеру.
Результаты. В 7 штаммах C. albicans в структуре гена ERG11 были обнаружены 5 вариантов мутаций (E266D, G464S, I471L, D116E и V488I), 6 штаммов оказались носителями сочетанных мутаций, которые не имели сопряжения. В 6 исследованных штаммах C. albicans была установлена повышенная экспрессия гена ERG11. Для мутации V488I была характерна сильная отрицательная связь с повышенной экспрессией гена ERG11 (r = –0,845; p < 0,05). Минимальная ингибирующая концентрация (МИК) штаммов — носителей мутации была на 2 порядка ниже (p < 0,05), чем штаммов без мутаций. У носителей мутаций МИК позаконазола и итраконазола были в среднем в 16,5 раза ниже, чем МИК вориконазола и флуконазола (p < 0,001). Наличие мутаций в гене ERG11 практически не отражалось на уровне МИК тестированных антимикотиков группы эхинокандинов, полиенов и пиримидина.
Заключение. В большинстве штаммов C. albicans, выделенных от ВИЧ-инфицированных пациентов и устойчивых к флуканазолу и вориконазолу, выявлен ряд мутаций в гене ERG11. За исключением V488I обнаруженные мутации не имели сопряжения с повышенной экспрессией гена ERG11 и снижали эффекты гиперэкспрессии гена ERG11 до 100 раз, хотя полностью не отменяли исходной резистентности к триазоловым препаратам.
 285-292
285-292


Оценка изменений фенотипа, интенсивности дегрануляции, гибели и лизиса нейтрофилов при моделировании ex vivo стафилококковой бактериемии
Аннотация
Введение. В настоящее время актуальным является изучение взаимодействия Staphylococcus аureus с клетками врождённого иммунитета человека в условиях моделирования бактериемии ex vivo, а не только в опытах с предварительно выделенными из крови фагоцитами.
Цель: сравнительная оценка изменений фенотипа, интенсивности аэурофильной дегрануляции, гибели и лизиса нейтрофилов в образцах цельной крови от условно здоровых доноров при добавлении живых и убитых микробных клеток S. aureus АТСС 6538 (209-P).
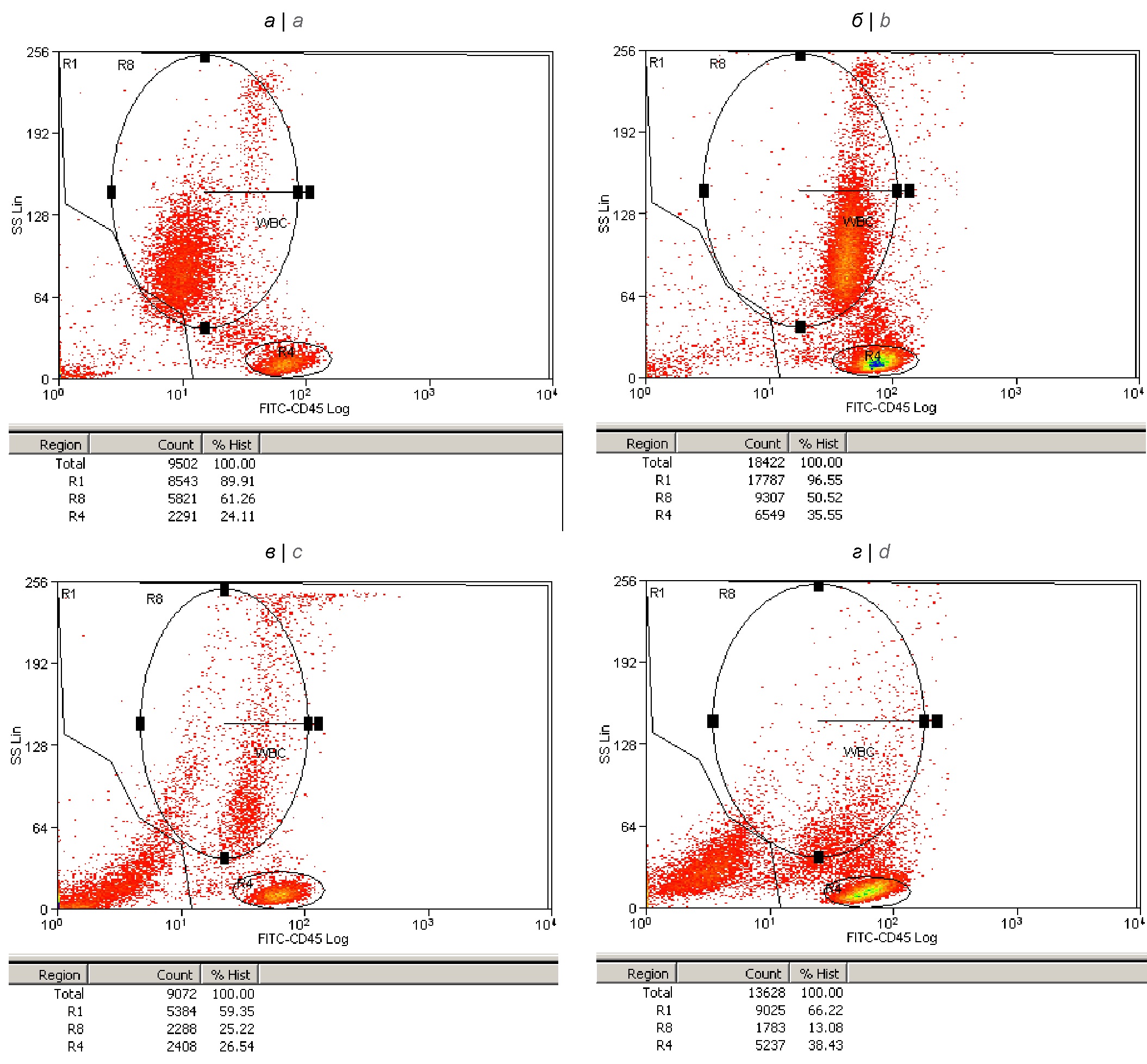
Материалы и методы. Бактериемию моделировали добавлением микробов в цельную кровь (с гепарином) в дозах 108–101 м.к./мл. Бактерицидный эффект определяли в различные сроки инкубации крови при 37оС (в течение 6 ч) микробиологическим методом. С помощью проточной цитометрии в крови проводили по протоколу Lyse/No-Wash иммунофенотипирование лейкоцитов для определения на поверхности нейтрофильных гранулоцитов (НГ) экспрессии маркеров азурофильной дегрануляции (СD63), раннего апоптоза (CD95) и клеточной адгезии (CD62L), а также для оценки плотности поверхностной экспрессии молекулярного триггера нетоза FcᵧRIIIb (СD16) и тирозиновой протеинфосфатазы (СD45), являющейся регулятором FcR-опосредованной передачи клеточных сигналов при фагоцитозе и нетозе. Наличие дегенеративных изменений в НГ подтверждали с помощью микроскопии при анализе мазков крови, окрашенных по Романовскому–Гимзе.
Результаты. Выявлены выраженные различия в реакции НГ крови человека на живые и убитые клетки S. aureus по исследуемым фенотипическим показателям. Только живые микробы запускали в НГ азурофильную дегрануляцию и стимулировали, начиная с 2 ч, появление в крови большого числа НГ с фенотипом СD95+. Кроме того, живые бактерии вызывали в фагоцитах вдвое более интенсивную функциональную перестройку по экспрессии СD45. Они индуцировали быстрое снижение плотности экспрессии СD16 на НГ и активировали в крови лизис НГ с интенсивностью, зависящей от исходной микробной концентрации. При концентрациях более 105 м.к./мл с помощью технологии проточной цитометрии регистрировали через 6 ч присутствие в крови характерной для сепсиса популяции нейтрофилов низкой плотности (с фенотипом CD63+СD16low), склонных к спонтанному аутолизису (нетозу).
Заключение. В условиях моделирования бактериемии ex vivo оценены различные стратегии нейтрофилов крови человека в реализации механизмов защиты макроорганизма от инфекции и определена перспектива применения полученных сведений для выявления лиц с высоким риском развития стафилококкового сепсиса.
 293-305
293-305


Молекулярно-генетическая характеристика и филогенетический анализ возбудителей норовирусной инфекции человека отдельных муниципалитетов в Свердловской области за 2022 год
Аннотация
Введение. Норовирусы являются высококонтагиозными возбудителями острой норовирусной инфекции (НВИ) человека. Известно, что превалирующей генетической группой в структуре заболеваемости норовирусным гастроэнтеритом по всему миру является GII. Ранее на территории Свердловской области в отдельных муниципалитетах молекулярно-генетический мониторинг вместе с филогенетическим анализом не проводился, поэтому не предоставляется возможным объективно оценить генетическое разнообразие популяции норовирусов.
Цель работы — выполнить генотипирование и провести филогенетический анализ возбудителей НВИ человека на территории Екатеринбурга, Нижнего Тагила, Каменск-Уральского за 2022 г.
Материалы и методы. Был организован сбор образцов фекального материала от больных детей с НВИ на территории Свердловской области. Все образцы были анализированы методом ПЦР с вырожденными праймерами, фланкирующими регион ORF1/ORF2. Нуклеотидные последовательности участка генома возбудителей НВИ определяли методом секвенирования по Сэнгеру. Был проведен филогенетический анализ консенсусных последовательностей с построением аддитивных филограмм.
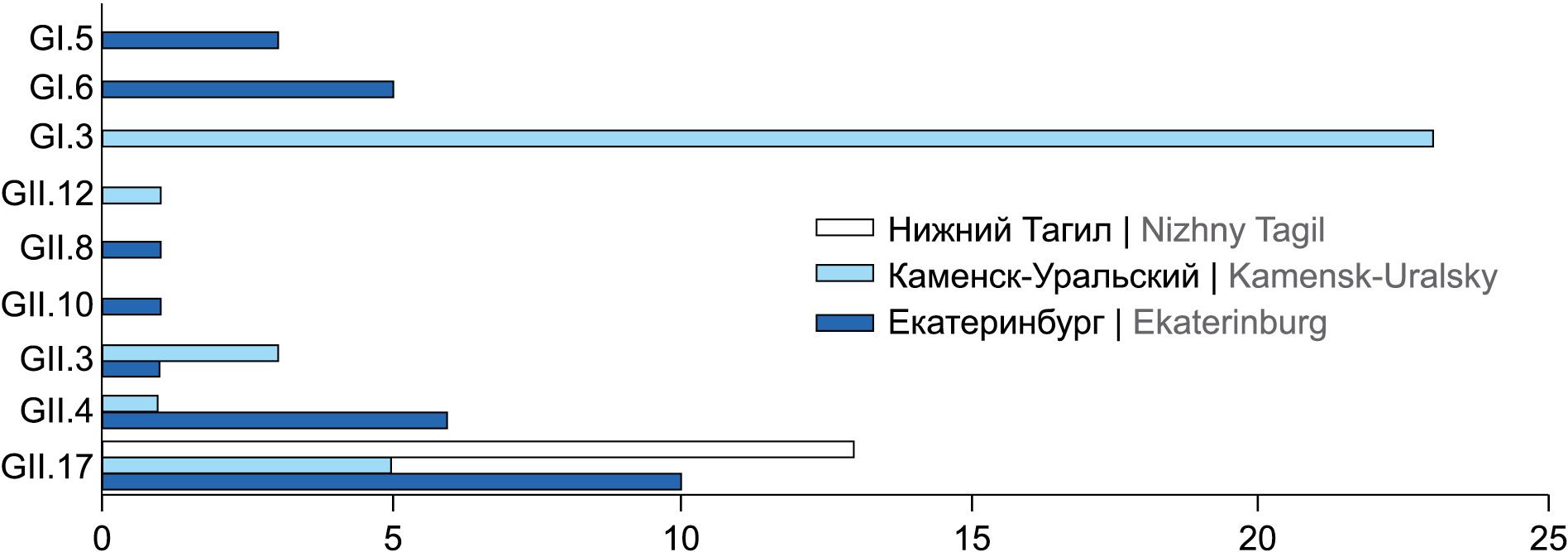
Результаты. Общее количество исследованных образцов составило 220. По результатам секвенирования удалось типировать 73 возбудителя НВИ. Наибольший удельный вес в генотипической структуре занимают норовирусы, относящиеся к геногруппе GII (58%), и норовирусы, относящиеся к геногруппе GI (42%). Норовирусы, относящиеся к генотипам GII.17, GI.3, являются доминирующими вирусами, выявленными на территории отдельных муниципалитетов Свердловской области. Филогенетический анализ демонстрирует, что идентифицированные последовательности на территории Свердловской области обладают наименьшей генетической дистанцией, что даёт основание для их объединения в общий кластер.
Заключение. Впервые на территории Свердловской области был проведён генетический анализ возбудителей. Система генотипирования норовирусов, основанная на амплификации региона ORF1/ORF2, позволяет успешно идентифицировать различные генотипы норовирусов. Было подтверждено, что норовирусы GII остаются доминирующей генетической группой. Результаты филогенетического анализа демонстрируют наибольшую гомологию в сформированных кластерах между изолятами из Екатеринбурга, Нижнего Тагила, Каменск-Уральского.
 306-313
306-313


Анализ энтомологических показателей и распространение личинок Aedes aegypti в эндемичных по лихорадке денге районах
Аннотация
Введение. Причиной эндемичности лихорадки денге является плотность популяции личинок комеров-переносчиков, основным из которых являются Aedes aegypti. Муниципалитет Бандунг является эндемичным районом с высоким уровнем заболеваемости лихорадкой денге. Следовательно, изучение характеристик среды обитания комаров рода Aedes имеет важное значение для контроля популяций комаров.
Целью данного исследования было выявление мест размножения личинок комаров рода Aedes и взаимосвязь между индексом риска размножения, индексом гигиенического риска, индексом Майя и наличием личинок с заболеваемостью лихорадкой денге.
Материалы и методы. В данном исследовании использовался метод перекрёстного опроса. Объём простой случайной выборки составил 544 дома.
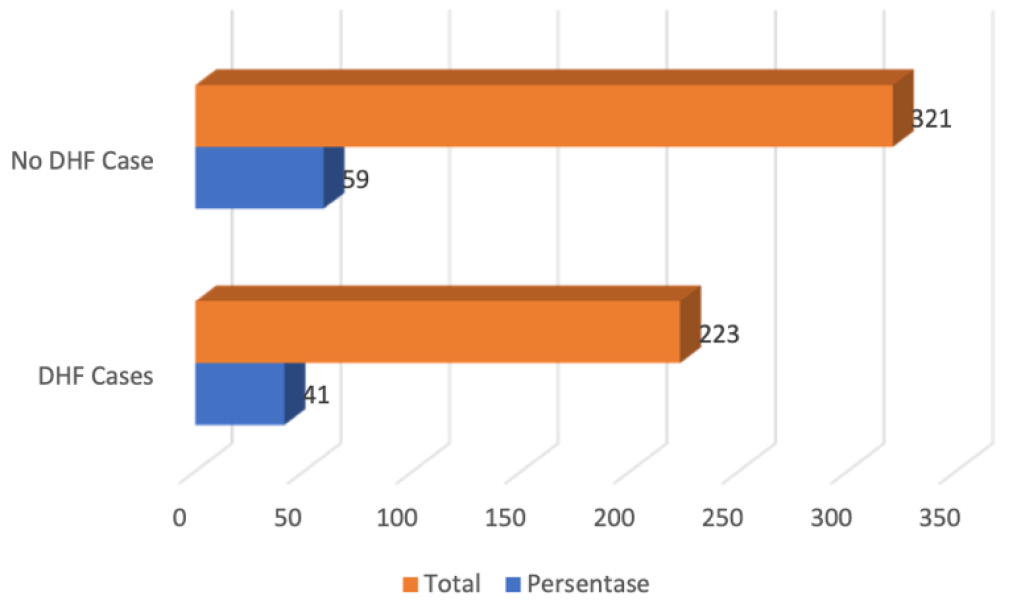
Результаты. Полученными энтомологическими показателями были индекс дома (23,89%), индекс контейнера (7,81%), индекс Брето (50,73%) и количество объектов, свободных от личинок (76,10%). Индекс риска размножения, индекс гигиенического риска и индекс Майя относятся к низкой категории. Тест χ2 показал, что индекс риска размножения, индекс Майя и наличие личинок были в значительной степени связаны с заболеваемостью лихорадкой денге.
Заключение. Энтомологический индекс может влиять на высокую заболеваемость лихорадкой денге. Эти выводы и результаты могут помочь властям оптимизировать программу по ликвидации мест размножения комаров с целью предотвратить распространение лихорадки денге.
 314-320
314-320


Антибиотикорезистентность и вирулентность карбапенем-устойчивых штаммов Klebsiella pneumoniae, выделенных у детей в реанимационных и хирургических отделениях
Аннотация
Введение. Инфекции, ассоциированные с карбапенемрезистентной (Карба-Р) Klebsiella pneumoniae (KP), представляют собой серьёзную проблему здравоохранения, поскольку приводят к увеличению длительности пребывания в стационаре, затрат на лечение, повышению заболеваемости и смертности пациентов.
Цель — охарактеризовать антибиотикорезистентность, вирулентные свойства и генотипы Карба-Р-штаммов KP, выделенных от пациентов, находившихся в реанимационных и хирургических отделениях.
Материалы и методы. В 2018–2020 гг. было собрано 455 штаммов KP, не чувствительных к меропенему и/или имипенему либо чувствительных к меропенему и/или имипенему при увеличенной экспозиции. Для дальнейшего исследования было отобрано 90 изолятов KP, выделенных из клинически значимых локусов: крови/ликвора/мочи/нижних дыхательных путей/ран/брюшной полости пациентов реанимационных и хирургических отделений. Чувствительность к антимикробным препаратам определяли методом микроразведений в бульоне. Гены карбапенемаз детектировали методом ПЦР в режиме реального времени. Гены вирулентности и принадлежность к К1/К2-капсульным серотипам определяли методом мультиплексной ПЦР. Сиквенс-типы (ST) были определены с помощью мультилокусного сиквенс-типирования.
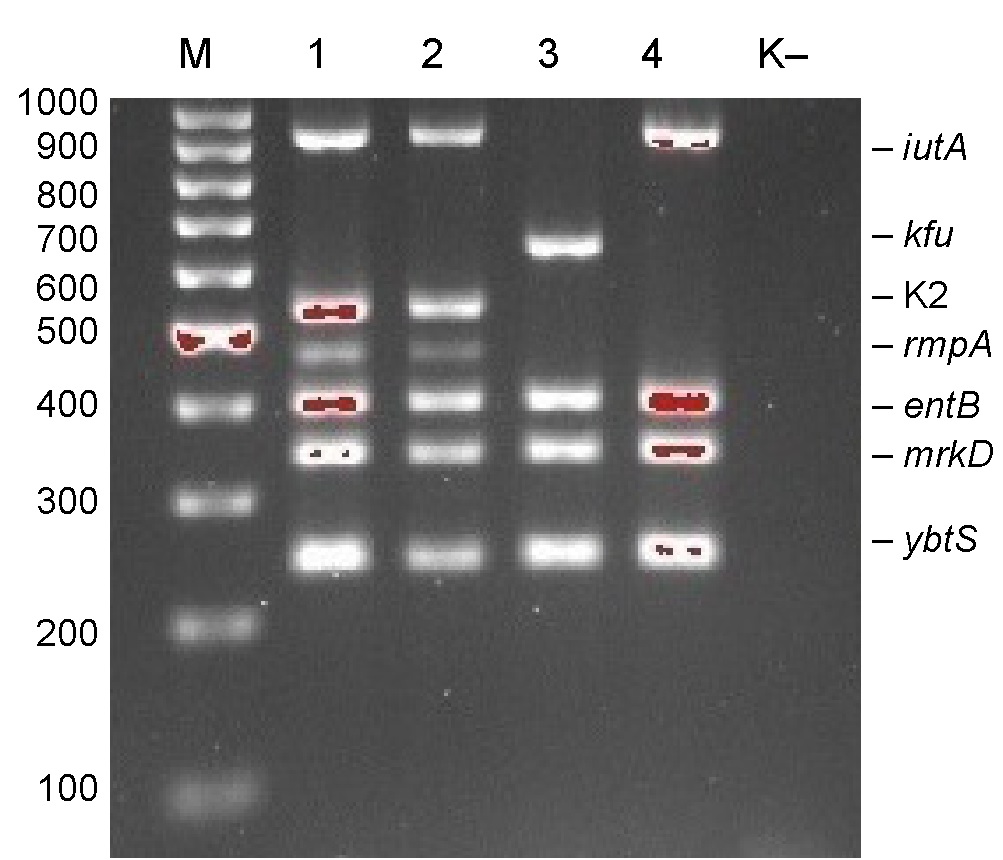
Результаты. Большинство отобранных штаммов (97%) продемонстрировали фенотип широкой лекарственной устойчивости, 3 изолята обладали фенотипом множественной лекарственной устойчивости. Главной детерминантой резистентности была карбапенемаза группы OXA-48 (53%), у 13% штаммов выявлена металло-бета-лактамаза группы NDM, сочетание карбапенемаз NDM и OXA-48 обнаружено у 31% изолятов. Два штамма обладали карбапенемазой группы KPC. У большинства изолятов встречались гены вирулентности entB (100%), mrkD (99%) и ybtS (78%). У 16% штаммов был найден ген iutA. Четыре изолята показали наличие генов kfu, и у 4 штаммов был найден ген rmpA. К серотипу K2 принадлежали 13% изолятов. В исследованной популяции преобладали ST: ST395 (26%), ST2975 (19%), ST198 (12%) и ST307 (11%).
Заключение. Карба-Р-изоляты KP имели высокий уровень устойчивости не только к карбапенемам, но и к антибиотикам других классов. Устойчивость к карбапенемам главным образом была обусловлена карбапенемазой OXA-48. Главными детерминантами вирулентности были entB, mrkD и ybtS. Преобладающими генетическими линиями были эпидемически успешные клоны CG395 и CG307. Резистентность к антимикробным препаратам сочеталась с наличием различных факторов вирулентности. Полученные данные важны для эпиднадзора за распространением KP и имеют важное клиническое значение.
 321-332
321-332


ОБЗОРЫ
Современное представление о диареегенных Escherichia coli — возбудителях острых кишечных инфекций
Аннотация
Острые кишечные инфекции, обусловленные Escherichia coli, характеризуются поражением желудочно-кишечного тракта с развитием диарейного синдрома, интоксикации и в некоторых случаях генерализации патологического процесса. Диареегенные E. coli (DEC) отличаются от непатогенных (комменсальных) штаммов наличием определённых генов вирулентности, особенностями патогенеза и клинико-эпидемиологическими проявлениями вызываемых ими заболеваний. В соответствии с детерминантами вирулентности выделяют 6 патогенных групп DEC: энтеропатогенные, энтеротоксигенные, энтероинвазивные, шигатоксин-продуцирующие, энтероагрегативные, диффузно-адгерентные. Штаммы каждой группы характеризуются конкретными патогенетическими механизмами, обеспечивающими развитие воспалительного процесса в разных отделах кишечника человека, клинически проявляющегося диарейным синдромом. В статье представлен обзор современной научной литературы по эпидемиологии, патогенезу, генетическим свойствам и антигенной характеристике патогенных E. coli. Несмотря на многолетнее и разностороннее изучение биологических свойств DEC, многие аспекты биологии этого вида требуют более углублённого анализа знаний, необходимых для разработки эффективных методов лабораторной диагностики, лечения, проведения противоэпидемических мероприятий и профилактики эшерихиозов.
 333-344
333-344


Система секреции 4-го типа у Clostridioides difficile: структурные особенности и её роль как фактора патогенности
Аннотация
Clostridioides difficile — грамположительный микроорганизм, вызывающий поражения стенки кишечника человека, которые проявляются клинически в виде антибиотикоассоциированной диареи и псевдомембранозного колита. Проблема инфекции C. difficile не теряет актуальности, а с распространением внутрибольничных вспышек и появлением внебольничных форм растёт потребность в новых видах её профилактики и лечения. Патогенез инфекции C. difficile связан с продукцией бактериями токсинов и большой группы иных белков, благоприятствующих размножению патогена в тканях макроорганизмов и его распространению в популяции людей. Исходя из исследований последних лет можно заключить, что высокой вирулентности C. difficile способствуют мобильные генетические элементы. Важнейшими компонентами этих элементов являются системы секреции 4-го типа (СС4Т), впечатляющее разнообразие которых среди грамположительных микроорганизмов вообще и C. difficile в частности говорит об их высокой эволюционной и, следовательно, медицинской значимости. Дальнейшее изучение состава и строения СС4Т позволит расширить понимание механизмов развития соответствующих инфекций и наметить патогенетически обоснованные подходы к профилактике и лечению заболеваний, вызываемых C. difficile. С другой стороны, ключевые компоненты секреторного аппарата патогена могут быть использованы для биоинформационного анализа и поиска новых адаптивных кластеров в геноме высоковирулентных штаммов.
 345-353
345-353


Перспективные фармацевтические разработки вакцин для профилактики менингококковой инфекции
Аннотация
Менингококковая инфекция (МИ) относится к антропонозам; представляет собой острое инфекционное заболевание с аэрозольным механизмом передачи, характеризующееся различными формами инфекционного процесса: от локальной (назофарингит) и бессимптомной до генерализованных форм в виде инвазивной инфекции с развитием менингококкцемии и менингита. Возбудителем МИ является менингококк (Neisseria meningitidis), относящийся к III группе патогенности. Профилактические прививки против МИ включены в календарь профилактических прививок по эпидемическим показаниям. Проблема МИ имеет важное медико-социальное значение для российского здравоохранения в связи с сохраняющимися высокими показателями летальности, инвалидизацией, высокими затратами на лечение и реабилитацию. В мире зарегистрированы вакцины против 5 из 6 основных серогрупп N. meningitidis. Вакцина против серогруппы X находится на стадии разработки. В последнее время отмечается увеличение гетерогенности популяции менингококка, обусловленное серогруппами W, Y и Х. Разработанные в России полисахаридные вакцины имеют ограничения по применению, а производство по полному циклу на территории России конъюгированных менингококковых вакцин отсутствует. Учитывая вышеизложенное, разработка и регистрация новых вакцин против МИ является актуальной задачей.
Цель работы — анализ современного состояния в области разработок вакцин для профилактики МИ.
В зависимости от технологии получения имеются следующие виды менингококковых вакцин: полисахаридные, конъюгированные, на основе везикул наружной мембраны (ВНМ), белковые и на основе синтетических полисахаридов. Менингококковые вакцины, направленные к отдельным серогруппам, являются эффективными в снижении бремени инвазивной МИ для общественного здравоохранения. Полисахаридные конъюгированные и белковые/ВНМ вакцины относятся к наиболее перспективным вакцинам и нацелены на борьбу с большинством инвазивных серогрупп менингококка.В современных условиях с развитием технологий в области создания полисахаридных конъюгированных вакцин будущего открываются новые возможности использования таких подходов, как химический/химико-ферментный синтез, улучшенная характеристика белка-носителя и сайт-специфическая конъюгация. Не теряет своей актуальности разработка единой вакцины против основных инвазивных серогрупп менингококка, а не его отдельных антигенных вариантов. Своевременной является разработка вакцины против N. meningitidis серогруппы X, являющейся редкой причиной возникновения спорадического менингита и вызвавшей вспышки в 2006–2010 гг. в различных странах Африки.
 354-363
354-363


Видовая характеристика бактерий рода Lactobacillus, циркулирующих в различных локусах организма человека (обзор литературы)
Аннотация
Бактерии рода Lactobacillus — это обитатели поверхностей слизистых оболочек человека: ротовой полости, пищеварительного и урогенитального тракта; они обнаруживаются также в грудном молоке и мокроте. Ввиду многочисленных генетических различий, метаболических способностей и других функций видов, включённых в этот род, в 2020 г. предложено пересмотреть классификацию рода Lactobacillus. В последнее время в научной медицинской литературе активно обсуждаются вопросы влияния лактобактерий на микробиом человека, поддержание здоровья и предупреждение патологических состояний организма. Настоящий обзор посвящён функциональным характеристикам и анализу видового разнообразия Lactobacillus spp., циркулирующих в различных системах организма, участию их в формировании и регулировании защитных механизмов. Вместе с тем отмечаются и негативные воздействия, связанные чаще всего с передачей генетических детерминант резистентности к антимикробным препаратам от лактобацилл к грамотрицательной микробиоте.
 364-375
364-375


ЮБИЛЕИ
 376-378
376-378


 379-380
379-380