Том 100, № 3 (2023)
- Год: 2023
- Выпуск опубликован: 11.07.2023
- Статей: 12
- URL: https://microbiol.crie.ru/jour/issue/view/178
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Итоги многоцентрового мониторинга возбудителя инвазивного листериоза в мегаполисе
Аннотация
Введение. Инвазивный листериоз — редкое заболевание, опасное для групп риска и часто приводящее к летальному исходу. Возбудитель — Listeria monocytogenes — убиквитарный сапрофит, ставший актуальным патогеном пищевого происхождения с развитием индустрии полуфабрикатов и продуктов быстрого приготовления.
Цель работы — характеристика изолятов L. monocytogenes в Московском регионе и определение возможных причин восприимчивости к инфекции.
Материалы и методы. Проведён многоцентровой мониторинг L. monocytogenes в Московском регионе с применением бактериологических и геномных методов в описании возбудителя, сбора анамнеза и подробного анализа эпикриза пациентов.
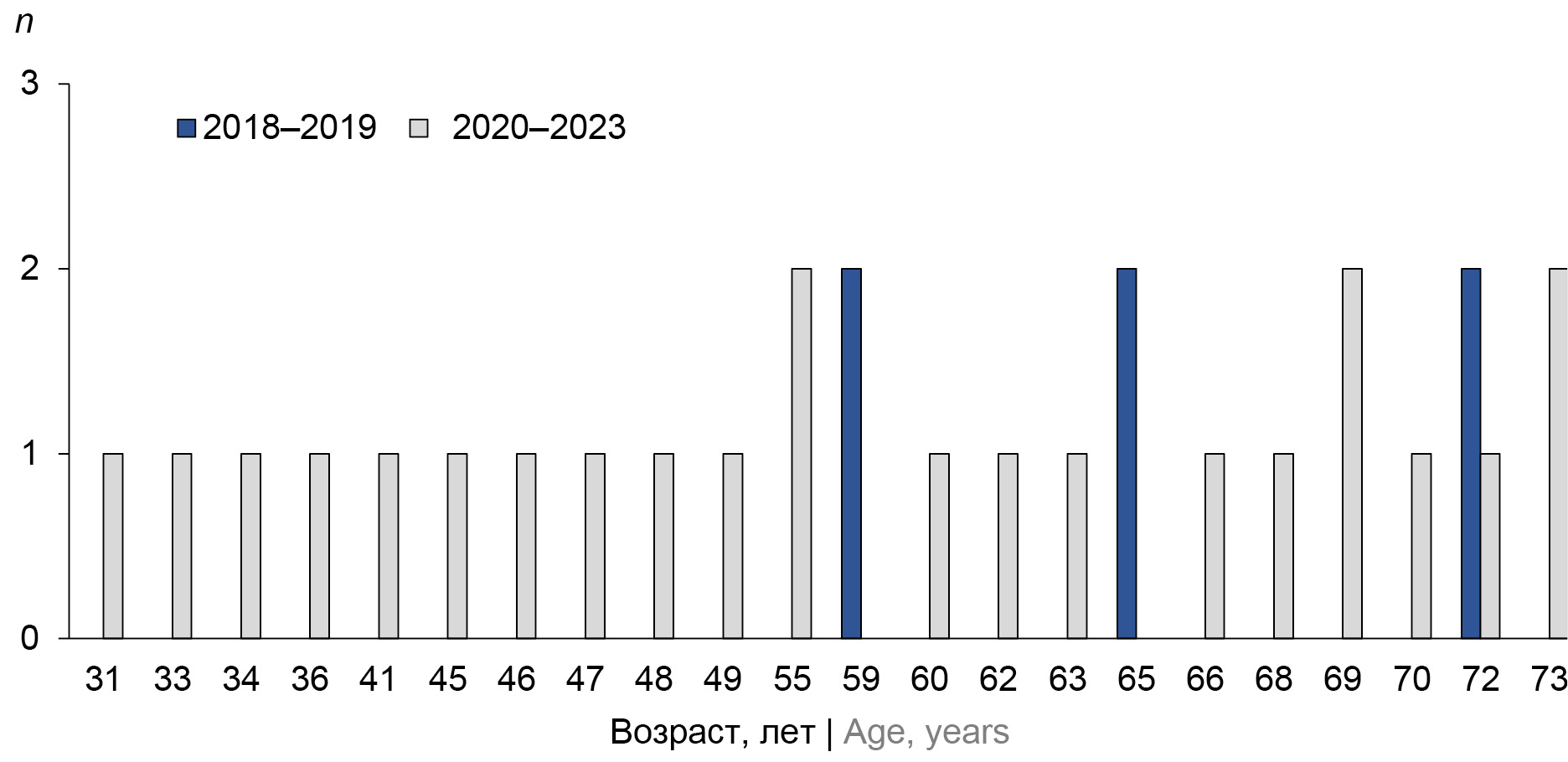
Результаты. В когортах перинатальный листериоз (ПЛ) и менингит-септицемия (МС) инвазивный листериоз встречался во все месяцы года с небольшими подъёмами в марте–апреле и июле–ноябре. В период пандемии COVID-19 в группе МС минимальный возраст пациентов снизился до 31 года, доля умерших выросла в 1,57 раза по сравнению с 2018–2019 гг. В период пандемии наблюдали рост разнообразия генотипов L. monocytogenes и изменения в спектре генотипов возбудителя на этапах пандемии.
За всё время мониторинга охарактеризовали 73 клинических изолята L. monocytogenes, относящихся к 24 генотипам. Семь генотипов принадлежали к первой филогенетической линии (PLI), 14 генотипов — к PLII. В когорте ПЛ была самая высокая доля генотипов PLI (52%). В когорте МС в группе мужчин отметили наибольшее разнообразие генотипов, 6 из которых совпадали с генотипами пищевых изолятов. В выборке изолятов описали 12 новых профилей генов интерналинов. Полногеномное секвенирование показало наличие плазмид в 9 из 58 геномов клинических изолятов. Сопоставление коровых геномов выявило эпидемическую связь между изолятами одного генотипа в отношении ST4, ST21, ST425.
Заключение. Проведённое исследование предоставило подробное описание разнообразия и вирулентности L. monocytogenes, циркулирующих в Московском регионе, что будет способствовать своевременной диагностике и лечению инвазивного листериоза.
 143-154
143-154


Анализ in silico геномов штаммов Bacillus anthracis главных генетических линий
Аннотация
Введение. Филогенетическая структура глобальной популяции Bacillus anthracis представлена главными генетическими линиями A, B и C c неравной распространённостью изолятов, причина которой неизвестна. Определение особенностей геномов штаммов трех линий, которые могут влиять на распространённость, является актуальным.
Цель — характеристика особенностей геномов разных генетических линий, потенциально влияющих на их распространённость, с использованием анализа in silico представительной выборки штаммов B. anthracis
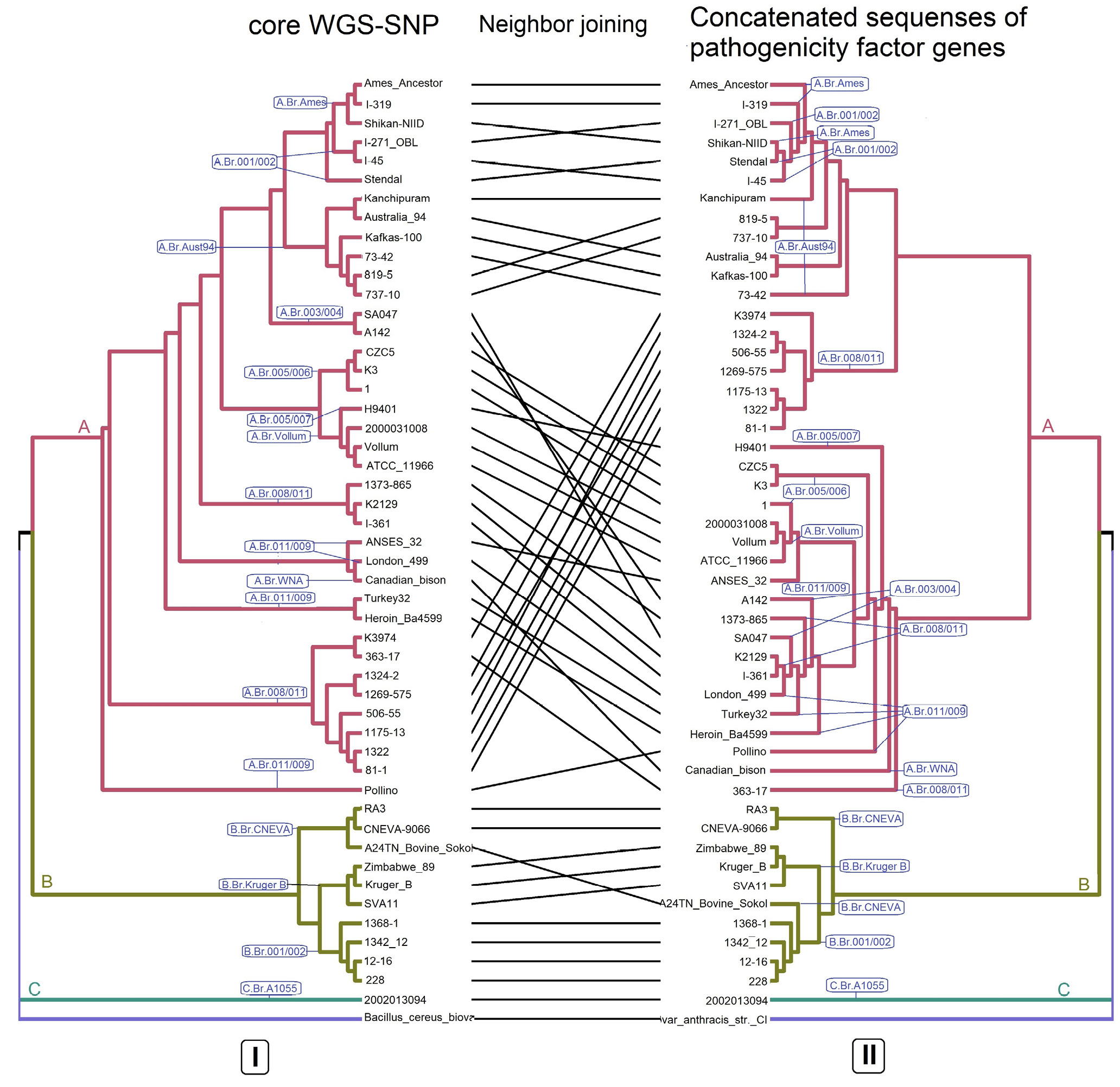
Материалы и методы. Изучены полногеномные последовательности 49 штаммов B. anthracis и штамма CI B. cereus biovar anthracis. Анализ in silico проводили с идентификацией полиморфизмов в программах «BLASTn», «MEGA X», «Tandem Repeat Finder», «Parsnp» из пакета «Harvest Suite».
Результаты. Вариабельность геномов определялась однонуклеотидными полиморфизмами, однонуклеотидными повторами, числом тандемных повторов, заменами и инделами. Их количество у штаммов линий B и С было в 1,6–13,4 раза больше, а у штамма B. cereus biovar anthracis — в 5–150 раз больше, чем у штаммов B. anthracis линии A. Значимые замены в генах домашнего хозяйства и факторов патогенности приводили к изменению аминокислотной последовательности белков также значительно чаще у штаммов B. anthracis главных линий B, C.
Молекулярное типирование на основе анализа однонуклеотидных полиморфизмов генов факторов патогенности (MVLST) с индексом дискриминации 0,9633 разделяло штаммы на три главные генетические линии с группами, отличающимися от канонических.
Заключение. Главное отличие геномов B. anthracis состоит в большом количестве значимых нуклеотидных замен в генах факторов патогенности и «домашнего хозяйства» штаммов главных линий B и C по сравнению с линией A. Изменения в кодируемых ими белках могут определять разную экологическую адаптацию и распространённость, более высокие у линии A. MVLST с высокой дискриминирующей способностью может быть дополнительным методом молекулярного типирования B. anthracis.
 155-165
155-165


Разнообразие СRISPR-локусов штаммов Yersinia pseudotuberculosis и их ассоциация с факторами патогенности возбудителя
Аннотация
Актуальность. Постоянный обмен наследственной информацией с участием внехромосомных и транспозируемых элементов является одним из факторов существования гетерогенных популяций микроорганизмов. Структуры, контролирующие горизонтальный перенос генов, могут влиять на формирование генетических вариантов патогенов.
Цель работы — изучить молекулярно-генетические характеристики CRISPR-локусов штаммов Yersinia pseudotuberculosis, циркулирующих на территории России, и их связь с факторами патогенности возбудителя псевдотуберкулёза.
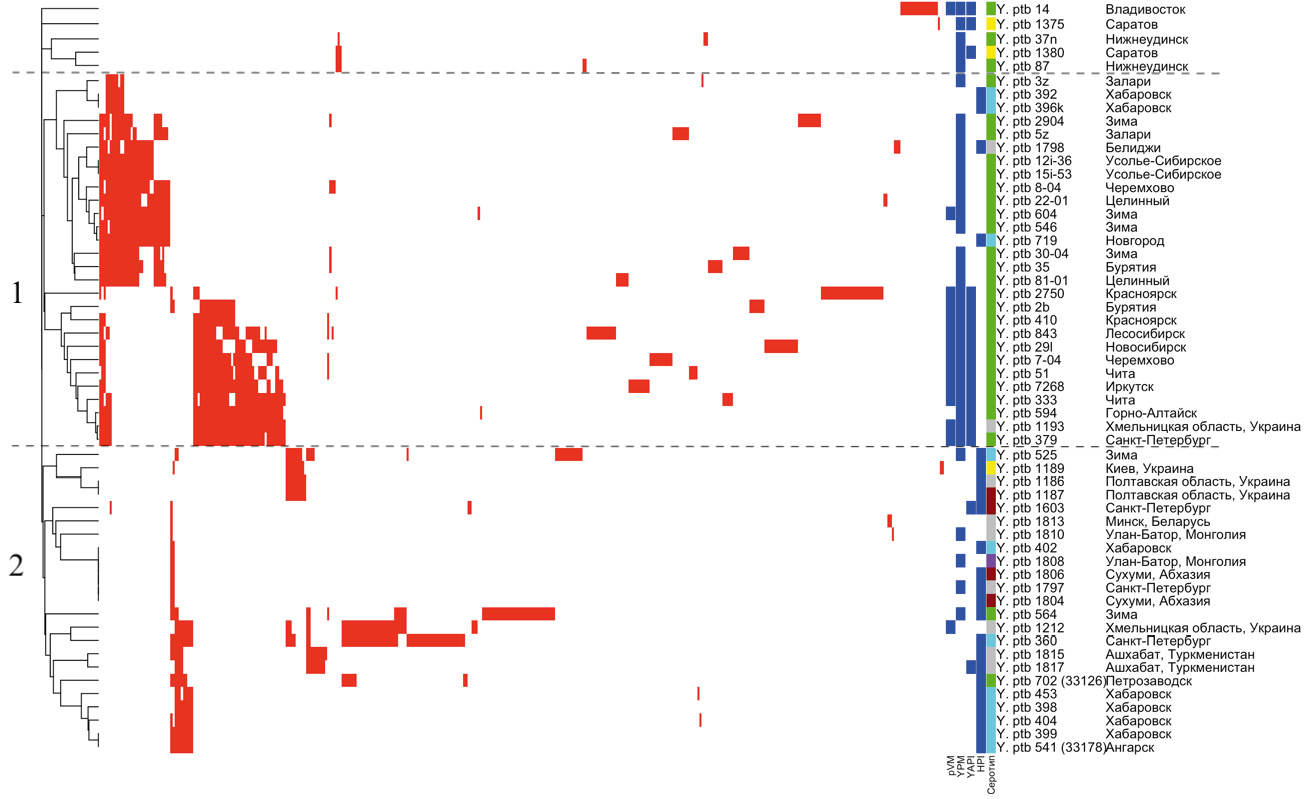
Материалы и методы. В работе изучены 56 штаммов Y. pseudotuberculosis, выделенных в течение 1935–2014 гг. на различных территориях России и других государств из разных источников. Выделение и амплификацию фрагментов ДНК, содержащих CRISPR-локусы, выполняли методом полимеразной цепной реакции. Секвенирование CRISPR-локусов осуществляли по методу Сэнгера. Для каждого штамма определён генотип по наличию основных факторов патогенности: хромосомных генов суперантигена ypmА/С, генов, локализованных на «островах патогенности» HPI, YAPI, генов плазмиды pYV, pVM82.
Результаты. В результате анализа CRISPR-локусов штаммов Y. pseudotuberculosis установлено, что спейсерный состав локусов различается у штаммов, отличающихся серотипом, набором факторов патогенности, регионом выделения. Наиболее вариабельны локусы YP1 и YP3, локус YP2 однороден. Состав локуса YP1 различается в группах штаммов, отличающихся по наличию плазмиды pVM82. Состав локуса YP3 зависит и от наличия плазмиды pVM82, и от «адгезивного острова патогенности» YAPI.
Заключение. На территории России циркулируют штаммы Y. pseudotuberculosis с различным набором детерминант вирулентности и спейсерным составом СRISPR-локусов. Большинство российских штаммов отличаются по данным молекулярным маркерам от штаммов из других стран. Высокая вариабельность штаммов внутри вида определяется способностью приобретать новые генетические элементы путём горизонтального переноса генов. CRISPR-Cas как система «иммунитета» бактерий против мобильных генетических элементов может участвовать в формировании патогенного потенциала штаммов Y. pseudotuberculosis.
 166-175
166-175


Патогенетическая роль цитокинов при геморрагической лихорадке с почечным синдромом в динамике и при различной степени тяжести
Аннотация
Цель работы — определение взаимосвязи между уровнями цитокинов провоспалительного и противовоспалительного действия в динамике геморрагической лихорадки с почечным синдромом (ГЛПС) и зарегистрированными ранее особенностями фенотипического состава лимфоцитов крови при заболевании разной степени тяжести.
Материалы и методы. Под наблюдением находились 65 пациентов с серологически верифицированным диагнозом ГЛПС. Контрольная группа включала 15 условно здоровых людей. Уровень цитокинов (интерлейкинов (ИЛ), интерферонов (ИФН), фактора некроза опухоли (ФНО)) в крови пациентов с ГЛПС определяли методом иммуноферментного анализа по периодам заболевания. Фенотипический состав лимфоцитов крови изучали методом проточной цитофлуориметрии.
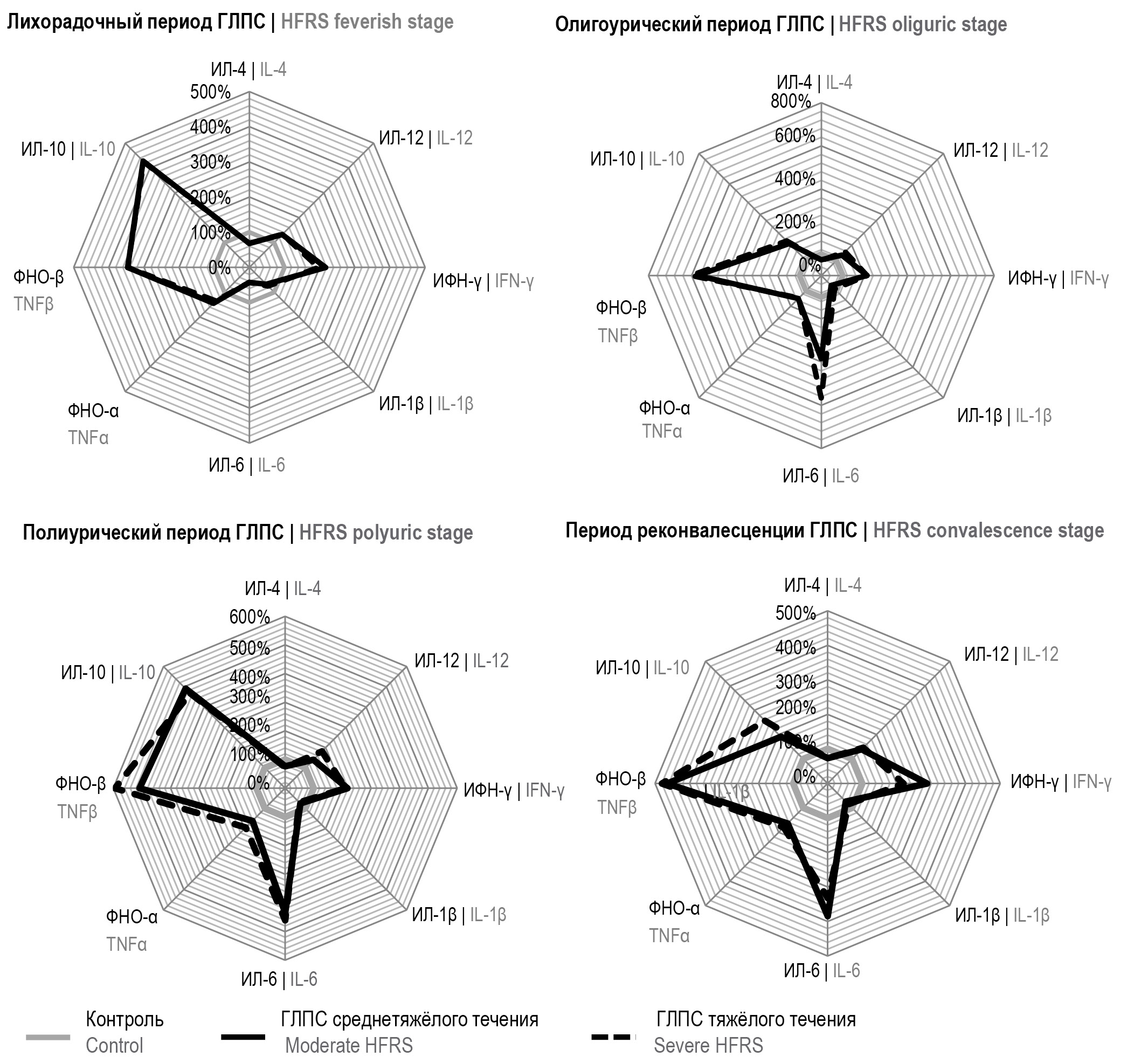
Результаты. В разные периоды заболевания отмечен количественно различный рост содержания в крови цитокинов, сопряжённых с цитотоксическими иммунными реакциями (ИЛ-12, ИФН-γ, ФНО-α, ФНО-β), а также ИЛ-10 и ИЛ-6, корреляционно связанных между собой при тяжёлом течении, на фоне падения в крови уровней ИЛ-4 и ИЛ-1β. При среднетяжёлом течении ГЛПС отмечены корреляции уровней ИЛ-12 и ИЛ-4 с NKG2D+ цитотоксических Т-лимфоцитов (ЦТЛ), участие ИЛ-12 во взаимосвязях практически со всеми остальными цитокинами, корреляционная связь CD8+-регуляторных Т-клеток (Трег) с уровнями ИЛ-6 и ФНО-α. При тяжёлом течении отмечено образование комплекса, в состав которого входят связанные между собой ИЛ-6 и ИЛ-10, образующие корреляции с числом NKG2D+-ЦТЛ, СD8+-Трег, подобных натуральным киллерам Т-лимфоцитов (НКТ).
Заключение. Патогенетически значимый механизм ГЛПС реализуется с преимущественным участием цитокинов клеточного иммунного ответа и ИЛ-6, корреляционно связанных с NKG2D+-ЦТЛ, СD8+-Трег, НКТ, способствующих в случае благоприятного исхода активному формированию пула CD8+-клеток памяти, предположительно нарушаемому при избыточной секреции ИЛ-10.
 176-185
176-185


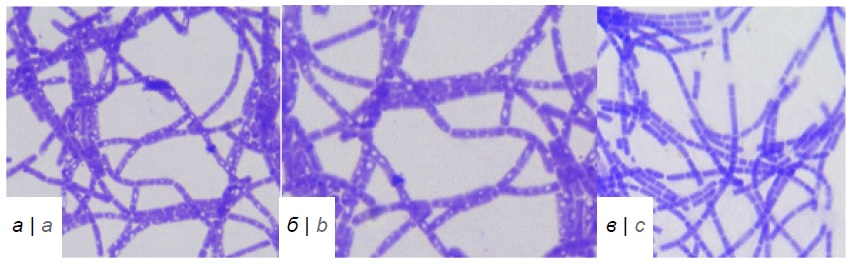
Способность к вегетированию и спорообразованию штаммов Bacillus anthracis c различными фенотипическими свойствами в условиях, имитирующих почву
Аннотация
Введение. Изучение способности штаммов Bacillus anthracis с различающимися фенотипическими свойствами к герминации спор, размножению и спорообразованию на среде, основой которой является водный экстракт почвы, может способствовать оценке значимости этих процессов в формировании и поддержании почвенных очагов сибирской язвы.
Цель работы — анализ индивидуальных особенностей развития вегетативной культуры штаммов возбудителя сибирской язвы с различным фенотипом на модели почвенной среды.
Материалы и методы. На группе штаммов сибиреязвенного микроба, имеющих разный плазмидный состав и вирулентность, исследована возможность прорастания спор, размножения бацилл и, по крайней мере у некоторых из них, продуктивное спорообразование на почвенной среде.
Результаты. Выявлены три варианта развития культуры штаммов B. anthracis: 1 — споры остаются интактными, не прорастая; 2 — после герминации спор формируются бациллы, которые с различной интенсивностью размножаются, переходя в инволюционные формы без образования спор; 3 — прохождение полного физиологического цикла «спора–бацилла–спора». Наличие 2% крови в почвенной среде способствовало прорастанию спор и размножению культуры, но тормозило процесс спорообразования в период наблюдения — 3 сут. Не выявлено корреляции между определённым фенотипом изученных штаммов B. anthracis и способностью к прорастанию и вегетации на почвенных средах.
Обсуждение. Полученные данные о том, что только 1–7% КОЕ даёт начало формированию колоний на почвенной среде, позволяют предположить неоднородность свойств популяции использованных штаммов. Выделение таких культур и их дальнейшее подробное изучение позволит выявить наиболее значимые для осуществления полного физиологического цикла в условиях, имитирующих почву, комплексы биологических свойств.
 186-193
186-193


Состояние специфического иммунитета населения Республики Таджикистан к вирусам кори, краснухи, полиомиелита
Аннотация
Актуальность. Для достижения целей программ элиминации кори, краснухи, искоренения полиомиелита необходим охват иммунизацией не менее 95% целевого населения. Объективные данные о состоянии специфического иммунитета представляют только результаты серологических исследований популяционного иммунитета. В Республике Таджикистан такой мониторинг регулярно не проводится, поэтому целью нашего исследования являлась оценка фактического состояния специфического иммунитета населения к инфекциям, вызываемым вирусами кори, краснухи, полиомиелита.
Материалы и методы. Исследовали 563 сыворотки крови детей и взрослых, собранные в 7 городах и 13 районах Таджикистана в 2020 г. Уровень антител (АТ) к вирусам кори определяли методом иммуноферментного анализа с помощью тест-системы «ВектоКорь-IgG» («Вектор Бест»), АТ к вирусу краснухи — с помощью тест-системы «Эколаб». Нейтрализующие АТ (нАТ) к 3-м типам полиовируса (ПВ) определяли в 359 сыворотках с помощью реакции нейтрализации со штаммами Сэбина типов 1, 2, 3.
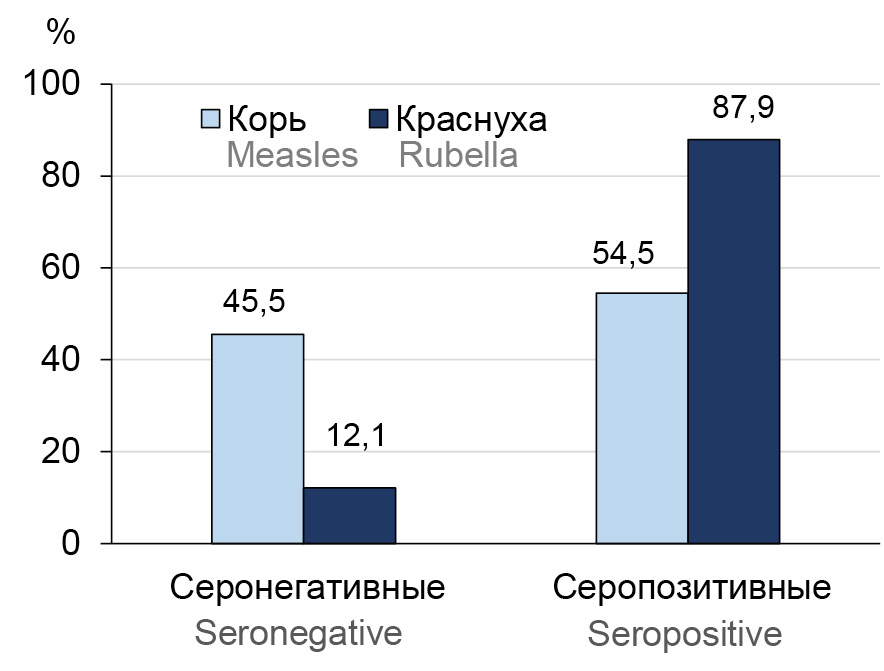
Результаты. Уровень серопревалентности к краснухе составил 87,9%, в том числе в группе детей — 86,2%, подростков — 93,1%, взрослых — 93,5%, что достаточно для предотвращения трансмиссии вируса. Доля серопозитивных к кори 54,5% недостаточна для предотвращения устойчивой вторичной передачи инфекции и возобновления циркуляции эндемичного штамма вируса кори. Детское население до 15 лет следует считать группой риска инфицирования, поскольку из 45,5% серонегативных на детей приходилось 38%.
В целом нАТ к ПВ имели менее 95% обследованных: 94,4% к ПВ1, 86,1% к ПВ2, 83,6% к ПВ3; 3,3% не имели АТ ко всем трём типам ПВ. Уровень популяционного иммунитета различался в группах обследованных в зависимости от схемы вакцинации и состава применяемых полиовирусных вакцин: нАТ к ПВ2 имели 59,6% детей, рождённых в период, когда вакцины, содержащие ПВ2, не применялись, а также 85,7% детей, рождённых после внедрения трёхвалентной инактивированной поливакцины. Дефицит иммунитета к ПВ2 стал в 2021 г. причиной вспышки полиомиелита, вызванной циркулирующим ПВ2 вакцинного происхождения.
Заключение. Определён высокий уровень гуморального иммунитета к вирусу краснухи. Выявлены недостатки плановой иммунопрофилактики в отношении кори и полиомиелита, связанные с недостаточным охватом и отсутствием вакцины. Проведение регулярного серологического мониторинга в Республике Таджикистан целесообразно для получения объективной информации об уровне популяционного иммунитета, выявления уязвимых групп населения, планирования дополнительных иммунизационных мероприятий.
 194-202
194-202


Сравнительная оценка ферментативной и биоцидной активности Candida auris и Candida albicans
Аннотация
Введение. Важную роль в реализации патогенности Candida spp. играют секретируемые продукты метаболизма, обладающие ферментативными или токсическими свойствами. Наиболее клинически значимым видом считается C. albicans, однако всё большую актуальность приобретает C. auris, часто вызывающая инвазивные инфекции.
Цель работы — сравнение некоторых ферментативных свойств и биоцидной активности C. auris и C. albicans.
Материалы и методы. Исследования проводили на штаммах C. albicans и C. auris. Оценивали рост микромицетов на мясо-пептонном агаре, среде Сабуро или кровяном агаре (с учётом гемолиза). Способность Candida spp. расщеплять белки выявляли на агаре Дифко с 2% казеином и по воздействию на молекулы IgG. Липазную активность кандид определяли на агаре, содержащем Твин-20. Жизнеспособность буккальных эпителиоцитов после воздействия (1–4 ч) метаболитов кандид оценивали с помощью трипанового теста. Статистическую обработку проводили с использованием программы «RStudio».
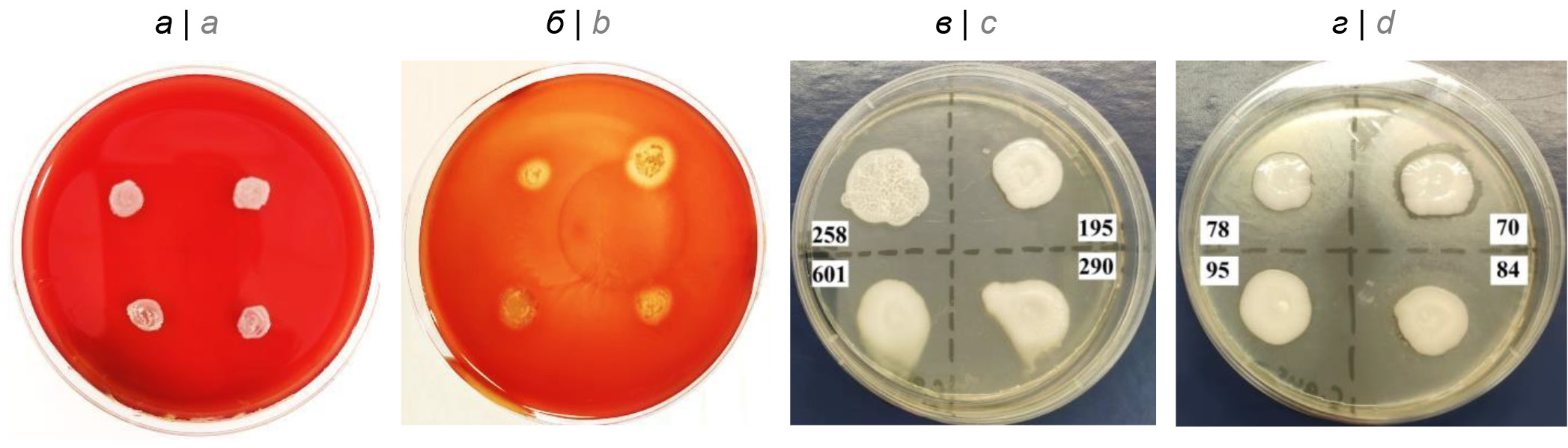
Результаты. C. albicans лучше всего росли на агаре Сабуро, а C. auris — на кровяном агаре. Гемолитическая и липазная активность была характерна только для C. auris. Наличие протеазной активности было отмечено для некоторых штаммов C. auris: они были способны расщеплять казеин и повреждать структуру молекул IgG. Продукты метаболизма некоторых штаммов кандид снижали жизнеспособность эпителиальных клеток, при этом кратность снижения была более выражена в экспериментах с C. auris (р < 0,05).
Заключение. Наиболее благоприятной средой для культивирования C. auris является кровяной агар. Выраженная протеолитическая, антиглобулиновая, гемолитическая и общая липазная активности были отмечены только у исследуемых штаммов C. auris, что показывает их более высокий инвазивный потенциал по сравнению с C. albicans. Биоцидная активность микромицетов в отношении буккальных эпителиоцитов имела штамм-зависимый характер.
 203-209
203-209


НАУКА И ПРАКТИКА
Применение иммуномагнитной сепарации для ускоренного обнаружения клеток F. tularensis в образцах почвы с помощью иммунохроматографического теста
Аннотация
Введение. Эпизоотологический мониторинг заражённости территории возбудителем туляремии предполагает сбор и исследование разнообразного полевого материала. Анализ таких объектов занимает длительное время и достаточно трудоёмок. В связи с этим существует потребность в разработке простых и быстрых диагностических методик, позволяющих проводить анализ образцов в условиях ограниченных ресурсов.
Цель работы — изучить возможность применения иммуномагнитной сепарации (ИМС) для ускоренной детекции клеток Francisella tularensis в образцах почвы с использованием иммунохроматографии.
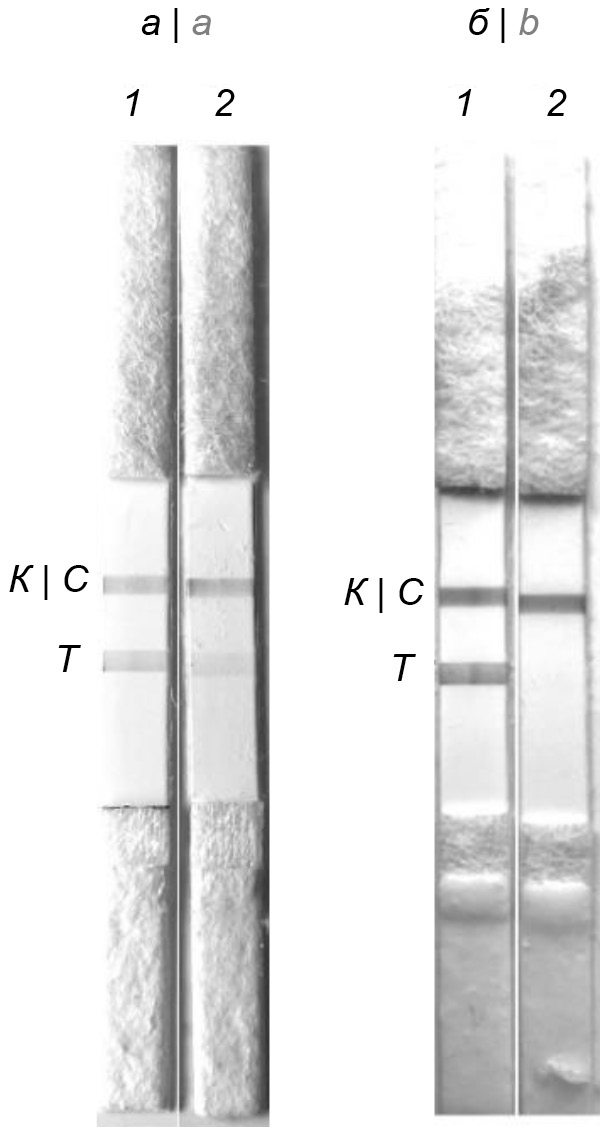
Материалы и методы. Иммуномагнитные частицы получали на основе моноклональных антител к липополисахариду возбудителя туляремии. Для исследования использовали образцы почвы массой 1 г, в которые предварительно вносили инактивированные клетки F. tularensis 15/10. Образцы почвы перемешивали в экстрагирующем буфере, фильтровали и проводили сепарацию туляремийных клеток с помощью суспензии иммуномагнитных частиц. Частицы отмывали, ресуспендировали в экстрагирующем буфере и прогревали при 100ºС в течение 5 мин. Супернатант анализировали с помощью тест-полосок «ИХ-тест F. tularensis».
Результаты. Применение сочетания метода ИМС и иммунохроматографического теста для детекции клеток F. tularensis позволило обнаружить до 1 × 106 клеток возбудителя туляремии в исследуемых образцах почвы, в то время как в пробах почвы без ИМС выявлено 1 × 107 клеток.
Выводы. Разработана методика, основанная на использовании ИМС и иммунохроматографического теста, открывающая перспективы ускоренной диагностики заражённости образцов почвы в очаге туляремийной инфекции. Время проведения анализа — около 3 ч. Чувствительность определения возбудителя — 1 × 106 микробных клеток в 1 г образца почвы. Методика проста, не требует сложного, дорогостоящего оборудования и может быть легко адаптирована для тестирования образцов другого происхождения (вода, зерно и др.). Полученные в процессе сепарации бактериальные клетки могут быть переданы для детекции F. tularensis другими методами.
 219-224
219-224


Получение Bst-полимеразы для диагностики различных инфекций методом петлевой изотермической амплификации
Аннотация
Введение. Большой фрагмент ДНК-полимеразы I из Geobacillus stearothermophilus GIM1.543 (ДНК-полимераза Bst) обладает 5'-3'-ДНК-полимеразной активностью, 5'-3'-вытесняющей активностью и высокой процессивностью. Благодаря этим свойствам ДНК-полимераза Bst используется в петлевой изотермической амплификации (LAMP), которая обеспечивает амплификацию целевой последовательности с высокой специфичностью и применяется для быстрого обнаружения возбудителей инфекционных заболеваний человека.
Цель работы — получение рекомбинантного фермента Bst-полимеразы в бактериальной системе экспрессии и оценка его свойств в условиях LAMP для диагностики инфекционных заболеваний.
Материалы и методы. Методами генетической инженерии получали экспрессионные конструкции, несущие ген Bst-полимеразы. Экспрессию белка проводили в различных штаммах клеток Escherichia coli. Для получения очищенных препаратов белка использовали методы металл-хелатной и гель-фильтрационной хроматографии. Оценку каталитических свойств фермента проводили в реакциях петлевой изотермической амплификации в диагностических системах «АмплиСенс® SARS-CoV-2-IT», «АмплиСенс® IAV-IT» и «АмплиСенс® IBV-IT», предназначенных для качественного определения РНК SARS-CoV-2, вируса гриппа А (IAV) и вируса гриппа B (IBV) соответственно.
Результаты. Разработанный протокол наработки, выделения и очистки рекомбинантной Bst-полимеразы позволяет получать фермент в бактериальной системе экспрессии на основе клеток E. coli в растворимой форме с выходом до 20% от собранной клеточной массы. В реакциях LAMР полученный фермент демонстрирует активность, сопоставимую с коммерческим ферментом Bst 2.0 («NEB»).
Заключение. Полученная рекомбинантная Bst-полимераза, учитывая быстрый способ очистки и получения фермента, пригодна для применения в диагностических наборах на основе LAMP.
 210-218
210-218


ОБЗОРЫ
Живые аттенуированные вакцины против COVID-19: подходы к разработке и перспективы клинического применения
Аннотация
Несмотря на объявленное ВОЗ завершение пандемии, COVID-19 остаётся актуальной проблемой здравоохранения во всём мире. Современные вакцины зачастую формируют либо только гуморальный, либо только клеточный иммунитет. Кроме того, появление и распространение новых эпидемиологически значимых вариантов SARS-CoV-2 значительно снижает эффективность вакцинопрофилактики. Всё это требует совершенствования существующих вакцин против COVID-19. Одним из возможных подходов к решению данной проблемы является создание «универсальной» вакцины, обладающей перекрёстной протективной активностью в отношении разных антигенных вариантов вируса. В связи с этим представляет интерес разработка живой аттенуированной вакцины, способной активировать не только гуморальное, но и клеточное звено иммунитета, обеспечивая продолжительный иммунный ответ и перекрёстную защиту от разных вариантов вируса.
В данном обзоре рассматриваются реализованные подходы к получению аттенуированных штаммов SARS-CoV-2 и оценивается потенциал их клинического применения. Одни авторы для аттенуации вируса используют методы генной инженерии и обратной генетики, такие как сайт-направленный мутагенез и деоптимизация кодонов. Другие используют традиционный подход, направленный на получение мутантов вируса путём длительного пассирования в культуре клеток в селективных условиях. Накопленный на сегодняшний день опыт показывает большой потенциал создания высокоэффективной живой аттенуированной вакцины против COVID-19.
 225-236
225-236


Основные группы адъювантов и перспективы их использования для специфической профилактики особо опасных и других инфекционных болезней
Аннотация
Цель данного обзора — анализ опубликованных в последние десятилетия научных работ, посвящённых изучению адъювантной способности веществ различного происхождения и химической природы (адъювантов), и оценка эффективности их применения для вакцинопрофилактики различных инфекций, в том числе особо опасных.
Проведённый анализ литературы, представленной в базах PubMed, Web of Science, Scopus, eLibrary, свидетельствует о том, что поиск новых веществ и препаратов, обладающих способностью усиливать иммунный ответ на антигены, входящие в состав антибактериальных и противовирусных зарегистрированных вакцин, а также экспериментальных профилактических препаратов, является важным и перспективным направлением. Использование различных веществ и соединений в качестве адъювантов усиливает иммуногенную и протективную способность вакцин, позволяет уменьшить антигенную нагрузку на организм человека и создать напряженный иммунный ответ у лиц со сниженной иммунологической активностью и пожилого возраста. При выборе адъюванта необходимо учитывать направленность его действия на формирование как местного, так и системного специфического иммунного ответа в зависимости от характера возбудителя.
 237-246
237-246


Кишечная микробиота и канцерогенез: актуальные аспекты
Аннотация
Микробиота совместно с хозяином формируют симбиотические отношения, в которых микробиота играет ключевую роль в поддержании гомеостаза организма человека, выполняя значимые функции: энергетический обмен, созревание и поддержание иммунной системы, синтез витаминов, регуляцию обратного всасывания в кишечнике желчных кислот и др. Научные исследования последних лет внесли значительный вклад в понимание сложной связи между микробиотой и рядом патологий человека, включая злокачественные новообразования.
В обзоре рассмотрены механизмы возможного влияния бактерий на развитие и прогрессию рака с акцентом на проканцерогенные свойства микробиоты. Отражено, что важнейшим фактором механизма влияния микробиоты на канцерогенез являются токсины, продуцируемые микроорганизмами, которые индуцируют прямые реакции повреждения ДНК клеток хозяина, вызывая мутации ДНК, нарушения её точной репликации, а также провоцируют нарушение баланса пролиферации и апоптоза клеток хозяина, их быстрое старение и онкогенез. Рассмотрены вероятные механизмы участия микроорганизмов в развитии рака через активацию TLRs и NLRs рецепторов, обладающих опухоль-активирующим эффектом. Приводится краткий обзор механизмов канцерогенеза, связанных с метаболической активностью микробиоты за счёт процессов регуляции выработки вторичных желчных кислот, активации проканцерогенных соединений: фенолов, этанола, сульфидов, аммиака, нитрозаминов. Описано влияние микробиоты на метаболизм половых гормонов и развитие гормонозависимых видов рака, опосредованных механизмами энтерогепатической циркуляции и деконъюгации эстрогенов.
Изучение канцерогенных механизмов действия микробиоты в организме хозяина открывает перспективы разработки новых успешных персонализированных подходов к вопросу диагностики, лечения и профилактики рака. Изменение состава микробиоты должно стать способом борьбы с онкологическими заболеваниями, наряду с хирургическим лечением, химиотерапией, лучевой терапией, таргетной терапией и иммунотерапией.
 247-260
247-260