Том 100, № 2 (2023)
- Год: 2023
- Выпуск опубликован: 22.05.2023
- Статей: 12
- URL: https://microbiol.crie.ru/jour/issue/view/55
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Вирусингибирующая активность комплекса антигенов условно-патогенных бактерий в отношении коронавируса SARS-CoV-2
Аннотация
Введение. Комплекс антигенов условно-патогенных бактерий (КАУПБ) обладает протективным эффектом в отношении вируса гриппа птиц, вируса герпеса 2-го типа и других вирусов, вызывающих острые респираторные вирусные заболевания. В связи с пандемией COVID-19 актуально выяснить, обладает ли КАУПБ протективным эффектом в отношении коронавируса SARS-CoV-2.
Цель работы — изучить in vitro вирусингибирующую активность КАУПБ в отношении лабораторного штамма коронавируса SARS-CoV-2 Dubrovka.
Материалы и методы. В работе использовали клеточную линию Vero CCL-81, мононуклеарные клетки периферической крови человека (МКПК), мышиные моноклональные антиидиотипические антитела, структурно имитирующие биологические эффекты интерферонов (ИФН) человека, лабораторный штамм вируса SARS-CoV-2 Dubrovka. Инфекционную активность вируса определяли двумя методами: титрованием вируса методом предельных разведений на клеточных культурах с оценкой результатов по цитопатическому действию и методом бляшкообразования. Реакция ингибирования вируса поставлена in vitro на клеточной культуре, чувствительной к вирусу SARS-CoV-2, с внесением в клеточную культуру cмеси определённой дозы вируса к двукратным разведениям КАУПБ после предварительного 2-часового взаимодействия препарата с вирусом при 4ºС. Вирусингибирующую активность КАУПБ в отношении SARS-CoV-2 определяли по показателям функциональной активности α/β- и γ-рецепторов ИФН (РИФН) на МКПК человека, индуцированных in vitro КАУПБ и смесью КАУПБ с определённой дозой вируса SARS-CoV-2. Уровень экспрессии РИФН оценивали в реакции непрямой мембранной иммунофлуоресценции.
Результаты. Для выявления ингибирующего белка SARS-CoV-2 поставлена реакция гемагглютинации с эритроцитами кур, мышей, морских свинок и человека. В лизате клеток Vero CCL-81, инфицированных SARS-CoV-2 Dubrovka, обнаружены максимальная гемагглютинирующая активность с эритроцитами морской свинки и низкие титры гемагглютинации в вируссодержащей жидкости. В реакции ингибирования вируса на культуре клеток Vero CCL-81 КАУПБ ингибировал 10 доз SARS-CоV-2 Dubrovka с титром 1 : 32 cо 100% защитой клеточной культуры в течение 8 сут (период наблюдения). КАУПБ индуцировал экспрессию РИФН-α/β и -γ на мембранах МКПК человека при культивировании in vitro и снижал экспрессию РИФН-α/β и -γ при предварительном взаимодействии с SARS-CoV-2 Dubrovka.
Заключение. На основе экспериментальных исследований, включающих реакцию ингибирования вируса на культуре клеток, чувствительных к SARS-CoV-2 Dubrovka, и в реакции непрямой мембранной иммунофлуоресценции с использованием для детекции моноклональных антиидиотипических антител, имитирующих ИФН-подобные свойства, продемонстрировано, что КАУПБ обладает иммуномодулирующей и вирусингибирующей активностью.
 143-152
143-152


Структура ESKAPE-патогенов, изолированных от пациентов отделения реанимации и интенсивной терапии новорождённых Национального госпиталя педиатрии г. Ханой, Социалистическая Республика Вьетнам
Аннотация
Введение. Заболеваемость инфекциями, связанными с оказанием медицинской помощи, является одной из глобальных мировых проблем на современном этапе развития здравоохранения и затрагивает все страны вне зависимости от их экономического статуса. Основными возбудителями этих инфекций являются патогены группы ESKAPE.
Цель исследования — изучить структуру, молекулярные и антигенные характеристики ESKAPE-патогенов, выделенных со слизистых зева и ануса пациентов отделения реанимации и интенсивной терапии новорождённых (ОРИТН), для установления их этиологического значения в возникновении инфекций, связанных с оказанием медицинской помощи.
Материалы и методы. Обследовано 49 детей, в том числе 40 новорождённых, пациентов ОРИТН Национального госпиталя педиатрии г. Ханой. Посев биоматериала (мазки со слизистых зева, ректальные мазки) и выделение бактериальных культур осуществлялись классическим бактериологическим методом. Идентификация изолятов проведена методом масс-спектрометрии. Штаммы Klebsiella pneumoniae изучены методом полногеномного секвенирования.
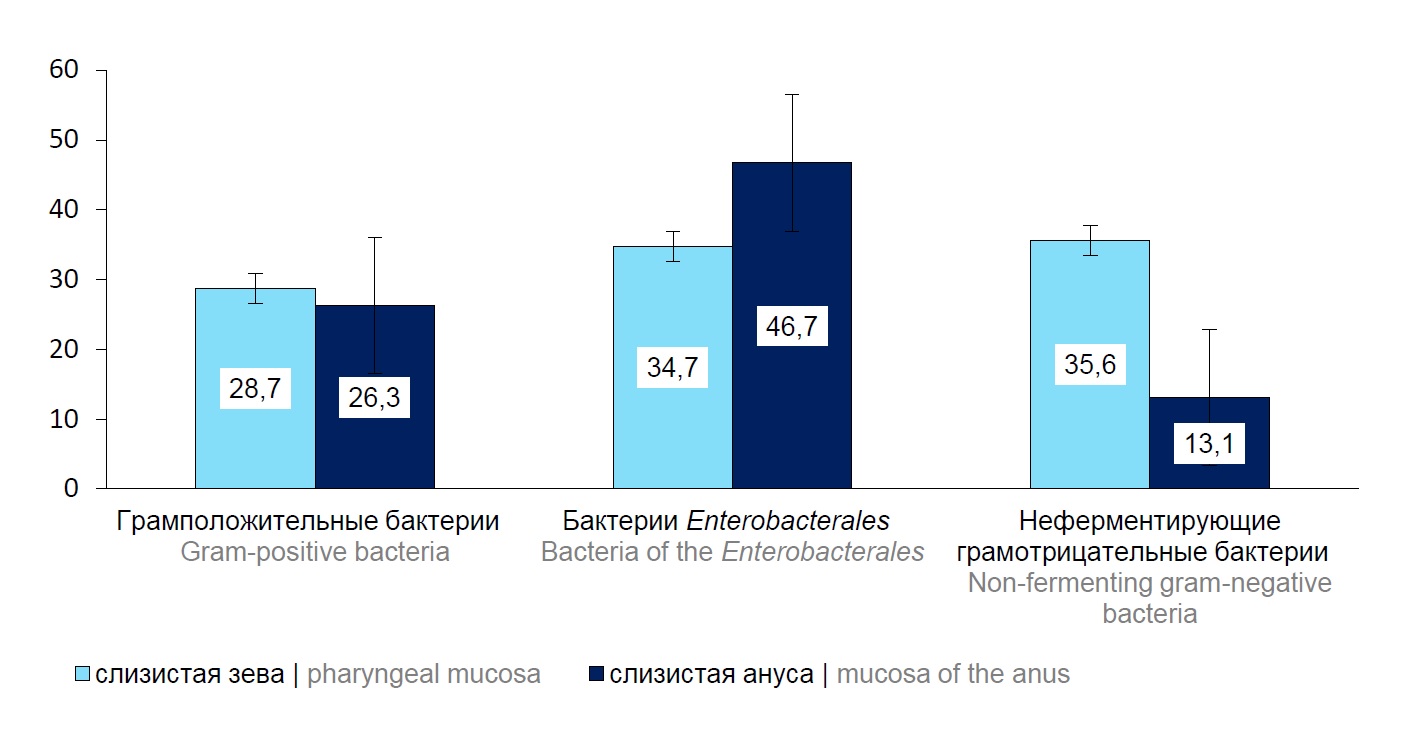
Результаты. Группа грамположительных ESKAPE-патогенов, идентифицированных со слизистой зева, представлена изолятами Enterococcus faecium и Staphylococcus aureus. Среди изолятов семейства Enterobacteriaceae выделены K. pneumoniae, Escherichia coli, Enterobacter cloacae; в группе неферментирующих грамотрицательных бактерий — Pseudomonas aeruginosa, Acinetobacter baumannii. Структура ESKAPE-патогенов, персистирующих на слизистой ануса, характеризовалась преобладанием бактерий Enterococcus spp., E. coli, K. pneumoniae и P. aeruginosa. Результаты полногеномного секвенирования изолятов K. pneumoniae выявили 7 кластеров и 8 сиквенс-типов. Преимущественно определены ST14 и ST1741 — по 25% соответственно от количества исследованных штаммов. Молекулярное серотипирование установило, что по О-антигену штаммы отнесены в основном к серотипам O1v1, О1/О2v2, O5; по наличию капсульного антигена — к серотипам KL2, KL104, KL60.
Заключение. Исследование структуры ESKAPE-патогенов, изолированных со слизистых зева и ануса пациентов ОРИТН Национального госпиталя педиатрии г. Ханой, выявили этиологически значимых возбудителей бактериальных инфекций: S. aureus, K. pneumoniae, E. coli, E. cloacae, P. aeruginosa, A. baumannii. Проведение молекулярно-генетических исследований штаммов K. pneumoniae, циркулирующих одновременно на слизистых нескольких пациентов отделения, позволило установить их гомологию, что указывает на контаминацию детей госпитальными штаммами при оказании медицинской помощи.
 168-177
168-177


Разработка метода молекулярного субтипирования Bacillus anthracis с использованием HRM-ПЦР
Аннотация
Введение. Bacillus anthracis — возбудитель сибирской язвы, патоген, характеризующийся высокой генетической мономорфностью, затрудняющей дифференциацию штаммов, в связи с чем актуальна разработка эффективных методов молекулярного типирования.
Цель исследования. Выбор маркерных однонуклеотидных полиморфизмов (SNP) для типирования генетических групп B. anthracis и разработка метода их лабораторного определения с использованием HRM-ПЦР.
Материалы и методы. Выравнивание корового генома 222 штаммов B. anthracis из базы данных GenBank и 66 штаммов из коллекции патогенных микроорганизмов ФКУЗ «Ставропольский противочумный институт» Роспотребнадзора проводили с использованием программы «Parsnp». Дендрограмму на основе 7242 SNP корового генома построили в программе «MEGA X». Штаммы для валидации метода HRM включали представителей различных генетических групп. Реакцию HRM-ПЦР проводили с использованием наборов «Type-it HRM PCR Kit» и «KAPA HRM FAST qPCR Kit» на амплификаторе ДНК «Rotor Gene» с функцией HRM. Анализ и визуализацию данных выполняли пользовательскими скриптами в среде разработки языка Python и языка R.
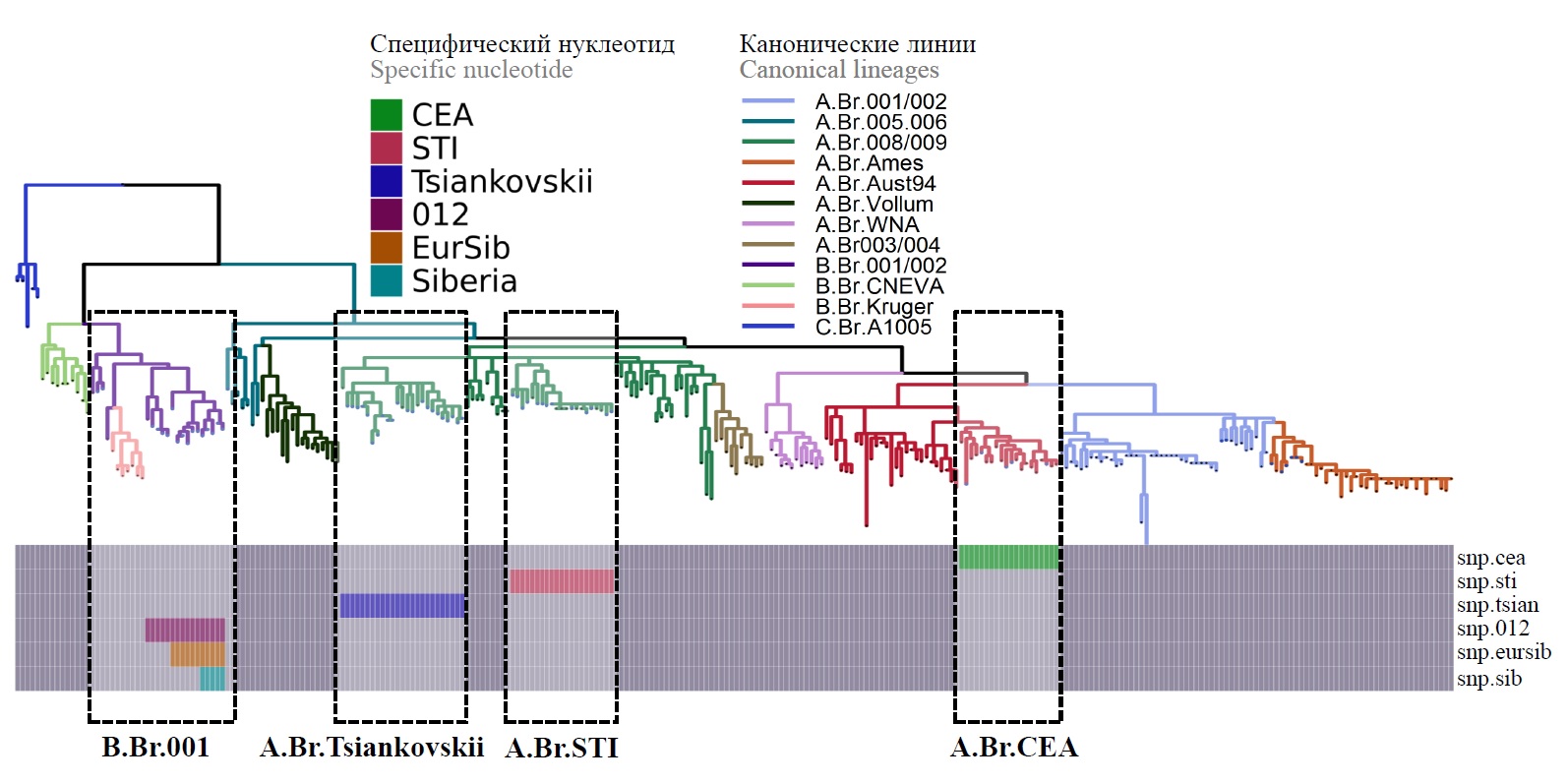
Результаты и обсуждение. Определены маркерные SNP для 6 генетических групп B. anthracis, позволяющие определять принадлежность штаммов к одному из 7 новых субкластеров. Подобраны пары праймеров, оптимизированы параметры HRM-ПЦР для дискриминации разных аллелей SNP-локусов и разработана схема анализа.
Заключение. Таким образом, выбраны маркерные SNP для определения генетических субкластеров B. anthracis A.Br.CEA, A.Br.STI, A.Br.Tsiankovskii, B.Br.Europe, B.Br.Sibеria, B.Br.Asia, B.Br.018 и разработан новый лабораторный метод молекулярного субтипирования B. anthracis с использованием HRM-ПЦР.
 178-187
178-187


Гуморальный иммунитет к коклюшу у медицинских работников
Аннотация
Введение. Вакцинация является самым эффективным способом профилактики инфекционных заболеваний. Недостаточный охват вакцинацией медицинских работников — серьёзная проблема всех учреждений здравоохранения. Отсутствие специфической защиты против коклюша обусловливает риск заболевания медицинских работников, в случае которого они становятся источником инфекции для пациентов. Коклюш — одна из наиболее актуальных вакциноконтролируемых инфекций, до настоящего времени остается проблемой общественного здравоохранения во многих странах, несмотря на высокий охват вакцинацией детей. Ревакцинация взрослых против коклюша не включена в Национальный календарь профилактических прививок Российской Федерации.
Цель работы — оценка гуморального иммунитета к коклюшу у медицинских работников инфекционных стационаров.
Материалы и методы. Проведено поперечное исследование с участием 252 медицинских работников. Участники исследования прошли опрос и были обследованы на антитела (иммуноглобулины G) к Bordetella pertussis методом иммуноферментного анализа.
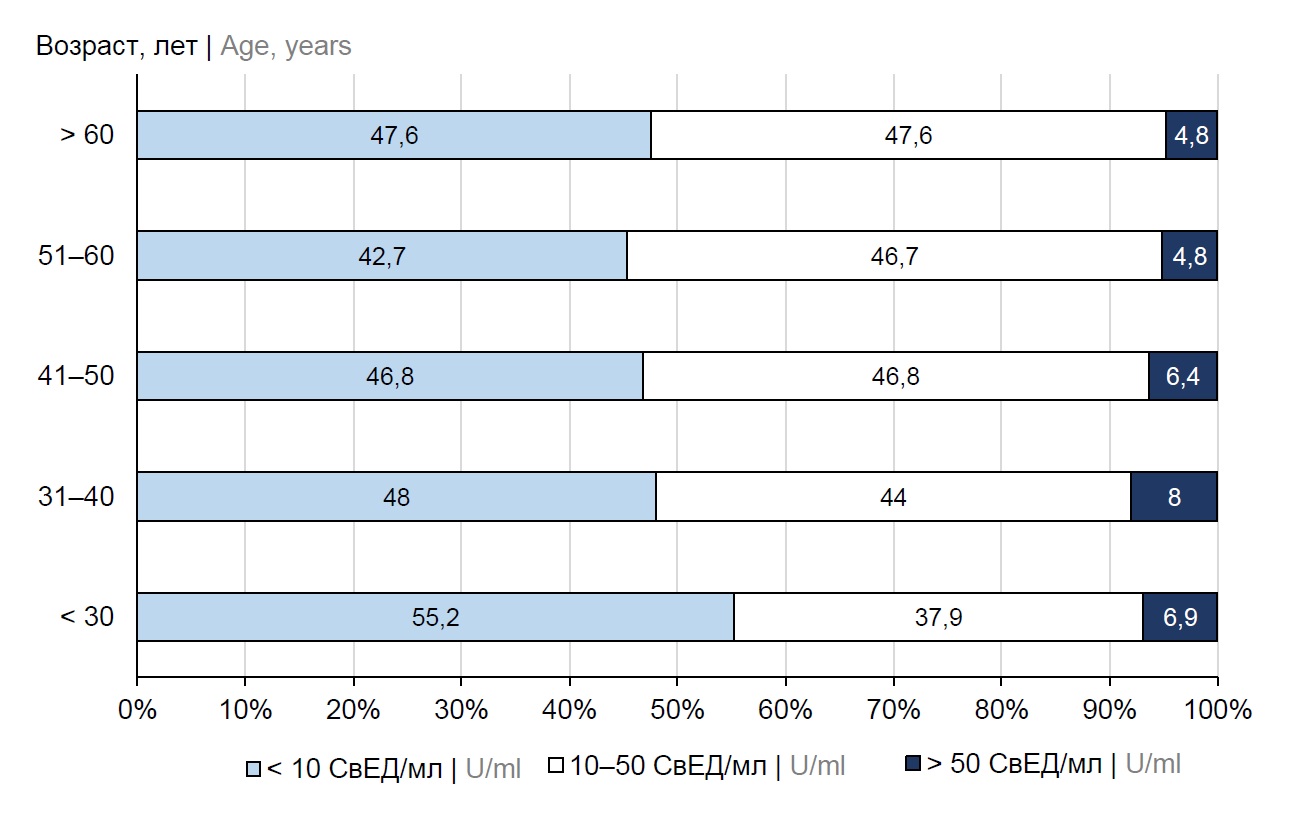
Результаты. Доля медицинских работников, серонегативных к коклюшу, составила 46,8%, медицинских работников с неизвестным вакцинальным статусом — 40,5%. Более половины (55,6%) участников исследования были вакцинированы, 3,9% переболели коклюшем в детстве. Недавняя инфекция была установлена у 8,0% участников, имевших уровень антител к Bordetella pertussis выше 50 СвЕд/мл. Доля серонегативных к коклюшу (55,2%) была выше в возрастной группе моложе 30 лет в сравнении с другими возрастными группами. Медиана концентрации противококлюшных антител у серопозитивных медицинских работников — 28,3 СвЕд/мл.
Заключение. Наличие значительной доли серонегативных (46,8%) и перенёсших острую инфекцию подтверждает необходимость оптимизации специфической профилактики коклюша, в том числе иммунизации групп риска, к которым относятся медицинские работники, с целью снижения рисков возникновения инфекций, связанных с оказанием медицинской помощи.
 196-202
196-202


Устойчивость к противомикробным препаратам пищевых изолятов Salmonella enterica на территории Республики Беларусь
Аннотация
Введение. Устойчивость к противомикробным препаратам является глобальной проблемой здравоохранения. Salmonella spp., которые могут передаваться человеку через контаминированную пищевую продукцию, признаны важными патогенами пищевого происхождения во всём мире.
Материалы и методы. Исследования противомикробной резистентности 358 изолятов микроорганизмов из пищевых продуктов и воды, изолированных на территории Республики Беларусь в 2018–2021 гг., проводились путём изучения фенотипических и генотипических характеристик антибиотикорезистентности микроорганизмов. Таксономическое положение бактерий было идентифицировано методом MALDI-TOF масс-спектрометрии. Фенотипическую чувствительность бактерий к антимикробным препаратам определяли методом минимальной подавляющей концентрации с помощью автоматизированного бактериологического анализатора «Sensititre» и диско-диффузионным методом к 45 противомикробным препаратам. Гены устойчивости к противомикробным препаратам у мультирезистентных изолятов сальмонелл определяли с помощью полногеномного секвенирования.
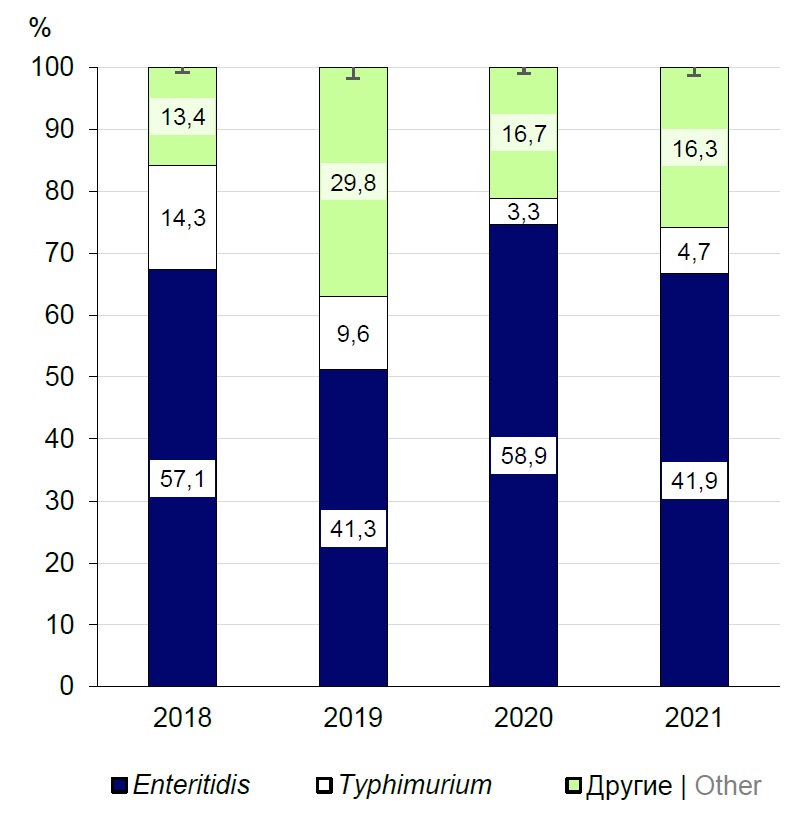
Результаты. Анализ фенотипической чувствительности бактерий in vitro показал высокую чувствительность к фторхинолонам (97,2%), цефалоспоринам 3-го поколения (93,9%), карбапенемам (98,0%), ампициллину (81,8%), аминогликозидам (97,5%), тетрациклинам (87,5%), хлорамфениколу (93,8%), триметоприм/сульфаметоксазолу (ко-тримоксазолу) (95,3%) и колистину (85,2%). Показано, что механизм резистентности к антибиотикам у S. enterica был ассоциирован с наличием генов blaTEM-1B (82%), blaTEM-1C (7,7%), blaSHV-12 (2,6%), blaDHA-1 (2,6%), blaCMY-2 (7,7%), qnrB2 (9,1%), qnrB4 (9,1%), qnrB5 (9,1%), qnrB19 (72,7%), aac(6’)-Ib-cr (9,1%), aac(6’)-Iaa (100%), aadA1 (13,2%), aadA2 (8,8%), tetB (74,3%), tetA (25,7%), tetM (2,9%), tetD (28,6%), mcr-9 (1,5%).
Заключение. Все изоляты микроорганизмов были фенотипически высокочувствительны к препаратам 1-й линии в терапии сальмонеллёза: фторхинолонам и цефалоспоринам 3-го поколения. Результаты полногеномного секвенирования мультирезистентных изолятов сальмонелл (19,0%) выявили гены устойчивости к 9 группам антибиотиков: аминогликозидам (100%), бета-лактамам (57,4%), фторхинолонам (16,2%), тетрациклинам (51,5%), макролидам (1,5%), фениколам (30,4%), триметоприму (13,0%), сульфаниламидам (47,8%) и колистину (1,4%). Таким образом, для контроля устойчивости к противомикробным препаратам среди сальмонелл пищевого происхождения решающее значение имеет эпидемиологический надзор за их распространением в цепи пищевых продуктов.
 153-167
153-167


Антибиотикочувствительность холерных вибрионов в сложных биоплёнках, сформированных на различных субстратах
Аннотация
Введение. Изучение антибиотикочувствительности биоплёнок холерных вибрионов может помочь в поиске эффективных препаратов для борьбы с холерой.
Цель работы — оценить эффективность антибактериальных препаратов в отношении клеток Vibrio cholerae в составе полимикробной биоплёнки, образованной на различных субстратах.
Материалы и методы. Проводили моделирование моно- и полимикробных биоплёнок in vitro на хитине и пластике во флаконах с водопроводной автоклавированной водой, контаминированных взвесью 104 микробных клеток трёх штаммов V. cholerae О1 El Tor отдельно и в сочетании с Escherichia coli QD 5003.
Результаты. В составе моно- и полимикробных бактериальных сообществ, образованных изучаемыми штаммами на хитине или на пластике, клетки холерных вибрионов и кишечной палочки оказались менее восприимчивы к действию антибактериальных препаратов.
Заключение. Повышенная антибиотикоустойчивость биоплёнок холерных вибрионов, образованных на биотических и абиотических поверхностях, подчёркивает опасность их распространения и сохранения в окружающей среде, создаёт дополнительные проблемы в отношении использования антибиотиков и требует разработки альтернативных стратегий снижения резистентности.
 188-195
188-195


Антигенная идентичность иммунодоминантных белков геновариантов Bacillus anthracis
Аннотация
Введение. Основным биологическим сырьём при производстве иммунобиологических препаратов для индикации и идентификации Bacillus anthracis являются специфические антигены — протективный антиген (ПА) и белок ЕА1.
Цель работы — определить антигенную идентичность иммунодоминантных белков, выделенных гель-хроматографией и электрофорезом, различных геновариантов B. anthracis.
Материалы и методы. В работе использованы культуральные фильтраты изогенных вариантов штамма B. anthracis 575/122 (рХО1+, рХО2+): R01 (pXO1+, pXO2–); R00 (pXO1–, pXO2–). Гель-хроматографическое фракционирование и электрофоретическое разделение проведено по стандартным методикам. Антигенные свойства белков, выделенных гель-хроматографией и электрофорезом, изучены в реакции иммунодиффузии с поликлональными моноспецифическими сыворотками к ПА и белку ЕА1 S-слоя.
Результаты. При гель-хроматографическом разделении культуральных фильтратов B. anthracis 575/122: R01 (pXO1+, pXO2–) и R00 (pXO1–, pXO2–) получены фракция 1 и фракция 5. Сыворотки к белку ЕА1, а также к фракции 1 культуральных фильтратов штаммов B. anthracis 575/122 R00 и B. anthracis 575/122 R01 выявили идентичные антигены. Сыворотка к антигенам фракции 5 B. anthracis 575/122 R01 содержит антитела к ряду белков, в том числе к ПА, выделенному электрофорезом.
Обсуждение. В ходе работы была установлена антигенная идентичность иммунодоминантных белков, выделенных гель-хроматографией и электрофорезом.
Заключение. Таким образом, нами в электрофорезе и гель-хроматографией выделены белок ЕА1 и ПА, которые могут быть использованы для получения моноклональных и поликлональных моноспецифических антител, пригодных для конструирования диагностических препаратов.
 203-208
203-208


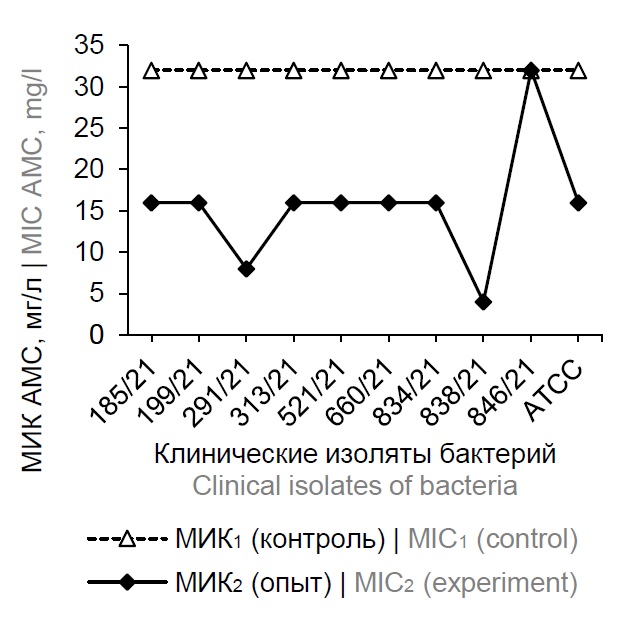
Влияние повидон-йода на чувствительность клинических изолятов Klebsiella pneumoniae к антибиотикам
Аннотация
Введение. Развитие устойчивости микроорганизмов к антибиотикам на фоне использования биоцидов в субингибирующих концентрациях является актуальной проблемой современного здравоохранения.
Цель работы — изучить влияние повидон-йода на чувствительность клинических изолятов Klebsiella pneumoniae к антибиотикам.
Материалы и методы. В работе проанализировано влияние повидон-йода в субингибирующих концентрациях на изменение чувствительности клинических изолятов K. pneumoniae (n = 9) к антибактериальным средствам (n = 15). Адаптацию бактерий к повидон-йоду проводили с использованием периодического культивирования микроорганизмов, которое осуществляли в 96-луночных культуральных планшетах для суспензионных культур (non-treated) без перемешивания. Оценку чувствительности бактерий к антибиотикам проводили с помощью автоматического анализатора «Vitek2Compact» («BioMerieux») с использованием карт AST-204.
Результаты. В ходе адаптации клинических изолятов K. pneumoniae к повидон-йоду показано увеличение чувствительности бактерий к антибиотикам. Минимальные ингибирующие концентрации 11 антибактериальных средств в отношении изученных культур снизились в среднем в 2,35–23,2 раза по сравнению с контрольными значениями. В условиях опыта чувствительность изученных культур возросла к амоксициллин/клавулановой кислоте в ≥ 2 – ≥ 8 раз, пиперациллин/тазобактаму — в ≥ 2 – ≥ 32 раза, цефтазидиму — 4 – ≥ 16 раз, амикацину — в 2 – ≥ 16 раз, эртапенему — в 2–8 раз, меропинему — в 2–8 раз, цефепиму — ≥ 4– ≥ 64 раз, ципрофлоксацину — в 4 – ≥ 16 раз, гентамицину — в 2 – ≥ 8 раз, норфлоксацину — в 2–8 раз, нитрофурантоину — в 2–4 раза. Повышение уровня чувствительности к антибиотикам выявлено у 50–100% изученных клинических изолятов бактерий. Подобный эффект не был установлен для ампициллина, цефотаксима, имипенема и триметоприм/сульфаметоксазола. В условиях опыта была выявлена внутривидовая гетерогенность клинических изолятов K. pneumoniae по уровню приобретённой чувствительности к антибактериальным средствам.
Обсуждение. Полученные нами результаты не описаны в научной литературе и требуют дальнейшего изучения и объяснения.
 209-218
209-218


ОБЗОРЫ
Российская база данных лекарственной устойчивости ВИЧ к антиретровирусным препаратам
Аннотация
Развитие технологий секвенирования и биоинформатического анализа дало возможность проведения молекулярно-эпидемиологических исследований, в которых нуклеотидные последовательности вируса иммунодефицита человека (ВИЧ) используются в качестве дополнительной характеристики пациента. При этом наиболее значимым с практической точки зрения направлением работ является изучение распространения лекарственной устойчивости (ЛУ) ВИЧ. В различных странах для организации таких исследований применяются базы данных, являющиеся хранилищами генетической и эпидемиологической информации. Российская база данных устойчивости ВИЧ к антиретровирусным препаратам (https://hivresist.ru/) была создана в 2009 г. Тем не менее длительное время её применение оставалось ограниченным. С 2021 г. после обновления нормативных документов внесение результатов исследований ЛУ ВИЧ в российскую базу данных устойчивости ВИЧ к антиретровирусным препаратам стало обязательным. В связи с этим были проведены работы по усовершенствованию базы данных и увеличению её функциональных возможностей. Были разработаны различные способы внесения клинико-эпидемиологических и генетических данных. На момент написания публикации российская база данных ЛУ ВИЧ содержала 10 626 уникальных записей о пациентах и 13 126 нуклеотидных последовательностей, загруженных 10 учреждениями. Для анализа данных были разработаны следующие функции: контроль качества эпидемиологической и клинической информации о пациенте, контроль качества нуклеотидных последовательностей, проверка на контаминацию, субтипирование, выявление мутаций ЛУ, определение вирусного тропизма и генерация стандартизированных отчётов. В планах по дальнейшему развитию российской базы данных ЛУ ВИЧ — разработка инструмента для выявления и анализа молекулярных кластеров и адаптация для рутинного использования в рамках эпидемиологического надзора за ВИЧ-инфекцией.
 219-227
219-227


Агрегированность Yersinia pestis как функциональная адаптация к организму блохи (обзор)
Аннотация
Проблема определения условий и механизмов агрегирования чумного микроба в организме переносчиков — блох — всегда была актуальной, а с конца 1990-х гг. в связи с началом исследований биоплёнок получила новое развитие.
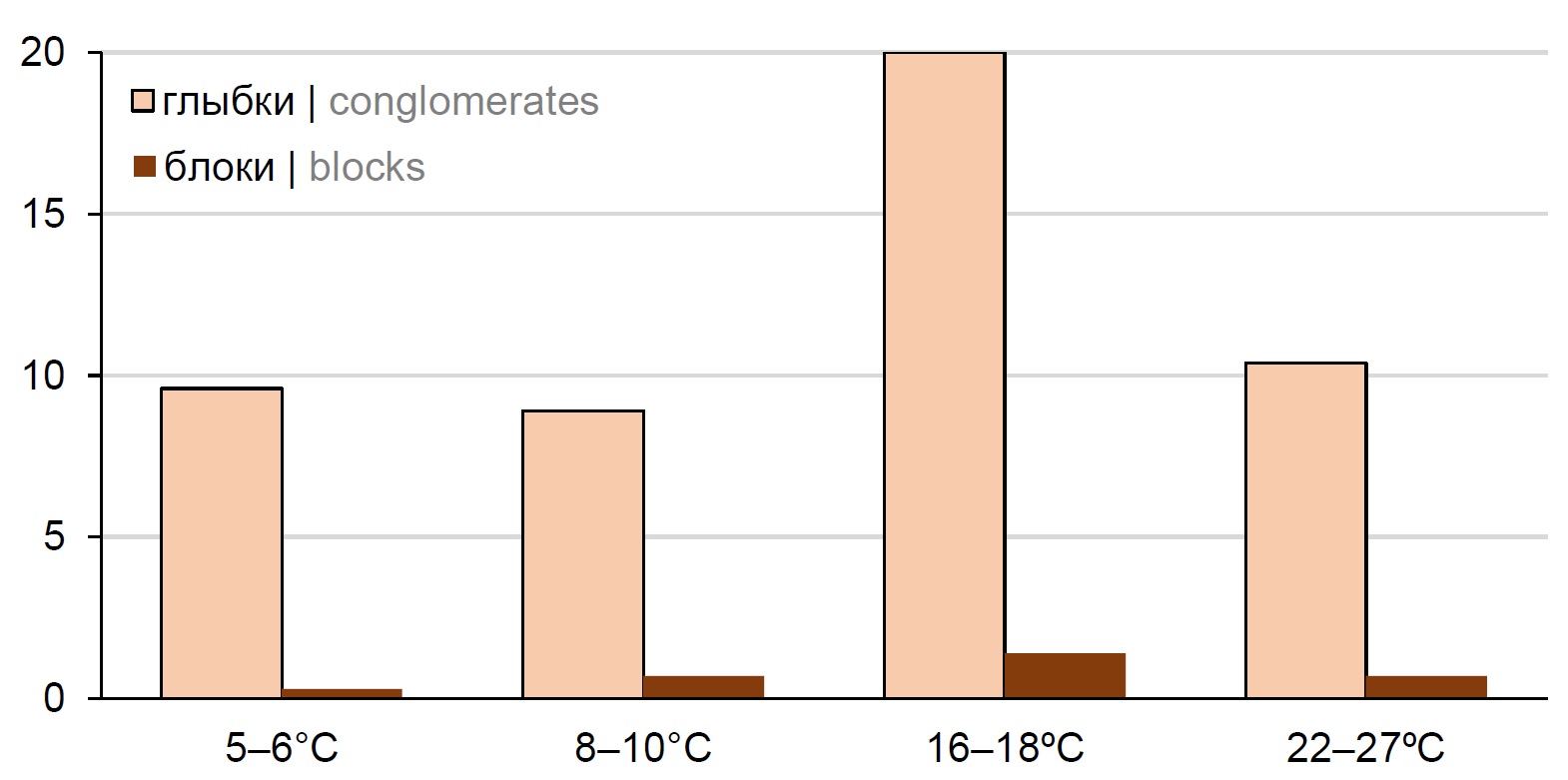
С целью выявления особенностей агрегирования чумного микроба в организме основного переносчика в Тувинском природном очаге — блохи Citellophilus tesquorum — проанализированы и обобщены данные многолетних экспериментальных исследований, проведённых с типичными для очага вирулентными штаммами Yersinia pestis subsp. pestis. Эктопаразитов инфицировали и проводили подкормки на их естественном прокормителе и основном носителе Y. pestis в Тувинском очаге — длиннохвостом суслике (Spermophilus undulatus). Взаимоотношения Y. pestis и блох оценивали по доле особей с конгломератами — «глыбками», сформировавшимися за подкормку, и «блоками» преджелудка за подкормку и за опыт в целом, которые регистрировали визуально в живых блохах после кровососания, а также по частоте передачи возбудителя животным, использованным для подкормок.
Проведённый анализ позволил выявить факторы, влияющие на частоту и динамику формирования различных форм агрегатов Y. pestis у C. tesquorum, и рассмотреть эти процессы как функциональную адаптацию микроба к организму блохи.
 240-250
240-250


Иммуногенез при лихорадке Ласса и перспективы разработки вакцины
Аннотация
В 2017 г. ВОЗ включила лихорадку Ласса в перечень приоритетных патогенов для разработки вакцин и объявила чрезвычайную ситуацию в области общественного здравоохранения по вызываемой им инфекции.
Анализ данных литературы по строению генома вируса Ласса и его штаммовому многообразию показал, что молекулярная гетерогенность штаммов существенна при конструировании вакцин и оценке их эффективности, что определено соответствующими рекомендациями ВОЗ. При репродукции вирус Ласса противодействует клеточному иммуногенезу — подавляет экспрессию супрессора сигнальных белков, цитокинов и рецептора RLR, распознающего вирусную двухсегментированную РНК.
Белок GP, определяющий инфекциозность возбудителя и тропизм, должен быть основной мишенью для разрабатываемых вакцин. Другие мишени — процессы синтеза вирусной РНК, определяющие особенности иммуногенеза. Исследование иммуногенеза лихорадки Ласса показывает, что предпочтительным кандидатом была бы реплицирующаяся апатогенная вакцина, способная индуцировать оптимальное сочетание клеточных и гуморальных ответов, т.е. вызывающая высокую активность Т-лимфоцитов и выработку вируснейтрализующих антител. Одной из важнейших характеристик живой кандидатной вакцины должна быть генетическая стабильность для исключения реверсии в направлении к более патогенному генотипу.
Из сконструированных более 130 кандидатных вакцин против лихорадки Ласса лишь две (рекомбинант на платформе вируса кори и ДНК-вакцина) как наиболее перспективные испытаны на иммуногенность и безвредность для людей. Для дальнейшей разработки перспективны рекомбинант вируса Ласса с вирусом везикулярного стоматита и реассортанты вирусов Мопейя (MOPV/LASV — ML29) и Ласса (r3ML29). Перспективна кандидатная вакцина rVSVΔG/LVGPC, аналогичная по конструкции вакцине rVSVΔG-ZEBOV-GP против лихорадки Эбола.
 228-239
228-239


НЕКРОЛОГИ
 251-252
251-252