Том 98, № 5 (2021)
- Год: 2021
- Выпуск опубликован: 02.11.2021
- Статей: 12
- URL: https://microbiol.crie.ru/jour/issue/view/46
Весь выпуск
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
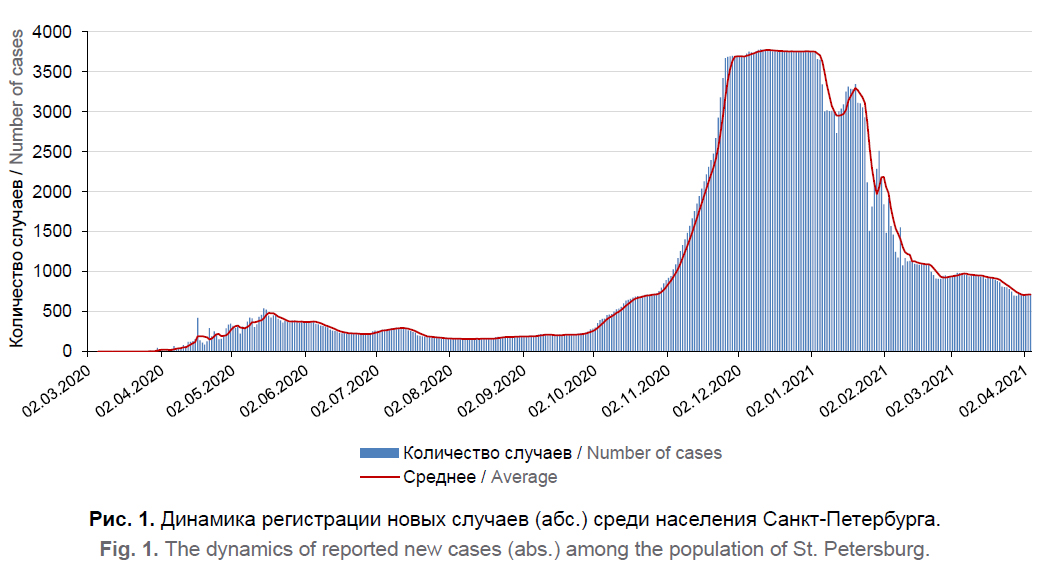
Характеристика эпидемиологической ситуации по COVID-19 в Санкт-Петербурге
Аннотация
Цель. Определить эпидемиологические закономерности распространения SARS-CoV-2 среди населения Санкт-Петербурга за годовой период пандемии COVID-19.
Материалы и методы. Проведён анализ динамики случаев заболеваний COVID-19 в Санкт-Петербурге в период с 02.03.2020 по 04.04.2021 и гендерно-возрастной характеристики пациентов. Информация о пациентах (возраст, пол, форма заболевания, госпитализация, социально-профессиональная принадлежность) извлечена из базы данных, сформированной на основе материалов формы статистического учёта № 058/у.
Результаты. По прошествии года в динамике выявления случаев COVID-19 в Санкт-Петербурге можно выделить два цикла сезонного подъёма заболеваемости (весенний и осенне-зимний) и 8 периодов эпидемии. Установлено, что в структуре заболевших COVD-19 отсутствует гендерно-возрастная избирательность, о чём свидетельствуют относительно равномерные показатели заболеваемости мужчин и женщин на 100 тыс. населения в каждой возрастной группе в отдельные периоды эпидемии. Отчётливо выражена зависимость клинических проявлений COVID-19 от возраста пациентов: тяжёлые формы заболевания чаще диагностированы у пациентов старше 70 лет независимо от гендерной принадлежности. Наиболее вовлечёнными в эпидемический процесс COVID-19 по социально-профессиональному статусу были пенсионеры и лица, связанные по роду деятельности с обеспечением жизнедеятельности Санкт-Петербурга. Удельный вес пенсионеров среди заболевших COVID-19 составил 13,69% (мужчины) и 17,67% (женщины). Доля медицинских работников составила 3,67% (мужчины) и 9,41% (женщины).
Заключение. Высказано предположение, что COVID-19 формируется как сезонное заболевание с ежегодными осенне-зимними эпидемическими циклами. Обсуждаются перспективы вакцинопрофилактики COVID-19 в России и необходимость учёта в системе эпидемиологического надзора за COVID-19 случаев осложнений, патогенетически связанных с острой фазой заболевания.
 497-511
497-511


Антигенная и генетическая характеристика штаммов Streptococcus pneumoniae, выделенных от больных инвазивными и неинвазивными пневмококковыми инфекциями, с использованием высокопроизводительного секвенирования
Аннотация
Цель работы заключалась в характеристике и сопоставлении данных об антигенных и генетических свойствах полученных с помощью высокопроизводительного секвенирования штаммов Streptococcus pneumoniae, выделенных от больных инвазивными и неинвазивными формами пневмококковой инфекции (ПИ). Материалы и методы. Исследовано 158 штаммов S. pneumoniae, выделенных при проведении различных этапов многоцентрового исследования «ПеГАС» в 2015-2020 гг. При анализе данных использовалась информация о полногеномных последовательностях 46 штаммов, выделенных ранее в том же исследовании. Для определения серотипов применены методики ПЦР в режиме реального времени и высокопроизводительное секвенирование (платформа «Illumina»). При обработке данных использовались программы «SeroBA», «PneumoCaT» и программные возможности интернет-ресурса PubMLST.org.
Результаты и обсуждение. Определены серотипы всех штаммов, включённых в исследование. Найден ряд несовпадений серотипов внутри серогруппы 6 и один дискордантный результат при анализе полногеномных последовательностей двумя программами. Предлагаемые ПЦР-подходы позволяют охарактеризовать серотип у 87% возбудителей инвазивных и 69% неинвазивных форм ПИ. Доля штаммов с серотипами, входящими в состав PCV13, составляет 59 и 37%, в состав PPV23 — 78 и 53% для штаммов, выделенных от больных инвазивными и неинвазивными ПИ соответственно. Анализ данных не позволяет выявить преобладающий сиквенс-тип (всего найден 81 сиквенс-тип) или определить клональные комплексы, за исключением штаммов серотипа 3, что согласуется с полученными ранее данными об отсутствии выраженной клональной структуры S. pneumoniae, ассоциированных с пневмококковыми менингитами, на территории России.
Заключение. Получены данные, позволяющие определить распределение циркулирующих серотипов и генетические характеристики штаммов, выделенных от больных ПИ, что даёт возможность оценить эффективность существующих поливалентных вакцин и предоставляет информацию для коррекции основанных на ПЦР способов серотипирования.
 512-518
512-518


Иммуногенные свойства препарата, содержащего инактивированный β-пропиолактоном антиген вируса Чикунгунья
Аннотация
Введение. Случаи лихорадки Чикунгунья зарегистрированы более чем в 100 странах Европы, Океании, Африки, Азии, Карибского бассейна, Америки. Поражения скелетно-мышечной системы, характерные для лихорадки Чикунгунья, могут длиться от нескольких месяцев до года и даже приводить к утрате трудоспособности. Считается, что перенесённая инфекция обеспечивает пожизненный иммунитет. Этот фактор, наряду с отсутствием специфической терапии, делает вакцинацию наиболее перспективным путём профилактики лихорадки Чикунгунья.
Целью настоящей работы было лабораторное изучение иммуногенных свойств препарата, содержащего инактивированный бета-пропиолактоном (β-ПЛ) антиген вируса Чикунгунья (ЧИКВ).
Материалы и методы. Очищенный инактивированный препарат с разными дозами антигена ЧИКВ был введён внутримышечно мышам BALB/c дважды с интервалом 14 сут. В динамике оценивали показатели гуморального и клеточного иммунитета в тестах ИФА, реакции нейтрализации и пролиферации спленоцитов.
Результаты. В ответ на введение инактивированного препарата антигена ЧИКВ наиболее выраженный иммунный ответ в ИФА и реакции нейтрализации отмечался для дозы 40 мкг. Стимуляция специфическим антигеном ЧИКВ вызывала выраженную пролиферацию спленоцитов иммунных животных. Максимальные показатели гуморального и клеточного иммунитета были отмечены у иммунизированных животных через 14 дней после 2-го введения препарата и сохранялись до конца срока наблюдения.
Обсуждение. Очищенный препарат, содержащий инактивированный β-ПЛ антиген ЧИКВ, обладал выраженными иммуногенными свойствами. Препарат, введённый мышам BALB/c двукратно с дозой инактивированного антигена ЧИКВ 40 мкг, вызывал формирование специфического гуморального иммунитета, характеризующегося появлением иммуноглобулинов класса G, обладающих вируснейтрализующей активностью, и формирование специфического клеточного ответа, характеризующегося пролиферацией спленоцитов в ответ на стимуляцию специфическим антигеном ЧИКВ.
Заключение. Очищенный инактивированный β-ПЛ препарат антигена ЧИКВ в дозе 40 мкг после двукратного введения мышам линии BALB/c продемонстрировал выраженную иммуногенность. Разработанный препарат может быть оценён как перспективный для профилактики лихорадки Чикунгунья с использованием дозы и схемы, апробированных в данном исследовании.
 519-527
519-527


Микробиота нижних дыхательных путей при внебольничных пневмониях, в том числе ассоциированных c SARS-CoV-2
Аннотация
Введение. Многие аспекты патогенеза и патоморфологии коронавирусной пневмонии нуждаются во всестороннем комплексном изучении с использованием современных методов диагностики.
Цель исследования — изучение микробиоты нижних дыхательных путей при внебольничных пневмониях (ВБП), ассоциированных c SARS-CoV-2, оценка антибиотико- и фагорезистентности циркулирующих штаммов микроорганизмов.
Материалы и методы. Проведён анализ биопроб от 486 пациентов, находящихся на стационарном лечении в 5 моногоспиталях Тюмени и Тюменской области с диагнозом ВБП средней и тяжёлой степени. Почти в 90% случаев пациенты получали оксигенотерапию, около 8% больных были подключены к аппаратам искусственной вентиляции лёгких. Посев клинического материала осуществлялся на протяжении 6 мес (с апреля по октябрь 2020 г.). Идентификацию выделенных штаммов бактерий выполняли методом масс-спектрометрии. У обнаруженных изолятов определяли резистентность к антимикробным препаратам и бактериофагам.
Результаты. В микробиоте нижних дыхательных путей пациентов с диагнозом «ВБП, ассоциированная с SARS-CoV-2» превалировали грамположительные кокки, преимущественно условно-патогенные микроорганизмы рода Streptococcus и грибы рода Candida. При этом бактерии семейства Enterobacteriaceae и неферментирующие грамотрицательные бактерии встречались реже, чем у пациентов без COVID-19. В структуре патогенов лидирующее положение занимали бактерии Klebsiella pneumoniae и Acinetobacter spp.Анализ чувствительности микроорганизмов к антимикробным препаратам показал наиболее высокую резистентность у штаммов Acinetobacter spp., Enterococcus spp., коагулазонегативных Staphylococcus spp. Установлено, что в группе пациентов с ВБП, ассоциированной с SARS-CoV-2, шансы встретить штаммы Streptococcus spp. с высокой устойчивостью к антибиотикам в 1,5 раза выше, а с учётом 95% доверительного интервала величина этого показателя колебалась в пределах 1,1-2,1 раза.
Вывод. Полученные данные свидетельствуют о том, что микробиота нижних дыхательных путей при ВБП, ассоциированных c SARS-CoV-2, представлена преимущественно бактериями рода Streptococcus, обладающими высоким уровнем резистентности к антимикробным препаратам.
 528-537
528-537


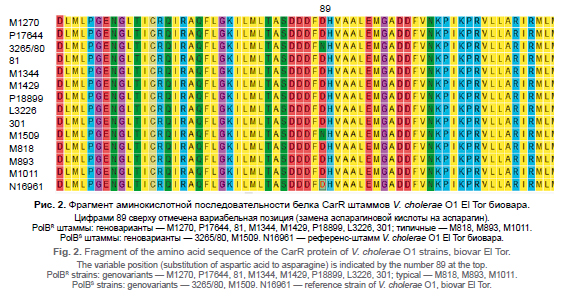
Выявление чувствительных к полимиксину В штаммов Vibrio cholerae О1 серогруппы El Tor биовара и их молекулярно-генетический анализ
Аннотация
Цель работы — выявление и молекулярно-генетическая характеристика чувствительных к полимиксину В штаммов Vibrio cholerae О1 серогруппы El Tor биовара, выделенных на территории России.
Материалы и методы. В работе использовали 56 токсигенных и нетоксигенных штаммов V. cholerae, выделенных от больных и из внешней среды в России в 1970-2020 гг. Устойчивость к полимиксину В определяли согласно МУК 4.2.2218-07. Для изучения способности штаммов формировать биоплёнку на абиотической поверхности использовали фотометрический метод. Нуклеотидные последовательности генов устанавливали с применением программ «UGENE v.1.32» и «MEGA X». Филогенетический анализ и построение дерева производили с помощью программы «MEGA X», используя метод «максимальной бережливости».
Результаты и обсуждение. Выявлены 2 чувствительных к полимиксину В клинических генетически изменённых штамма V. cholerae О1 El Tor биовара М1509 и 3265/80, завезённых в Россию из Индии в 2012 и 2014 гг. соответственно. При изучении структуры 12 генов, обеспечивающих устойчивость штаммов V. cholerae О1 El Tor биовара к полимиксину В, установлено, что указанные штаммы содержат аллель гена carRS, что характерно для всех чувствительных к полимиксину В штаммов V. cholerae. Изучение филогении штаммов V. cholerae М1509 и 3265/80 на основе SNP-анализа показало, что они входят в один кластер с изолятами, содержащими аллель carRS и выделенными в Индии (2015 г.) и Бангладеш (2018 г.). При сравнительном изучении способности штаммов V. cholerae М1509 и 3256/8 к формированию биоплёнки установлено, что они не отличаются по данному свойству от других, взятых в анализ генетически изменённых штаммов V. cholerae.
Заключение. В Россию завозятся высоковирулентные штаммы возбудителя холеры с изменёнными диагностически значимыми признаками, что необходимо учитывать при идентификации штаммов V. cholerae О1 El Tor биовара, выделяемых от больных и из внешней среды при мониторинговых исследованиях.
 538-547
538-547


Оценка мутагенности, генотоксичности и хронической токсичности имидазолилэтанамида пентандиовой кислоты в тест-системах in vitro и in vivo
Аннотация
Введение. Имидазолилэтанамид пентандиовой кислоты (ИПК) обладает доказанными на различных экспериментальных моделях противовирусными свойствами. Однако данные о токсикологических свойствах ИПК ограниченны.
Цель. Оценить мутагенные и генотоксические свойства на моделях in vitro и in vivo, а также токсичность ИПК при хроническом пероральном введении крысам и собакам.
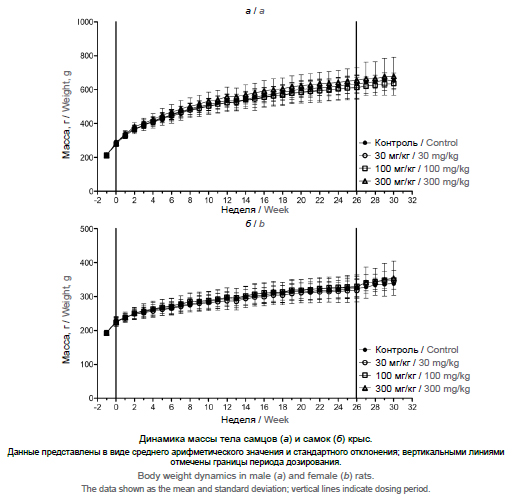
Материалы и методы. Мутагенные и генотоксические свойства ИПК оценивали в тесте Эймса, в тесте хромосомных аберраций на лимфоцитах человека, в микроядерном тесте у крыс. Хроническую токсичность ИПК изучали на крысах линии Спрег-Доули и собаках породы бигль обоих полов, которым ИПК вводили перорально в дозах 30-300 мг/кг/сут в течение 26 и 39 нед соответственно.
Результаты. В тесте Эймса внесение ИПК вплоть до максимальной дозы (5000 мкг на чашку) не приводило к увеличению числа ревертантных колоний. В концентрации до 5000 мкг/мл ИПК не вызывал хромосомных аберраций в лейкоцитах человека. В дозах ≤ 2000 мг/кг ИПК не увеличивал количество микроядер в костном мозге крыс. В хронических экспериментах животные хорошо переносили введение ИПК: доза без наблюдаемого эффекта (NOEL) для крыс и собак составляла 300 мг/кг/сут.
Заключение. ИПК не проявлял мутагенных и генотоксических свойств в стандартных тестах in vitro и in vivo. При хроническом пероральном введении крысам и собакам NOEL ИПК, равная 300 мг/кг/сут, обеспечивала системную экспозицию, превышающую таковую у человека в 8-10 и в 41-65 раз соответственно. Полученные результаты позволяют считать профиль безопасности ИПК при длительном применении у человека обоснованно благоприятным.
 548-557
548-557


Определение возможной мишени действия 4,4а-дигидроксантонов в бактериальных клетках
Аннотация
Введение. В настоящее время интенсивно изучаются частично гидрированные производные ксантона — дигидроксантоны (ДК). Они представляют интерес в связи с тем, что обладают антимикробным, противоопухолевым, антиоксидантным действием. Много работ посвящено исследованию цитотоксичности ДК и совсем немного сведений об их антимикробной активности.
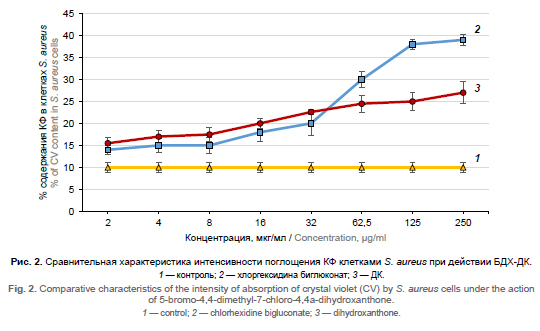
В связи с этим актуальным является исследование антимикробной активности и механизма действия новых синтетических производных 4,4а-ДК. В предварительных исследованиях установлено, что 4,4а-ДК активны в отношении грамположительных бактерий и обладают выраженным противостафилококковым действием. Выявлено наиболее активное производное — 5-бром-4,4-диметил-7-хлор-4,4а-ДК (БДХ-ДК).
Цель исследования — определить возможную мишень действия активного производного БДХ-ДК в бактериальных клетках, а также его острую токсичность.
Материалы и методы. Для доказательства воздействия БДХ-ДК на проницаемость цитоплазматической мембраны в бактериальных клетках был использован метод измерения интенсивности поглощения клетками бактерий красителя кристаллического фиолетового. С целью определения влияния БДХ-ДК на процесс синтеза белка было проведено исследование плазмокоагулазной активности Staphylococcus aureus под действием ДК. Для изучения действия БДХ-ДК на бактериальную ДНК использовали метод расщепления плазмидной ДНК. Острую токсичность БДХ-ДК определяли по экспресс-методу В.Б. Прозоровского.
Результаты. БДХ-ДК вызывал повышение проницаемости цитоплазматической мембраны S. aureus, не влиял непосредственно на плазмокоагулазную активность S. aureus и проявлял слабое повреждающее действие на бактериальную ДНК. Соединение индуцировало разрывы в плазмидной ДНК в очень высокой концентрации — 1 мМ, или 384 мкг/мл и выше. БДХ-ДК относится к малотоксичным соединениям (средняя летальная доза при пероральном введении соединения составила 1710 ± 170 мг/кг, при внутрибрюшинном — 116,9 ± 13,3 мг/кг).
Заключение. Впервые были проведены углублённые исследования возможного механизма действия нового синтетического биологически активного соединения из группы 4,4а-ДК — БДХ-ДК. Установлено, что вероятной мишенью действия БДХ-ДК в клетках S. aureus является цитоплазматическая мембрана. БДХ-ДК не влиял на процесс синтеза белка, а именно на активность фермента плазмокоагулазы. Соединение не оказывало выраженного повреждающего действия на бактериальную ДНК. Установлено, что 4,4а-ДК относится к малотоксичным соединениям.
 558-566
558-566


ОБЗОРЫ
Роль плазменного ингибитора сериновых лейкоцитарных протеиназ в защите организма от COVID-19
Аннотация
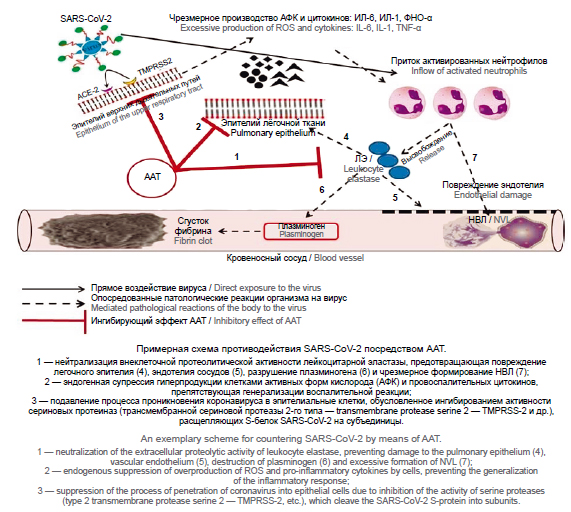
Пандемия COVID-19 продолжается, нанося колоссальный ущерб населению и мировой экономике. По мере изучения COVID-19 появляются новые данные относительно риска тяжёлого течения коронавирусной инфекции у пациентов с дефицитом α1-антитрипсина (ААТ). ААТ — основной ингибитор и ключевой эндогенный регулятор активности сериновых лейкоцитарных протеиназ, высвобождаемых из гранул активированных нейтрофилов на поверхность клеток и во внеклеточное пространство. Установлено, что число случаев тяжёлого течения и летального исхода COVID-19 на территориях 68 стран мира коррелирует с частотой распространения среди населения этих стран мутации в гене протеиназного ингибитора, при которой концентрация ААТ в плазме крови человека в 10 раз ниже нормы. Всё это способствует пересмотру ряда положений патогенеза и терапии COVID-19.
В обзоре представлен анализ литературы о роли ингибитора сериновых лейкоцитарных протеиназ в защите организма от COVID-19. Рассмотрено участие ААТ в ингибировании процесса проникновения SARS-CoV-2 в эпителиальные клетки дыхательных путей, в защите эндотелия сосудов, белков плазмы крови и эластина лёгочной ткани от повреждающего действия лейкоцитарной эластазы, высвобождаемой при дегрануляции нейтрофилов и формировании нейтрофильных внеклеточных ловушек. Показана роль ААТ в супрессии воспаления посредством ограничения секреции в кровь провоспалительных цитокинов и нейтрофильных внеклеточных ловушек. Детализированы отдельные звенья патогенеза новой коронавирусной инфекции, что позволит пересмотреть стратегию снижения рисков тяжёлого течения COVID-19.
 567-578
567-578


Применение штамма MVA вируса вакцины для создания рекомбинантных векторных вакцин против актуальных арбовирусных инфекций
Аннотация
Эпидемические трансмиссивные вирусные инфекции представляют собой серьёзную угрозу для здравоохранения многих стран. Для большинства из них отсутствуют средства специфической профилактики. В настоящее время одним из перспективных направлений борьбы с вирусными лихорадками является создание векторных вакцин, в том числе на основе штамма MVA, которые практически не вызывают побочных реакций. Безопасность штамма MVA и отсутствие реактогенности рекомбинантных вакцин, разработанных на его основе, показана в многочисленных клинических испытаниях.
В статье рассматриваются результаты испытаний подобных профилактических препаратов против вирусных лихорадок: Крымской-Конго геморрагической лихорадки, лихорадки долины Рифт, жёлтой лихорадки, лихорадок Чикунгунья и Зика.
Их иммуногенность оценивалась на иммунокомпетентных и иммунодефицитных белых мышах, а протективная эффективность — на иммунодефицитных белых мышах, дефектных по α-, β-рецепторам интерферона, на которых моделируют эту инфекцию. Почти все разработанные рекомбинантные вакцины, экспрессирующие иммунодоминантные антигены, обеспечивали 100% защитную эффективность. Показано, что, хотя вакцина, экспрессирующая структурные белки вируса Зика, индуцировала антитела против специфических вирусных гликопротеинов, её применение может вызывать опасность для профилактики лихорадки Зика у лиц, переболевших лихорадкой денге, в связи с наличием феномена антителозависимого усиления инфекции при заболеваниях, вызванных антигенно-родственными флавивирусами. По этой причине для иммунизации против лихорадки Зика разработана вакцина, экспрессирующая неструктурный белок NS-1.
Сконструированная на основе штамма MVA вакцина против жёлтой лихорадки обладала такой же иммуногенностью, что и коммерческая вакцина 17D, однако по уровню безопасности превосходила её.
 579-587
579-587


Эпидемиологическая характеристика инфекций Campylobacter в странах с высоким уровнем дохода: систематический обзор
Аннотация
Введение. Campylobacter — наиболее частая бактериальная причина болезней пищевого происхождения в странах с высоким уровнем доходов. В отличие от других инфекционных заболеваний, количество случаев Campylobacter увеличилось в развитых странах за последние 10 лет. Систематический обзор был проведён для выявления факторов, способствующих распространению инфекции Campylobacter в развитых странах, и оценки её по возрасту, полу, географии и сезону.
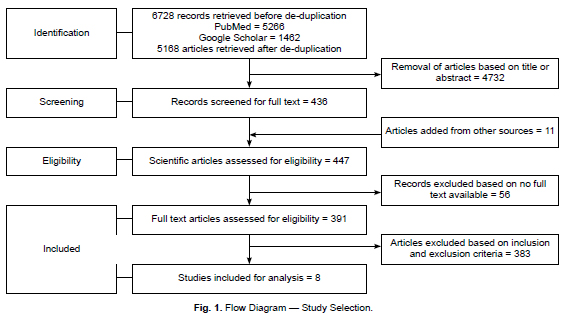
Материалы и методы. Обзор ограничен исследованиями, опубликованными на английском языке за 2010-2021 гг. В обзор были включены восемь общенациональных эпиднадзора и когортных исследований на основе регистров, которые соответствовали критериям отбора.
Результаты. В то время как самая высокая заболеваемость Campylobacter была зарегистрирована среди детей раннего возраста, живущих в сельской местности, самое большое количество случаев Campylobacter среди взрослых было зарегистрировано в городских условиях. Тем не менее больше всего страдают дети и пожилые люди, а уровень заболеваемости выше у мужчин, чем у женщин, причём пик заболеваемости приходится на каждое лето.
Заключение. Инфекция Campylobacter представляет собой проблему для общественного здравоохранения в странах с высоким уровнем доходов, её трудно искоренить, и она стала неотложной проблемой для существующих хорошо развитых систем эпиднадзора. Кроме того, угроза устойчивости Campylobacter к антибиотикам растет с угрожающей скоростью. Причины, по которым Campylobacter поражает больше мужчин, чем женщин, а также возраст и географическое распространение инфекции ещё требуют тщательного исследования.
 588-596
588-596


ЮБИЛЕИ
Академик В.Д. Беляков — творец современной отечественной теории эпидемиологической науки: к столетию со дня рождения выдающегося учёного, педагога и военного эпидемиолога
Аннотация
В статье анализируются итоги жизнедеятельности и творческое наследие академика РАМН и РАЕН профессора генерал-майора медицинской службы Виталия Дмитриевича Белякова (1921-1996 гг) в связи со 100-летием со дня его рождения и 85-летием образования кафедры общей и военной эпидемиологии Военно-медицинской академии им. С.М. Кирова. Выдающийся ученый-эпидемиолог, организатор и педагог в течение 18 лет возглавлял эту кафедру, а затем 14 лет руководил кафедрой эпидемиологии 1-го Московского медицинского института им. И.М. Сеченова. За эти годы он создал две собственные эпидемиологические школы и внёс неоценимый вклад в эпидемиологическую науку, профессиональную подготовку кадров для военно-медицинской службы и здравоохранения страны, а также в совершенствование систем противоэпидемического обеспечения войск (флота) и профилактической медицины. Главные заслуги В.Д. Белякова и его учеников состоят в разработке теории саморегуляции паразитарных систем, признанной биологическим фундаментом эпидемиологии инфекционных заболеваний; внедрении в медицинских вузах преподавания основ эпидемиологии неинфекционных болезней и методологии эпидемиологической диагностики; обосновании современных систем эпидемиологического надзора за заболеваемостью населения и управления эпидемическим процессом актуальных инфекций. Он и его сотрудники внесли большой вклад в изучение и профилактику значимых для личного состава войск (флота) и населения инфекций; совершенствование иммуно- и экстренной профилактики; реформирование профилактических направлений системы высшего медицинского образования и структур здравоохранения.
 597-606
597-606


РЕЦЕНЗИИ
 607-609
607-609