Том 99, № 2 (2022)
- Год: 2022
- Дата публикации: 15.05.2022
- Статей: 11
- URL: https://microbiol.crie.ru/jour/issue/view/49
Весь выпуск
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Оценка эпидемиологической значимости молекулярногенетических факторов в отношении напряжённости поствакцинального иммунитета против гепатита B
Аннотация
Введение. Гепатит В, сохраняя статус социально значимой инфекции, остаётся актуальной проблемой здравоохранения в России. Важной задачей является повышение эффективности действующего комплекса противоэпидемических мероприятий, в том числе вакцинопрофилактики. После проведения полного курса вакцинации против гепатита В удельный вес лиц с отсутствием или низкой концентрацией поствакцинальных анти-HBs составляет 5–10%. Одной из причин, детерминирующих отсутствие или недостаточность поствакцинального иммунитета против гепатита В, могут быть однонуклеотидные полиморфизмы (ОНП), в том числе определяющие реализацию механизма иммуногенеза. С учётом возможных ассоциаций ОНП с напряжённостью поствакцинального иммунитета, важной проблемой является оценка их эпидемиологической значимости.
Цель работы — определение влияния ОНП генов IL1B (rs1143634, rs1143627), IL1RN (rs4251961, rs419598), IL6 (rs1800795), IL10 (rs1800896), TULP1 (rs9380516), TLR4 (rs4986790), MERTK (rs4374383) на формирование поствакцинального иммунитета против гепатита В.
Материалы и методы. Изучаемую группу составили медицинские работники Лечебно-реабилитационного центра Минздрава России (n = 271) с установленным прививочным анамнезом, наличием данных о возрасте, стаже работы и отделении медицинского учреждения. Серологические исследования по определению наличия и уровня анти-HBs и анти-HBcore класса IgG выполняли методом ИФА с использованием тест-систем «ДС-ИФА-АНТИ-HBs» и «ДС-ИФА-АНТИ-HBc». Генотипирование проводили методом полимеразной цепной реакции в режиме реального времени. Статистическую обработку полученных данных осуществляли с использованием програмы «Statistica 6.0».
Результаты. В ассоциации с напряжённостью поствакцинального ответа против гепатита В установлены статистически значимые различия частот генотипов CC (rs9380516) (p = 0,034; отношение шансов (ОШ) 0,497; 95% ДИ 0,261–0,949) и CT (p = 0,044; ОШ 1,967; 95% ДИ 1,015–3,812) гена TULP1 в группе лиц с концентрацией анти-HBs 10–100 MЕ/л. Для этой группы также выявлены различия генотипов TT/CT генов IL10/TULP1 (rs1800896/rs9380516) (p = 0,003; ОШ = 5,39; 95% ДИ 1,7–17,4) и сочетания генотипов AA/TT ОНП MERTK/IL1RN (rs4374383/rs4251961) (p = 0,003; ОШ = 7,96; 95% ДИ 1,7–37,6).
Заключение. В настоящем исследовании показана роль вариантов генотипов в прогнозировании повышенного риска развития слабого поствакцинального иммунного ответа (или его отсутствия) против гепатита В. Ассоциации полиморфизмов ряда генов с низкой концентрацией поствакцинальных анти-HBs целесообразно использовать при разработке сценариев развития эпидемического процесса гепатита В, поскольку выявленные зависимости позволяют дать количественную характеристику рисков формирования слабого иммунитета против данной инфекции на популяционном уровне.
 149-159
149-159


Оценка интенсивности дегрануляции и изменений фенотипа нейтрофилов по уровню экспрессии FcᵧRIIIb в крови больных COVID-19 и реконвалесцентов
Аннотация
Введение. Тяжесть течения COVID-19 коррелирует с относительным содержанием в крови пациентов специфической популяции нейтрофильных гранулоцитов (НГ) низкой плотности, клетки которой характеризуются сниженной гранулярностью, высокой неоднородностью по экспрессии FcᵧRIIIb (CD16) и склонностью к спонтанному аутолизису (нетозу).
Цель исследования — сравнить интенсивность дегрануляции НГ и экспрессию FcᵧRIIIb на этих клетках в крови больных COVID-19 и реконвалесцентов.
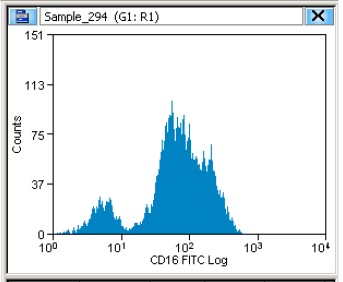
Материалы и методы. С помощью проточной цитометрии исследовали лейкоциты крови 40 пациентов с диагнозом COVID-19, 33 реконвалесцентов и 20 здоровых доноров (контроль). Для идентификации НГ (CD16+-гранулоцитов) и оценки поверхностной экспрессии молекулярного триггера нетоза FcᵧRIIIb применяли одноцветный реагент меченых моноклональных антител CD16-FITC. Иммунофенотипирование лимфоцитов осуществляли с использованием двух четырехцветных реагентов. Кроме того, в каждом образце цельной крови, окрашенном по Lyse/No-Wash-протоколу, определяли содержание клеточного дебриса. Присутствие в крови нейтрофилов на стадии нетоза подтверждали с помощью микроскопии. Продукцию цитокинов клетками определяли на автоматическом иммуноферментном анализаторе.
Результаты. На фоне характерных изменений субпопуляционного состава лимфоцитов и продукции цитокинов в крови больных COVID-19 с острой пневмонией, гипоксией и тахикардией, в сравнении с реконвалесцентами, перенёсшими тяжёлую и среднетяжёлую форму болезни, зарегистрирована более интенсивная дегрануляция НГ (в 2,6 раза), более высокая степень неоднородности по экспрессии CD16 (в 1,8 раза) и повышенная интенсивность лейкоцитолиза (в 1,6 раза). У реконвалесцентов степень различий с контролем по данным показателям зависела от тяжести ранее перенесённого заболевания.
Заключение. Характер изменения изученных в работе показателей у пациентов с COVID-19 в острый период болезни и в период реконвалесценции подтверждает возможный механизм развития осложнений вследствие нарушения баланса между активностью высвобождаемой из гранул НГ эластазы и её плазменным ингибитором α1 -антитрипсином.
 172-184
172-184


Распространённость антител к вирусу гепатита Е у населения регионов Республики Беларусь
Аннотация
Актуальность. Гепатит Е (ГЕ) является зооантропонозом. Основной резервуар вируса гепатита Е (ВГЕ) в Республике Беларусь (РБ) — домашние свиньи, что, в связи с развитой системой свиноводства, предполагает высокий риск распространения инфекции среди населения, однако реальные масштабы циркуляции вируса и закономерности эпидемиологии ГЕ в данном регионе остаются малоизученными.
Цель — изучение серопревалентности ВГЕ, характеризующей эпидемический процесс ГЕ в РБ.
Материалы и методы. В образцах сывороток крови (n = 2784), полученных от пациентов инфекционных отделений лечебно-профилактических учреждений (n = 1669) и практически здоровых людей (n = 1114) из разных регионов РБ, определяли активность аланинаминотрансферазы (АЛТ) кинетическим методом и антитела IgG к ВГЕ методом иммуноферментного анализа.
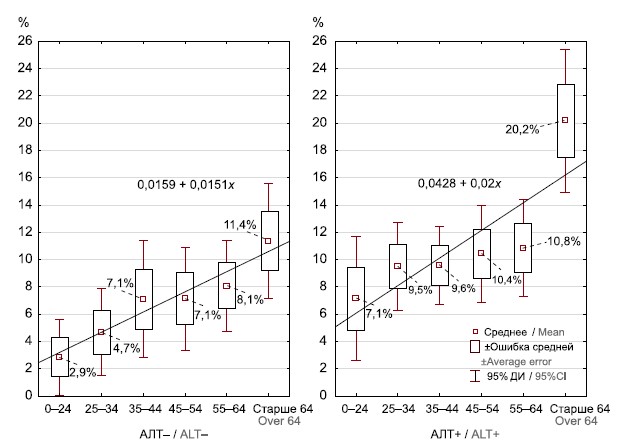
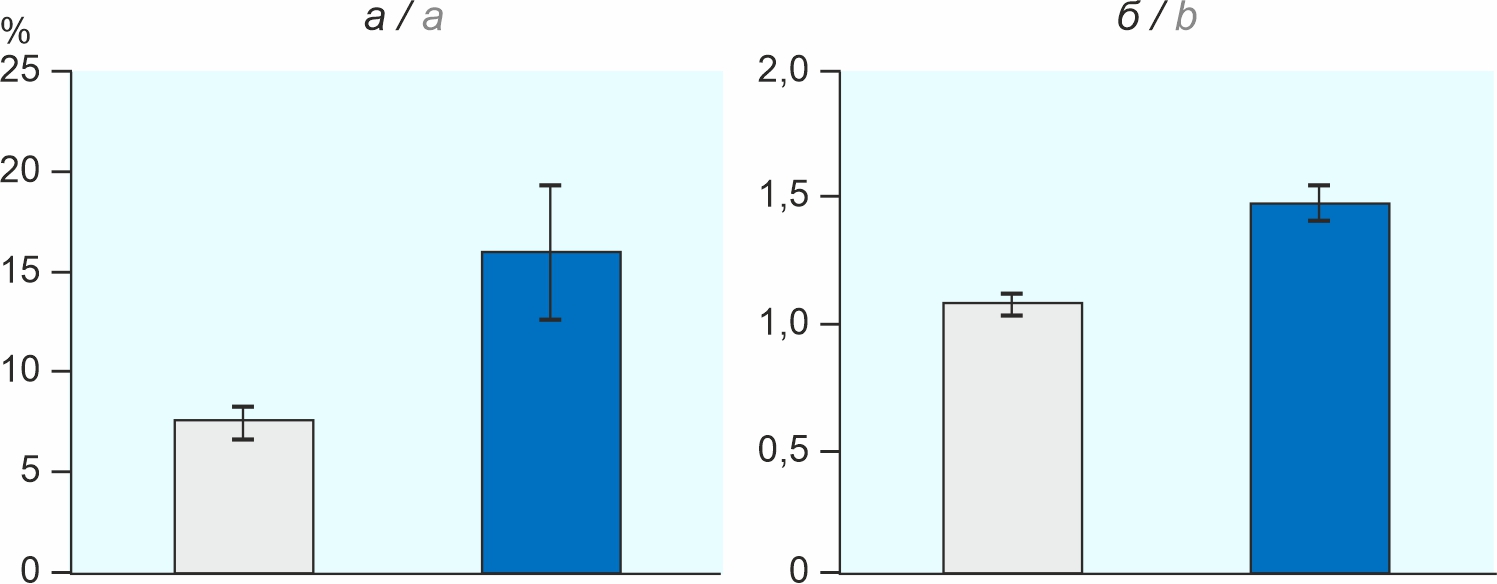
Результаты. Частота встречаемости анти-ВГЕ IgG в группе условно здоровых людей составила 7,3% (95% ДИ 5,8–9,0). В группе пациентов с поражением печени этот показатель был достоверно выше — 11,2% (95% ДИ 9,6–12,9). Серопревалентность ВГЕ в группах условно здорового населения и пациентов с повышенным уровнем АЛТ не зависела от пола и региона проживания обследуемых лиц. Частота выявления анти-ВГЕ IgG постепенно нарастала по мере увеличения возраста, достигая пиковых значений (в среднем 15,9%) в возрастной группе старше 64 лет.
Выводы. На территории РБ происходит интенсивная циркуляция ВГЕ, при этом эпидемический процесс ГЕ в РБ носит скрытый характер. Реальное распространение серомаркеров ВГЕ среди населения РБ превосходит частоту диагностированных случаев заболевания, что отражает отсутствие настороженности медицинского персонала в отношении ГЕ и указывает на субклиническое течение заболевания у большинства пациентов.
 160-171
160-171


Использование ПЦР-РВ как теста, подтверждающего отсутствие остаточной нейровирулентности штаммов для живых противовирусных вакцин
Аннотация
Введение. Учитывая особую важность заключения о безопасности применения противовирусных вакцин, содержащих хоть и ослабленные, но живые вирусы, с возможным сохранением остаточной нейровирулентности весьма актуальной представляется разработка дополнительных, подтверждающих стабильность аттенуации тестов, основанных на современных методах лабораторной диагностики.
Цель исследования — оценка возможности использования метода ПЦР-РВ в качестве дополнительного теста при контроле остаточной нейровирулентности аттенуированных вакцинных штаммов вируса краснухи.
Материалы и методы. В работе использовали живые аттенуированные вакцинные штаммы вируса краснухи «Орлов-В» и RA27/3. Исследование проводили на 11 клинически здоровых обезьянах вида Macaca mulatta массой 3–5 кг, родившихся и содержащихся в питомнике НИИМП. Клиническим материалом служили образцы тканей различных отделов ЦНС, региональных лимфатических узлов, паренхиматозных органов, плазма и спинномозговая жидкость экспериментальных животных. Контроль экстраневральной диссеминации вакцинных штаммов проводили с использованием вирусологического (реакция цитопатического действия) и молекулярно-биологического методов (ПЦР-РВ).
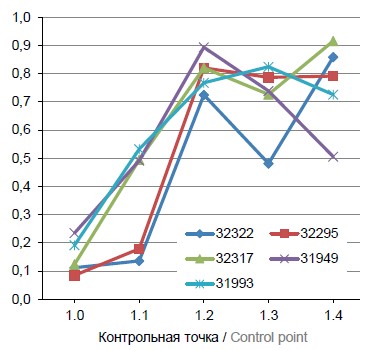
Результаты. Установлено отсутствие инфекционного вируса в ЦНС, периферических органах и плазме крови обезьян, заражённых вакцинными штаммами, что свидетельствует о высоком уровне аттенуации штаммов «Орлов-В» и RA27/3 вируса краснухи. Также выявлено, что аналитическая чувствительность метода ПЦР-РВ превышает аналитическую чувствительность реакции цитопатического действия на 1,7–3,3 lg при определении содержания вируса краснухи в тканях ЦНС и периферических органах инокулированных животных.
Заключение. Сравнительный анализ экспериментальных данных показал, что выявление вируса краснухи методом ПЦР-РВ имеет ряд преимуществ — это специфичность, чувствительность и меньшая длительность реакции. В связи с этим метод ПЦР-РВ может быть использован в качестве дополнительного теста при доклинической оценке специфической безопасности, а именно экстраневральной диссеминации аттенуированных вакцинных штаммов, что крайне необходимо при контроле качества и безопасности применения живых краснушных вакцин.
 185-192
185-192


Дифференциация подвидов Francisella tularensis методом INDEL-типирования
Аннотация
Введение. Francisella tularensis, этиологический агент туляремии, относится к факультативным внутриклеточным патогенам, вызывающим тяжёлое заболевание у многих видов животных и человека, и является агентом биотерроризма категории А. В настоящее время F. tularensis делится на четыре подвида: F. tularensis subsp. tularensis (nearctica), F. tularensis subsp. holarctica, F. tularensis subsp. mediasiatica, F. tularensis subsp novicida, которые различаются по патогенности и географическому распределению. Исторически такое разделение было обусловлено различным ареалом циркуляции штаммов, их отличиями в биохимической активности и патогенностью для разных хозяев. Биохимическое определение подвидов весьма трудоёмко и требует работы с живыми культурами микроорганизма, что и определяет необходимость разработки новых молекулярно-генетических подходов для генотипирования штаммов F. tularensis.
Целью настоящего исследования является разработка способа дифференциации подвидов и отдельных групп F. tularensis на основе INDEL-типирования. Задачи исследования: создание локальной базы данных нуклеотидных последовательностей штаммов F. tularensis разных подвидов, поиск INDEL-маркеров, значимых для дифференциации подвидов возбудителя туляремии, конструирование праймеров для детекции INDEL-маркеров с помощью ПЦР, оптимизация набора INDEL-маркеров и выяснение филогенетических связей между изученными штаммами.
Материалы и методы. Локальную базу данных нуклеотидных последовательностей штаммов F. tularensis разных подвидов, представленных в базе данных GenBank, создавали с помощью авторского программного обеспечения. Детекцию INDEL-маркеров в геномах штаммов локальной базы данных проводили с помощью программы «GeneExpert». Конструирование праймеров и ПЦР in silico осуществляли при помощи программы «Primer3Plus» и авторской программы «VirtualPCR», кластерный анализ и построение филогенетического дерева — программы «GrapeTree».
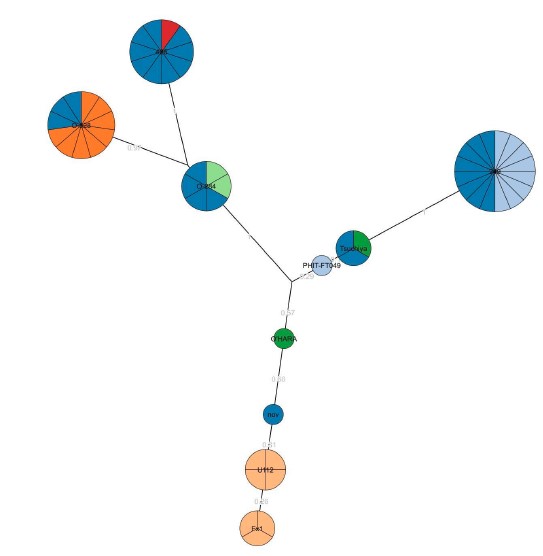
Результаты и обсуждение. Использование предложенных 5 INDEL-маркеров для генотипирования 29 изученных штаммов разных подвидов из базы данных GenBank позволило обнаружить 9 индивидуальных генотипов с высоким индексом разнообразия (DI = 0,85). Отмечено не только соответствующее разделение подвидов tularensis, holarctica, mediasiatica и novicida по разным кластерам, но и внутривидовое деление на группы штаммов. Дифференциация подвидов F. tularensis подтверждена in vitro на коллекции штаммов разных подвидов музея живых культур Ростовского-на-Дону противочумного института.
Заключение. Впервые разработана схема дифференциации подвидов F. tularensis на основе метода INDEL-типирования, позволяющая in vitro без необходимости секвенирования штаммов идентифицировать как подвиды F. tularensis (tularensis, holarctica, mediasiatica и novicida), так и группы штаммов внутри подвидов. Метод защищен патентом. Топология филогенетического дерева INDEL-генотипов штаммов F. tularensis коррелирует со схемами эволюции туляремийного микроба, представленными ранее. Предлагаемый метод может быть применён для комбинированного типирования штаммов F. tularensis совместно с MLVA- или SNP-типированием.
 193-202
193-202


Безопасность и иммуногенность препарата живой коклюшной вакцины ГамЖВК интраназального применения на экспериментальной модели детёнышей обезьян вида павиан гамадрил
Аннотация
Введение. В ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России разработана живая коклюшная вакцина ГамЖВК интраназального применения для профилактики коклюша, предназначенная для вакцинации детей младенческого возраста и ревакцинации всех возрастных групп населения. Доклинические исследования на сосунках мышей и крыс и взрослых обезьянах, а также клинические исследования на взрослых добровольцах показали безопасность и эффективность препарата ГамЖВК. Расширение области применения препарата ГамЖВК для вакцинации младенцев требует проведения дополнительных доклинических исследований безопасности и иммуногенности на наиболее адекватной экспериментальной модели детёнышей обезьян вида павиан гамадрил (Papio hamadryas).
Цель исследования: изучение безопасности и иммуногенности препарата ГамЖВК при интраназальном одно-, двух и трёхкратном введении детёнышам обезьян P. hamadryas.
Материалы и методы. В работе использовали 3 детёнышей обезьян P. hamadryas 1–2-месячного возраста, содержащихся в изолированном вольере вместе с матерями. Измерены показатели общего и биохимического анализов крови до и после иммунизации, а также экспериментальной инфекции. В сыворотках крови матерей и детёнышей определяли в динамике значения специфических антител класса IgG методом ИФА и титры общих противококлюшных антител в реакции агглютинации.
Результаты. Интраназальная иммунизация препаратом ГамЖВК детёнышей обезьян P. hamadryas приводила к формированию специфического гуморального иммунного ответа антител класса IgG (коклюшный токсин + филаментозный гемагглютинин), увеличению титра общих противококлюшных антител в реакции агглютинации, не вызывала местных и общих реакций организма и не изменяла показатели общего и биохимического анализов крови. Экспериментальная инфекция иммунизированных препаратом ГамЖВК детёнышей обезьян P. hamadryas не вызывала изменений лабораторных показателей крови и клинических проявлений, характерных для коклюшной инфекции.
 203-214
203-214


Ретроспективный серологический анализ распространения флавивирусных лихорадок и лихорадки Чикунгунья в Никарагуа — авидность специфических антител как инструмент дифференциальной диагностики
Аннотация
Введение. Арбовирусные инфекции представляют собой проблему для здравоохранения не только отдельных стран, но и всего мира в связи с повторяющимися вспышками в последнее десятилетие.
Целью настоящей работы было серологическое исследование распространённости вирусов денге (ДЕНВ), Зика (ЗИКВ), жёлтой лихорадки (ЖЛВ) и Чикунгунья (ЧИКВ) на примере ограниченной выборки в Никарагуа.
Материалы и методы. Одномоментно были исследованы 200 образцов сывороток крови, собранные в Никарагуа. Использовались доступные коммерческие диагностические наборы, а также in house-методы. Антитела (АТ) в положительных образцах сывороток оценивали по уровню авидности после обработки 8М мочевиной.
Результаты. АТ к одному или к нескольким вирусам одновременно имели 85 (42,5%) образцов. Индекс авидности (ИА) ≥ 30% был у 46 (23%) образцов, содержащих АТ только к одному вирусу. Из 39 (19,5%) образцов, содержащих АТ к нескольким вирусам, только 19 (9,5%) образцов содержали АТ с ИА ≥ 30% сразу к нескольким вирусам; 16 (8,0%) образцов имели АТ с высоким ИА к ДЕНВ и одновременно АТ с ИА < 30% к ЗИКВ и/или к ЖЛВ.
Обсуждение. Результаты анализа сывороток в тестах иммуноферментного анализа были скорректированы, т.к. только АТ с высоким ИА подтверждают инфицирование в анамнезе. Анализ авидности специфических АТ способствовал не только подтверждению случаев сочетанного или последовательного инфицирования в анамнезе, но и выявлению феномена кросс-реактивности АТ к флавивирусам. Наличие кросс-реактивных АТ, с одной стороны, мешает получить истинную картину инфицирования популяции флавивирусами, а с другой стороны, может увеличивать риск антителозависимого усиления заболевания, которое известно при вторичной лихорадке денге и при последовательном заражении ДЕНВ и ЗИКВ.
Заключение. Анализ авидности специфических АТ позволил подтвердить инфицирование в прошлом, в том числе несколькими вирусами, а также дифференцировать АТ с низкой авидностью, которые, вероятно, отражают феномен кросс-реактивности АТ к флавивирусам.
 215-224
215-224


Активность факторов периферической крови против Candida albicans
Аннотация
Введение. Колонизация разных биотопов человека дрожжеподобными грибами рода Candida встречается достаточно часто. При этом клиническая картина воспалительного процесса развивается не в каждом случае, что предполагает формирование уникального симбиоза между микроскопическим грибами и клетками организма человека, поддержание которого во многом зависит от активности иммунной системы. Основная масса исследований противогрибковой активности иммунной системы человека сконцентрирована вокруг патологических состояний, и практически не уделяется внимания таковой у здоровых лиц. Показано, что факторы иммунитета человека могут, с одной стороны, способствовать формированию биоплёнок C. albicans, а с другой стороны — принимают самое активное участие в их разрушении.
Цель исследования — изучение кандидацидной, антибиоплёночной, фагоцитарной и радикалпродуцирующей активности периферической крови здоровых доноров при использовании в качестве объекта клеток C. albicans.
Материалы и методы. От 32 практически здоровых доноров получали пробы периферической крови, изучали микоцидную активность, поглотительную и радикалпродуцирующую способность лейкоцитов, а также эффект сыворотки крови на биомассу плёнки. Для опсонизации клеток C. albicans использовали иммуноглобулины класса G (IgG) согласно апробированной ранее методике.
Результаты. Показана слабая микоцидная активность периферической крови здоровых доноров. Опсонизация C. albicans IgG существенно повышает эту функцию крови. В ранней фазе контакта с C. albicans дрожжеподобные клетки поглощают главным образом нейтрофильные лейкоциты, а мононуклеарные лейкоциты практически не участвуют в процессе фагоцитоза. Вероятно, их активность проявляется в более поздний период. Опсонизация C. albicans стимулирует поглотительную активность лейкоцитов, что отражается в увеличении среднего числа поглощённых объектов на один лейкоцит. Показано, что опсонины могут участвовать в усилении радикалпродуцирующей активности лейкоцитов. Так, инактивация белков системы комплемента нивелирует стимулирующий эффект опсонизации C. albicans.
Заключение. Таким образом, IgG и белки системы комплемента вносят существенный вклад в подавление патогенной активности C. albicans.
 225-230
225-230


ОБЗОРЫ
Роль цианотоксинов в патологии человека и животных (обзор)
Аннотация
Цианобактерии (ЦБ) являются древнейшей и широко распространённой формой жизни на Земле. Некоторые представители этих микроорганизмов образуют токсины, опасные для человека и животных. В работе приводятся данные о распространении токсинообразующих ЦБ, патогенезе действия токсинов на клетки и ткани человека, сельскохозяйственных, домашних и диких животных. Уделено серьёзное внимание нейротоксическому действию цианотоксинов (ЦТ), наиболее часто являющихся причиной гибели животных. ЦТ способны вызывать тяжёлые поражения центральной и периферической нервной системы, печени, почек, репродуктивной системы и пищеварительного тракта. Приводятся данные о гепатотоксическом, нефротоксическом, кардиотоксическом, иммунотоксическом действии ЦТ. Рассматривается их роль в возникновении тяжёлых дегенеративных процессов в мозге человека. Оценивается возможность влияния ЦТ на канцерогенез, особенно в печени, толстом кишечнике и прямой кишке. Отмечена ограниченность существующих данных о болезнетворности ЦБ и той помощи, которая необходима при вызванных ими поражениях. Обсуждается необходимость дальнейших исследований клинических проявлений патологических процессов, вызванных ЦТ, разработки методов диагностики и специфической терапии отравлений.
 231-243
231-243


Гнойно-септические инфекции у родильниц. Часть 2. Клинико-патогенетическая характеристика нозологических форм, этиология и антибиотикорезистентность (обзор литературы)
Аннотация
Несмотря на совершенствование системы оказания акушерской помощи, гнойно-септические инфекции (ГСИ) родильниц и связанная с ними материнская смертность не теряют актуальности. В данном исследовании проведён анализ публикаций на следующих информационных ресурсах: eLibrary, Google Scholar, PubMed, NCBI по клинико-патогенетической характеристике ГСИ послеродового периода (сепсис, перитонит, эндометрит, мастит и инфекции области хирургического вмешательства) и их ведущих возбудителей. Клиническая картина ГСИ послеродового периода не всегда соответствует степени активности инфекционного процесса, что приводит к поздней диагностике локального очага инфекции и в дальнейшем к генерализации инфекционного процесса. Современной чертой ГСИ родильниц является их полиэтиологичность с преобладанием условно-патогенных микроорганизмов, роль отдельных представителей которых неоднозначна. В последние годы увеличивается этиологическая и эпидемиологическая значимость грамотрицательных микроорганизмов семейства Enterobacteriaceae, в том числе с множественной лекарственной устойчивостью. Таким образом, несмотря на достаточное количество информации об этиологии и клинико-патогенетических особенностях ГСИ послеродового периода, необходим междисциплинарный подход к изучению этой проблемы с участием акушеров-гинекологов, микробиологов, клинических фармакологов и эпидемиологов.
 244-259
244-259


НЕКРОЛОГИ
 260-262
260-262