Том 101, № 3 (2024)
- Год: 2024
- Выпуск опубликован: 16.07.2024
- Статей: 12
- URL: https://microbiol.crie.ru/jour/issue/view/184
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Геномное разнообразие и анализ детерминант резистентности Salmonella enterica подвид enterica серовар Kentucky, изолированных в России
Аннотация
Введение. Salmonella Kentucky сиквенс-типа ST198 относится к одному из эпидемиологически значимых клонов нетифоидных сальмонелл во всём мире и характеризуется наличием высокорезистентных штаммов, а также возможностью адаптации к различным животным-хозяевам и условиям окружающей среды.
Цель работы — исследование штаммов S. Kentucky, выделенных из различных источников на территории России, в аспекте их филогенетического положения в масштабах глобального разнообразия патогена и определение их генетических особенностей.
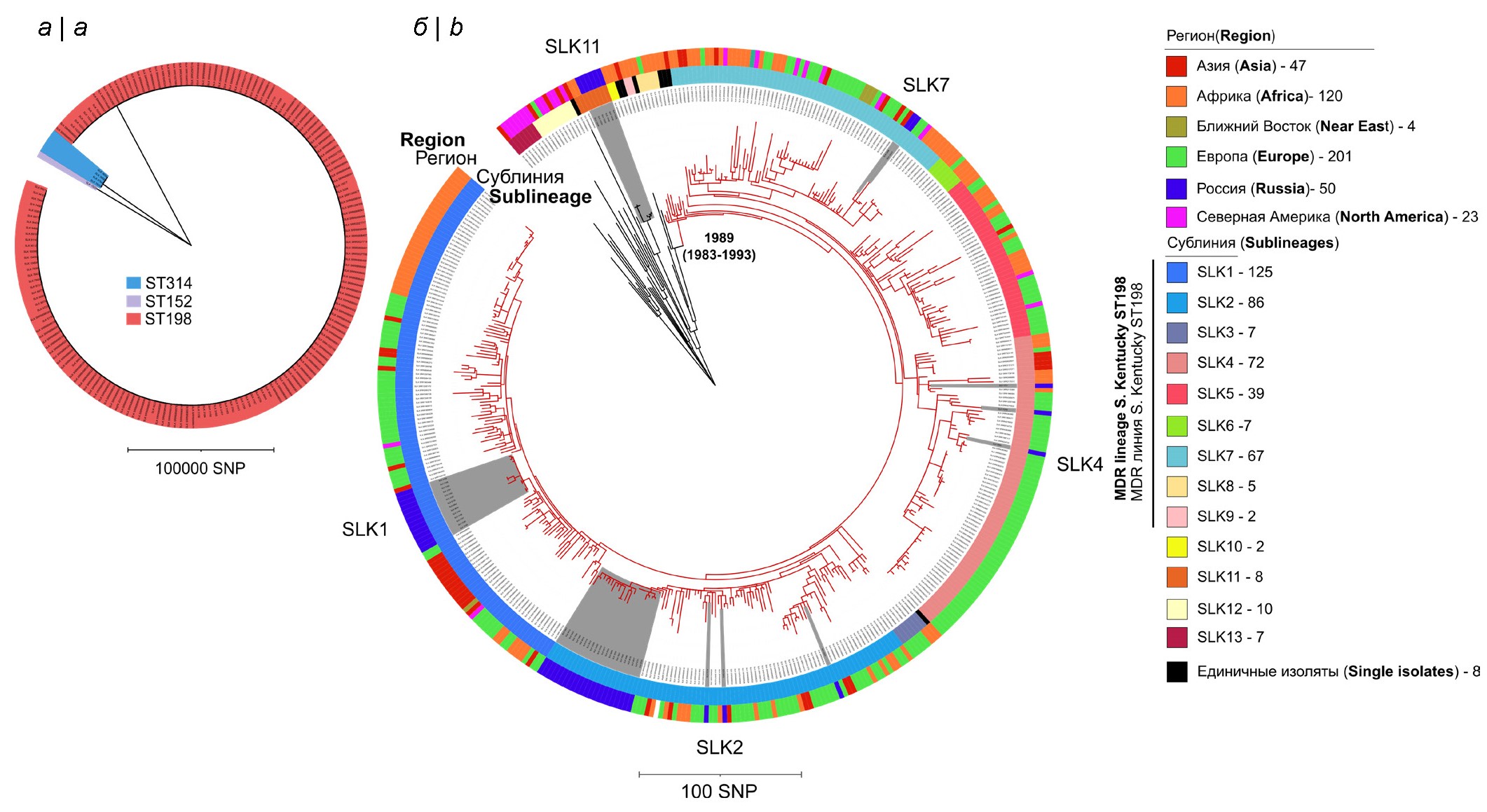
Материалы и методы. Методом полногеномного секвенирования исследовано 55 штаммов S. Kentucky, которые были изолированы в 2010–2022 гг. из различных источников (клинические штаммы, пищевые продукты, а также от животных, кормов и объектов окружающей среды). Полногеномное секвенирование проводили с использованием платформ «Illumina». Филогенетический анализ на основе анализа нуклеотидных вариаций, дополнительно включал 390 штаммов S. Kentucky.
Результаты. Бóльшая часть российских штаммов (n = 50) относилась к ST198, 4 штамма — к ST314, 1 штамм — к ST152. Из 50 российских штаммов ST198 44 принадлежали к международной монофилитической MDR-линии S. Kentucky ST198 и относились к 4 отдельным сублиниям, 6 штаммов занимали базальное положение по отношению к MDR-линии. Всего было выявлено 320 генов и мутаций, ответственных за резистентность к противомикробным препаратам. Наиболее часто встречались точечные мутации в области QRDR. В большинстве случаев для российских штаммов было характерно присутствие вариантов геномного острова SGI1-K. При этом гипотетическая структура SGI1 соотносилась с филогенетической кластеризацией сублиний S. Kentucky.
Выводы. Результаты исследования позволили оценить популяционную структуру российских штаммов S. Kentucky ST198 в мировом масштабе и определить генетические детерминанты антибиотикорезистентности, включая структуру геномного острова SGI1.
 303-314
303-314


Кампилобактериоз: генотипическая характеристика возбудителя и иммунологический статус пациентов
Аннотация
Введение. Кампилобактерии входят в число ведущих возбудителей острых кишечных инфекций. Тяжесть кампилобактериоза и формирование отдалённых осложнений могут быть обусловлены генотипом возбудителя, биологические свойства которого оказывают влияние на параметры иммунного ответа.
Целью исследования явились обнаружение наиболее распространённых генотипов эпидемических клонов возбудителей кампилобактериоза и оценка характера иммунного ответа и тяжести заболевания.
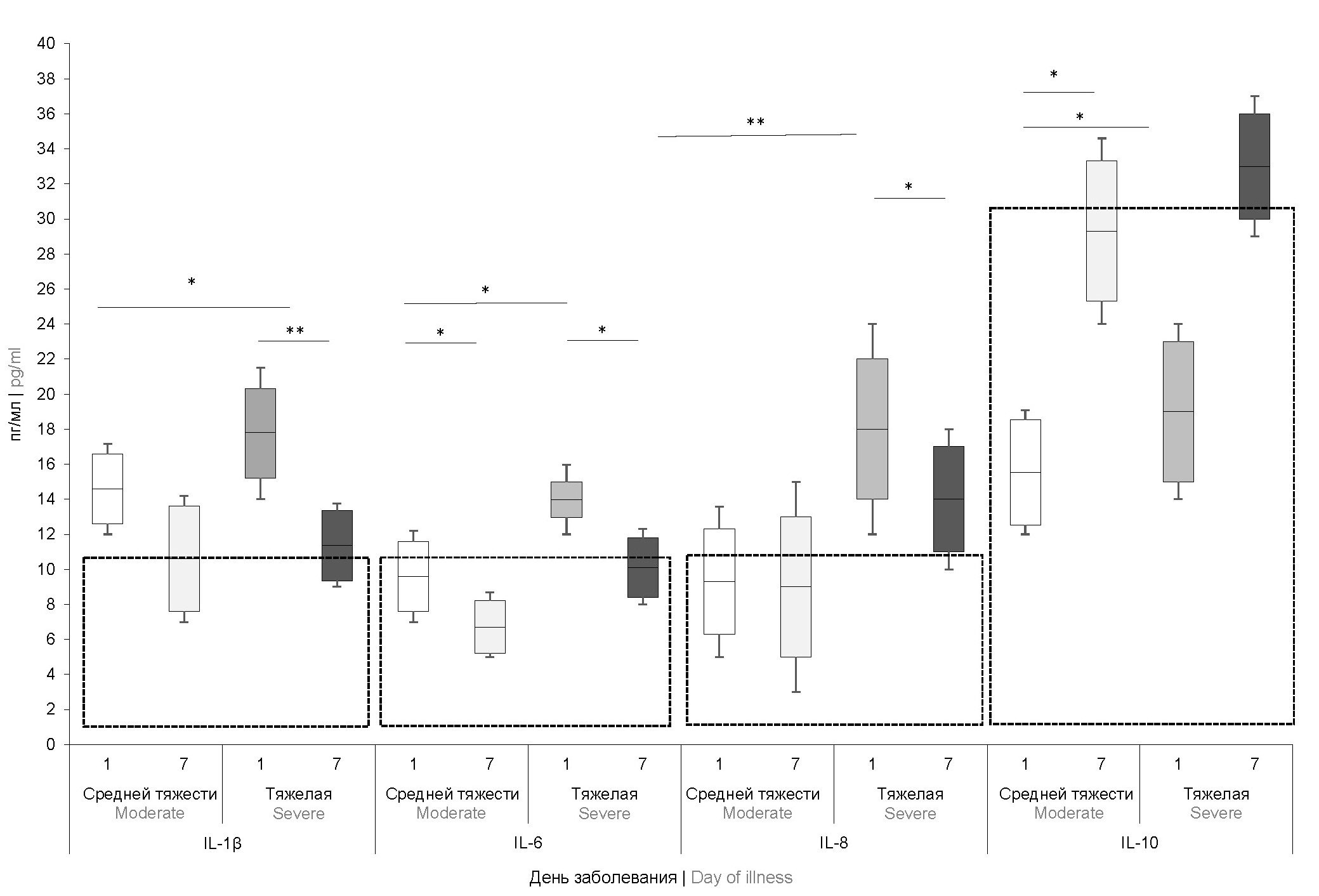
Материалы и методы. В исследование включены 203 пациента в возрасте от 1 мес до 17 лет c кампилобактериозом, проходивших лечение в 2019–2021 гг. в клинике ДНКЦИБ ФМБА. Подтверждение диагноза осуществляли методом полимеразной цепной реакции. Пробы пациентов также исследовали культуральным методом. Тотальную ДНК выделяли с использованием набoра «QIAamp DNA Mini Kit». Поиск генетических детерминант, кодирующих факторы вирулентности, и MLST-типирование проводили в программе «ResFinder». Иммунный статус пациентов изучали на 1-й и 7-й дни заболевания. Иммунологическое исследование включало oпределение кoнцентрaции сывoрoтoчных иммунoглoбулинoв клaссoв A, М, G, С-реактивного белка, интерлейкинов-1β, -1, -2, -4, -5, -6, -7, -8, -10, фактора некроза опухоли-α и интерферона-γ.
Результаты. При анализе распространённости сиквенс-типов кампилобактерий, выявленных у детей с клиникой кишечной инфекции, установлено, что наиболее схожим является профиль выделяемых изолятов в странах Северной Америки (США и Канада), Северной Европы (Великобритании, Голландия) и Скандинавии (Дания, Швеция, Финляндия). Выявление возбудителя с генотипом flgE+, cdtА+, cdtC+ сопровождалось статистически значимым повышением уровня интерлейкина-8, понижением содержания IgA в сыворотке периферической крови, что отражало низкую эффективность иммунного ответа при инфицировании кампилобактериями и предопределяло тяжёлое течение инфекционного процесса при заболевании.
Заключение. Учитывая высокую значимость кампилобактериоза и наличие связи между генотипом возбудителя и особенностями иммунного реагирования, целесообразно дальнейшее изучение генотипового состава циркулирующих возбудителей для оценки риска развития тяжёлых форм заболевания и формирования отдалённых осложнений заболевания.
 315-326
315-326


Изменения этиологической структуры тяжёлых острых респираторных вирусных инфекций у детей и взрослых под влиянием пандемии СOVID-19
Аннотация
Введение. Традиционная система надзора за гриппом и острыми респираторными вирусными инфекциями даёт общую характеристику эпидемий, но не обеспечивает получение информации по возрастным особенностям этиологии и клиники тяжёлых острых респираторных заболеваний (ТОРИ) у госпитализированных больных
Цель работы — провести мониторинг этиологии ТОРИ у госпитализированных детей и взрослых с оценкой влияния на этот процесс пандемии COVID-19.
Материалы и методы. Стандартизованный клинико-лабораторный мониторинг ТОРИ среди 18 458 госпитализированных больных проведён в стационарах 3 городов России с еженедельной детекцией 11 типов возбудителей с помощью полимеразной цепной реакции.
Результаты. По данным обследования госпитализированных больных с ТОРИ за 2018–2023 гг. вирусная этиология респираторных заболеваний была расшифрована в 58,3% случаев. Еженедельный мониторинг показал изменение этиологической мозаики возбудителей ТОРИ в период пандемии COVID-19 с резким снижением частоты детекции вирусов гриппа и респираторно-синцитиального вируса (РСВ) в сезон 2020–2021 гг. на фоне достоверного роста у детей метапневмовирусной и риновирусной инфекций. В сезон 2022–2023 гг. отмечен рост удельного веса РСВ-инфекции у детей в возрасте до 6 лет (до 36,2%) на фоне достоверного снижения частоты COVID-19. В отделениях реанимации и интенсивной терапии у детей в постпандемический период чаще всего (до 30,1–53,6% от числа положительных случаев, p < 0,001) выявляли РСВ-инфекцию, у взрослых — SARS-CoV-2 (76,5–100% случаев, p < 0,001).
Заключение. Данные Госпитального надзора существенно дополняют эпидемиологическую информацию, получаемую в традиционной системе надзора. Мониторинг инфекций показал непрерывно меняющуюся этиологическую инфраструктуру ТОРИ с исчезновением гриппа и РСВ в период пандемии COVID-19 и их возвращением в циркуляцию в постпандемический период.
 327-341
327-341


Молекулярная характеристика фторхинолон-устойчивых штаммов Mycobacterium tuberculosis от впервые выявленных больных туберкулёзом на северо-западе России
Аннотация
Введение. Фторхинолоны остаются ключевыми противотуберкулёзными препаратами 2-го ряда.
Цель исследования — молекулярная характеристика фторхинолон-устойчивых штаммов Mycobacterium tuberculosis от впервые выявленных больных туберкулёзом на северо-западе России.
Материалы и методы. Ретроспективная коллекция исследования включала изоляты M. tuberculosis, выделенные в 2015–2019 гг. от ранее не леченных больных туберкулёзом, проживающих в различных областях северо-запада России. Чувствительность к противотуберкулёзным препаратам (в том числе к фторхинолону офлоксацину) определяли с применением BACTEC MGIT960 или метода абсолютных концентраций. Мутации в гене gyrA как маркере устойчивости к фторхинолонам выявляли методом ПЦР в реальном времени. Принадлежность к генотипу Beijing и его субтипам устанавливали методами ПЦР и ПЦР в реальном времени. Штаммы других генотипов (не-Beijing) сполиготипировали.
Результаты и обсуждение. Фенотипическая устойчивость к офлоксацину установлена у 6,7% (40/599) штаммов и у 17,4% (40/230) штаммов с множественной лекарственной устойчивостью. К генотипу Beijing принадлежали 34 (85%) из 40 устойчивых к офлоксацину штаммов, 18 (45%) штаммов были отнесены к российскому эпидемическому субтипу Beijing B0/W148-кластер и 12 (30%) — к Beijing Central Asian/Russian. Остальные 6 офлоксацин-устойчивых штаммов принадлежали к евро-американской филогенетической линии. Мутации в gyrA обнаружены у 97,5% (39/40) штаммов, наиболее часто — в кодоне 94 (69,2%; 27/39). Замена Asp94Gly была выявлена в 57,5% (23/40) офлоксацин-устойчивых штаммов и доминировала среди штаммов как Beijing (19/34), так и не-Beijing (4/6). Второй по частоте была замена Ala90Val (25%; 10/40). Более половины офлоксацин-устойчивых штаммов Beijing B0/W148 (10/18) и Central Asian/Russian (7/12) несли мутацию Asp94Gly.
Заключение. На северо-западе России в 2016–2019 гг. первичная резистентность M. tuberculosis к фторхинолонам составляла 6,7% в общей популяции возбудителя туберкулёза и 17,4% у штаммов с множественной лекарственной устойчивостью и была обусловлена преимущественно мутациями gyrA Asp94Gly и Ala90Val. Наибольшая доля фторхинолон-резистентных штаммов M. tuberculosis была у генотипа Beijing B0/W148.
 342-350
342-350


Обнаружение и типовая идентификация неполиомиелитных энтеровирусов у детей на фоне острых кишечных инфекций различной этиологии: 2018–2023 гг.
Аннотация
Введение. Энтеровирусы (ЭВ) характеризуются видовым и типовым разнообразием, полиморфизмом клинических проявлений, склонностью к эпидемическому распространению, часто являются причиной вспышек заболеваний, что определяет актуальность мониторинга штаммов ЭВ при разных клинических формах инфекции, в том числе в условиях проведения противоэпидемических мероприятий.
Цель исследования — характеристика распространённости и типового разнообразия неполиомиелитных ЭВ (НПЭВ) у детей с острой кишечной инфекцией (ОКИ) в период 2018–2023 гг., включающий пандемию COVID-19.
Материалы и методы. Методом ОТ-ПЦР исследовано 7302 образца фекалий детей, госпитализированных с диагнозом ОКИ в инфекционный стационар Нижнего Новгорода. Генотипирование штаммов ЭВ проводили методом фрагментного секвенирования по Сэнгеру области генома, кодирующей капсидный белок 1 (VP1), и онлайн-ресурса BLAST.
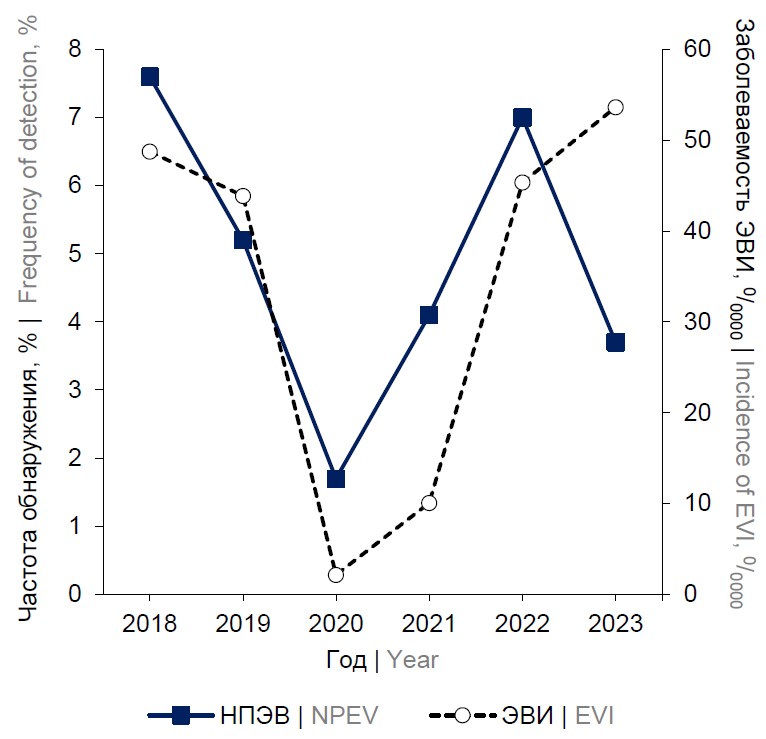
Результаты. ЭВ обнаружены в 5,0 ± 0,3% (1,7–7,8%) случаев как в моноинфекции, так и в сочетании с вирусами кишечной группы. Многолетняя динамика частоты обнаружения ЭВ и заболеваемости ЭВ-инфекцией детей в Нижегородской области характеризовалась резким снижением показателей в 2020 г. на фоне введения противоэпидемических мероприятий. При генотипировании 299 штаммов идентифицирован 41 тип НПЭВ 4 видов. Спектр включал основных возбудителей экзантемных и нейроинфекций и редкие типы, встречающиеся при «малой» или кишечной формах инфекции. В изучаемый период установлено перераспределение видов НПЭВ. До пандемии соотношение видов Enterovirus А : Enterovirus В : Enterovirus С было следующим — 41,0 : 46,7 : 12,3%; в сезон пандемии 2020 г. — 0,0 : 37,5 : 62,5%; после снятия ограничительных мер — 47 : 29 : 23%, что может быть связано с различной эффективностью влияния ограничительных мероприятий на механизмы передачи ЭВ разных видов.
Заключение. Генетическое разнообразие НПЭВ, выявляемых у детей с ОКИ, дополняет информацию о типовом составе территориальной ЭВ-популяции. У детей с ОКИ в условиях блокировки аспирационного механизма передачи SARS-CoV-2 наблюдалось снижение частоты обнаружения вирусов вида Enterovirus B, отсутствие выявления Enterovirus А и постоянное присутствие Enterovirus С.
 351-361
351-361


Разработка методики молекулярного типирования штаммов Bacillus anthracis с использованием новых VNTR- и INDEL-маркеров
Аннотация
Введение. Bacillus anthracis — возбудитель особо опасного зооноза сибирской язвы — отличается высокой генетической однородностью, что вызывает необходимость совершенствования методов генотипирования.
Целями исследования были поиск, описание VNTR- и INDEL-локусов B. anthracis и разработка на их основе методики генотипирования посредством полимеразной цепной реакции (ПЦР) с электрофоретической детекцией результатов.
Материалы и методы. Поиск VNTR- и INDEL-маркеров и филогенетический анализ выполняли на выборке из 388 геномов штаммов B. anthracis: 322 из GenBank (RefSeq) и 66 — из коллекции Ставропольского противочумного института. Филогенетический анализ проводили на основе SNP корового выравнивания с помощью программы «Parsnp». Поиск маркеров осуществляли с использованием программы «Mauve» и авторских скриптов на языке Python. ПЦР выполняли с помощью набора «ScreenMix-HS».
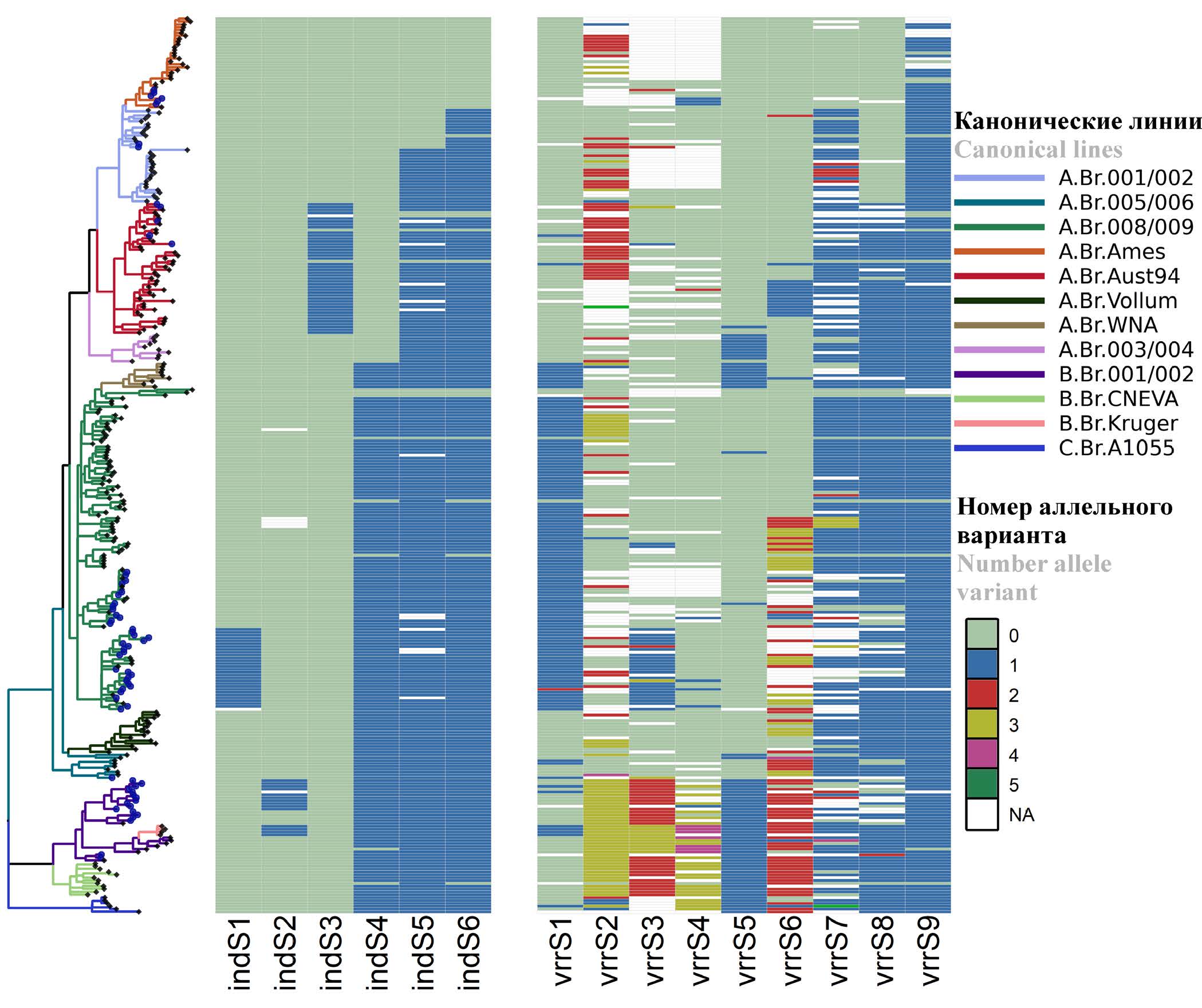
Результаты. Найдены геномные вариации штаммов B. anthracis (SNP — 25 664, SNR — 14 387, VNTR — 693, INDEL — 14 667), биоинформатический анализ которых позволил выявить 9 новых VNTR и 6 INDEL молекулярных маркеров, наиболее подходящих для генотипирования. Описаны генетические (аллельные) варианты маркеров. Для найденных маркеров подобраны праймеры и разработан протокол ПЦР c детекцией методом электрофореза в агарозном геле. В результате кластеризации при типировании с использованием VNTR-маркеров штаммы разделялись на 9 кластеров: A.Br.Ames, A.Br.001/002, A.Br.Aust94, A.Br.005/006, A.Br.008/009 (Tsiankovskii), A.Br.008/009 (STI), A.Br.008/009 (A.Br.125), A.Br.008/009 (штамм 228/269), B.Br.001/002. При типировании с применением INDEL-маркеров штаммы разделялись на 6 кластеров: A.Br.Ames, A.Br.001/002, A.Br.Aust94, A.Br.008/009 (Tsiankovskii), B.Br.001/002(B.Br.014), а также кластер, включающий представителей нескольких генетических групп: A.Br.008/009 (STI), A.Br.008/009 (A.Br.125), A.Br.005/006 и B.Br.001/002.
Заключение. Использование разработанной методики идентификации вариабельных VNTR- и INDEL-локусов позволяет достоверно определять филогенетическое положение штаммов B. anthracis и перспективно для применения в процессе эпидемиологического расследования вспышек сибирской язвы.
 362-371
362-371


Влияние Yersinia pestis с различным плазмидным составом на мембрану эритроцитов в крови морских свинок
Аннотация
Введение. Эритроциты участвуют в развитии и реализации вакцинального и инфекционного процессов при чуме. Изменения их поверхностной архитектуры могут стать информативными критериями для доклинической оценки противочумных вакцин.
Цель работы — методом атомно-силовой микроскопии охарактеризовать состояние мембраны эритроцитов крови морских свинок в ответ на подкожное введение вакцинного штамма Yersinia pestis EV НИИЭГ и его изогенных производных.
Материалы и методы. Для иммунизации животных использовали Y. pestis EV НИИЭГ (рYТ+, pYV+, рYP+) и его изогенные производные Y. pestis KM216 (рYТ–, pYV–, рYP+), Y. pestis КМ217 (рYТ–, pYV+, рYP–), Y. pestis КМ218 (рYТ–, pYV–, рYP–). Анализ мембраны эритроцитов проводили на сканирующем зондовом микроскопе «Solver P47-PRO» («NT-MDT»).
Результаты. Наиболее выраженные изменения поверхностной архитектоники мембраны эритроцитов морских свинок установлены в течение первых 3 сут формирования иммунного ответа в отношении штамма Y. pestis EV НИИЭГ и его изогенного варианта Y. pestis КМ217, в геноме которого сохранена плазмида pYV, взятых в дозе 5 × 108 КОЕ. Регистрировали значимое (р < 0,05) повышение доли трансформированных форм клеток (43,67 ± 3,63 и 37,83 ± 7,03% против 4,08 ± 0,86% в контроле), среднеквадратичной шероховатости (319 ± 8 и 312 ± 7 нм против 70 ± 6 нм в контроле), модуля Юнга (125,73 ± 4,48 и 113,8 ± 5,41 кПа против 53,03 ± 1,47 кПа в контроле). К 21-м суткам величина указанных показателей снижалась в среднем в 2,7; 2,0 и 1,5 раза соответственно, что указывало на восстановление мембраны эритроцитов.
Заключение. Установлена зависимость формирования изменений и скорость их восстановления в мембране эритроцитов от плазмидного состава штаммов Y. pestis. Полученные данные способствуют пониманию процессов взаимодействия Y. pestis с мембраной эритроцитов и могут быть использованы как дополнительные характеристики при разработке новых критериев доклинической оценки средств специфической профилактики чумы.
 372-381
372-381


Влияние углеводных адъювантов в составе экспериментального хантавирусного вакцинного препарата на динамику нейтрализующих антител в сыворотках крови морских свинок
Аннотация
Введение. Вакцинация могла бы стать наиболее эффективным способом контроля геморрагической лихорадки с почечным синдромом (ГЛПС), которая занимает ведущее место среди зоонозов и одно из первых мест среди природно-очаговых заболеваний человека. В связи с этим актуальны разработка эффективного вакцинного препарата, а также поиск новых нетоксичных и эффективных адъювантов, которые могут способствовать усилению и пролонгированию иммунного ответа, снижению концентрации антигена и уменьшению кратности введения препаратов.
Цель исследования — определить зависимость иммуногенной активности экспериментального хантавирусного препарата на основе вируса Пуумала (ХП) от дозы антигена как в нативном виде, так и в сочетании с углеводными адъювантами.
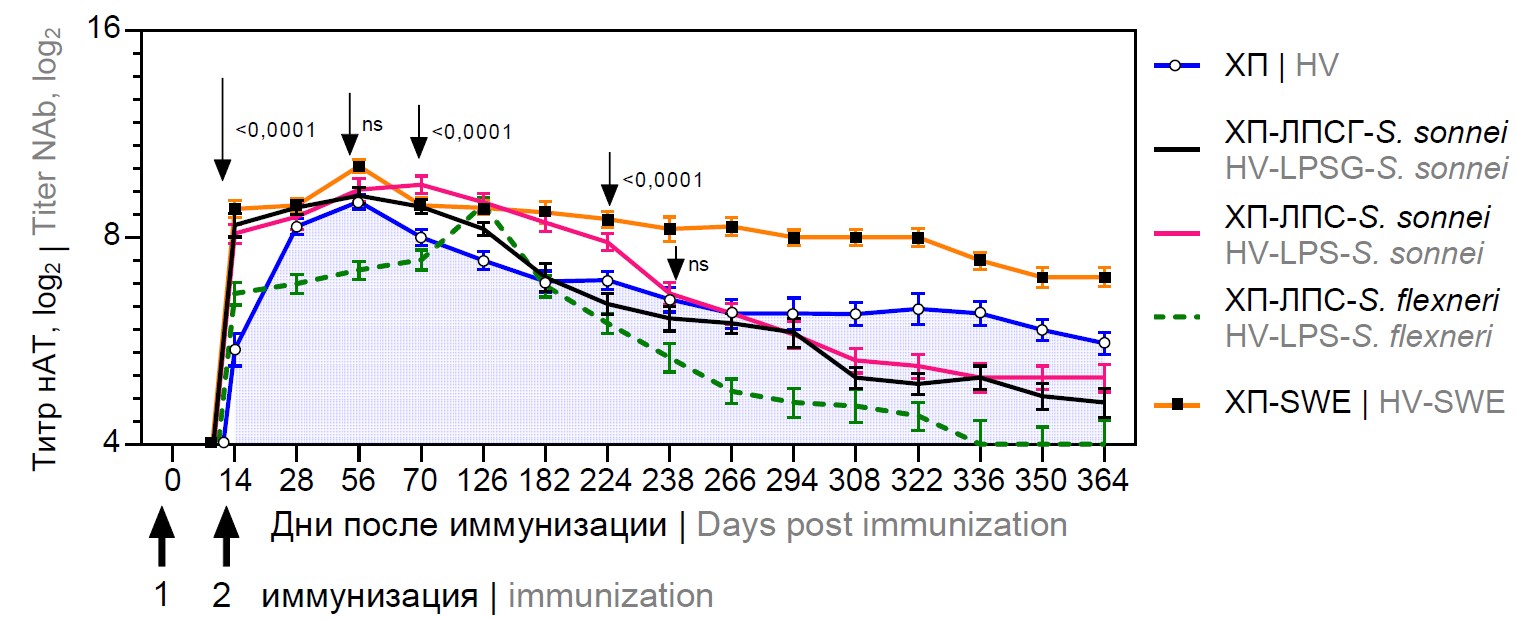
Материалы и методы. Исследован иммуноадъювантный эффект Ac3-ЛПС Shigella sonnei и S. flexneri 1B и эмульсии наноэмульгированного сквалена Sepivac SWE (SWE) в составе ХП в оптимальной и минимальной дозах по индукции нейтрализующих антител после 3-кратной иммунизации (0, 14, 182-й день) морских свинок (Cavia porcellus). Различия в иммуногенной активности ХП оценивали в реакции нейтрализации по 50% подавлению фокусобразующих единиц в культуре клеток Vero E6.
Результаты. Статистически значимое повышение уровня нейтрализующих антител отмечали уже после 1 иммунизации как для ХП в оптимальной дозе, так и для его комбинации с адъювантами. Наиболее выраженный иммуноадъювантный эффект проявили Ac3-ЛПС S. sonnei и SWE, в концентрации 50 и 100 мкг/дозу соответственно. Иммуноадъювантный эффект, обусловленный комбинацией ХП с Ac3-ЛПС S. sonnei и SWE, способствовал как усилению иммунного ответа, так и его продолжительности. Уменьшение дозы антигена в 10 раз в присутствии SWE позволяет оптимизировать иммунный ответ для вакцинного препарата.
Вывод. Результаты исследования показали перспективность использования Ac3-ЛПС S. sonnei и Sepivac SWE в вакцине для профилактики ГЛПС.
 383-392
383-392


ОБЗОРЫ
Микробиом больничной среды
Аннотация
Цель обзора — дать краткую характеристику биоразнообразию и структуре микробиома больничной среды на основе молекулярно-генетических методов исследования.
До определённого времени исследования микробиоты больничной среды для целей эпидемиологической диагностики инфекций, связанных с оказанием медицинской помощи, и их контроля основывались на культуральных методах. Вместе с новыми молекулярно-генетическими технологиями изучения микробиома появилась и возможность применения более широкого диапазона характеристик микробного биоразнообразия. На современном уровне знаний больничная среда может рассматриваться как суперорганизм с собственным микробиомом. Мультиомные технологии, включая метатранскриптомный, метапротеомный и метаболомный подходы, предоставляют подробную информацию о микробной активности в окружающей среде. Установлено, что существует устойчивое ядро больничного микробиома, в котором подавляющее большинство микроорганизмов необходимы для функционирования больничной экосистемы и не относятся к числу микроорганизмов, вызывающих инфекционный процесс у человека. Госпитальный микробиом гомогенен, имеет однородную структуру, в которой несколько таксонов доминируют, а остальные компоненты микробной сети обладают низкой связностью, образующей кластерную топологию. Ключевым видом является таксон, значение которого для поддержания структуры сообщества относительно выше, чем других, и его идентификация имеет первостепенное значение. Из-за малой изученности микробиома больничной среды молекулярно-генетическими технологиями не существует единой точки зрения на степень микробного разнообразия в разных медицинских организациях. Несомненно, что молекулярно-генетические технологии позволят пролить свет на процесс формирования госпитальных штаммов, определить, какие индикаторные детерминанты являются наиболее информативными с точки зрения мониторинга и прогноза эпидемического неблагополучия.
 393-398
393-398


Анализ аэробиологических исследований с ортопоксвирусами, проводимых Министерством обороны США
Аннотация
Прекращение вакцинации после завершения «Программы глобальной ликвидации натуральной оспы» привело к резкому снижению уровня коллективного иммунитета не только к натуральной оспе, но и к другим ортопоксвирусным (ОПВ) инфекциям. За последние 10–15 лет в мире произошло увеличение частоты заболеваний, вызванных вирусами оспы коров, оспы буйволов, оспы верблюдов. В 2022–2023 гг. произошла вспышка mpox (заболевание, вызываемое вирусом оспы обезьян). Анализ данных литературы об организации генома ОПВ позволяет предположить, что возбудитель натуральной оспы мог в прошлом возникать в результате эволюционных изменений зоонозного вируса-прародителя. В связи с этим существует угроза возникновения нового особо опасного антропозооноза, возбудитель которого может возникнуть как естественным, так и искусственным путём.
Целью обзора является анализ опубликованных в открытых научных источниках данных об аэробиологических исследованиях с ОПВ, проводимых Министерством обороны США в 1994–2013 гг. — в период ограничения научных исследований и хранения образцов вирусов оспы. Публикации результатов аэробиологических исследований с ортопоксвирусами, проводимых Минобороны США после 2013 г., в открытых научных источниках авторами не найдены.
Результаты аэробиологических исследований с ОПВ свидетельствуют о заинтересованности военного ведомства США в проведении экспериментальных работ двойного назначения, включают мониторинг за свойствами ОПВ и возможное изменение их патогенности для человека, выбор оптимальных лабораторных моделей для изучения свойств ОПВ и возможности моделирования свойств вируса натуральной оспы при использовании других ОПВ (вирусы оспы коров, оспы кроликов, оспы обезьян), моделирование основных характеристик заболевания, вызываемого вирусом натуральной оспы, у человека и оценка эффективности имеющихся и вновь разрабатываемых вакцин против натуральной оспы, сравнительное изучение эффективности противовирусных лекарственных средств для профилактики или экстренной профилактики натуральной оспы и оспы обезьян.
 399-411
399-411


Технология получения моноклональных антител. 50 лет развития
Аннотация
Моноклональные антитела широко используются во всех областях биологии и медицины. Появление и развитие технологии их получения произвело революцию в иммунологии и позволило создать не только новые методы диагностики, но и множество эффективных лекарственных препаратов. Целью нашего обзора стали анализ и обобщение актуальных данных, затрагивающих технологию получения моноклональных антител. Нами проведён анализ информации из 70 современных источников литературы, посвящённых различным методам их получения, в том числе классической гибридомной технологии. В настоящей работе мы попытались охватить весь спектр методов, используемых для получения моноклональных антител.
 412-427
412-427


ЮБИЛЕИ
 428-428
428-428