Том 97, № 5 (2020)
- Год: 2020
- Дата публикации: 04.11.2020
- Статей: 12
- URL: https://microbiol.crie.ru/jour/issue/view/39
Весь выпуск
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Распределение серопревалентности к SARS-CoV-2 среди жителей Тюменской области в эпидемическом периоде COVID-19
Аннотация
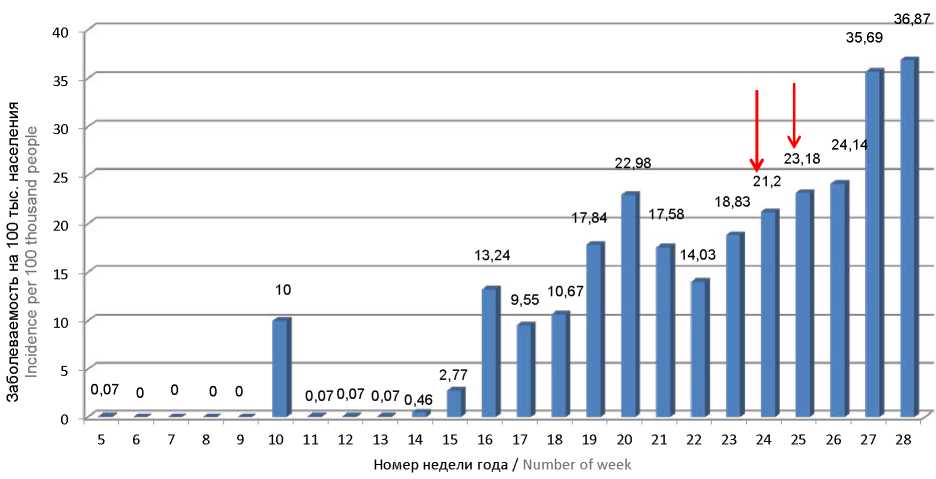
Введение.В конце 2019 г — начале 2020 г была зарегистрирована вспышка инфекции, вызванная новым штаммом бета-коронавируса SARS-CoV-2. ВОЗ определила идентифицированное заболевание как «коронавирусная болезнь 2019» (COVID-19). В Тюменской области первый случай заболевания COVID-19 был диагностирован 31.01.2020 г. Источником инфекции была студентка, приехавшая из Цзинаня, провинция Шаньдун (КНР). С 16-й по 28-ю неделю 2020 г наблюдался устойчивый рост заболеваемости. Максимальный уровень составил 36,87 на 100 тыс. человек. Впоследствии кумулятивная заболеваемость постепенно увеличивалась, хотя и с меньшей интенсивностью.
Целью сероэпидемиологического исследования было определение уровня и структуры популяционного иммунитета к вирусу SARS-CoV-2 среди населения Тюменской области в период интенсивного распространения COVID-19.
Материалы и методы. Отбор добровольцев для исследования проводился путем анкетирования и рандомизации. Критерием невключения являлась активная инфекция COVID-19 на момент обследования. На наличие специфических антител к SARS-CoV-2 были обследованы 2758 человек. Возраст опрошенных добровольцев составлял от 1 года до 70 лет и старше.
Результаты исследования. Среди населения Тюменской области в активной фазе заболеваемости COVID-19 наблюдалась умеренная (24,5%) серопревалентность к SARS-CoV-2. Одновременно с этим выявлена высокая (97,8%) частота случаев бессимптомной инфекции у серопозитивных людей, у которых в анамнезе не было заболевания COVID-19, положительного результата ПЦР и симптомов острых респираторных вирусных инфекций в день обследования. Максимальные показатели коллективного иммунитета, установленные у детей 1-6 лет (34,7%), были статистически значимыми по сравнению со средним уровнем серопревалентности для всей когорты. У реконвалесцентов COVID-19 антитела обнаруживались в 68,2% случаев. У лиц с положительным результатом ранее проведенного ПЦР-анализа антитела выявляются в 64% случаев.
Вывод. Результаты исследования состояния коллективного иммунитета к вирусу SARS-CoV-2 необходимы для разработки прогноза развития эпидемиологической ситуации, а также для планирования мероприятий по специфической и неспецифической профилактике COVID-19.
 392-400
392-400


Особенности изменений спектров жирных кислот бактерий семейства Enterobacteriaceae в процессе формирования устойчивых (дормантных) клеточных форм
Аннотация
Введение. С появлением парадигмы гетерогенности популяции бактерий возросло внимание к фенотипу дормантных (дремлющих) клеток, активная генерация которых происходит при неблагоприятных условиях среды обитания микроорганизмов. Эти клетки характеризуются метаболическим и репродуктивным покоем, а также резистентностью к антибиотикам. Однако при наступлении благоприятных для них условий обитания они способны вновь прорастать и вызывать обострение инфекционных заболеваний. С этими фенотипами патогенных бактерий связывают угрожающее снижение эффективности антимикробной терапии, рост уровня заболеваемости персистирующими, хроническими и госпитальными инфекциями. С учетом ключевой роли в адаптации бактерий жирных кислот (ЖК) целью исследования было выявление специфических особенностей изменений ЖК-состава грамотрицательных бактерий семейства Enterobacteriaceae в процессе их многолетнего хранения в экстремальных условиях и формирования дормантных (некультивируемых) субпопуляций клеточных форм.
Материалы и методы. Для исследования использовали статические культуры эталонных штаммов: Yersinia pseudotuberculosis, Salmonella enterica Typhimurium и Escherichia coli, хранившиеся под вазелиновым маслом при 4-8оС в течение 5-10 лет. Дормантные клеточные формы получали путем удаления масляного слоя и сбора микробной массы. Ультраструктурные признаки дормантных клеточных форм были подтверждены трансмиссионной электронной микроскопией. Жизнеспособность дормантных клеток оценивали молекулярно-генетическим методом. Отсутствие репродуктивной активности дормантных форм проверяли путем многократных посевов на LB-бульон, среды Эндо и Серова и инкубации при 4-6, 22-24 и 37оС. Получение метиловых эфиров общих ЖК проводили по методике, утвержденной Европейским комитетом по стандартизации и рекомендованной Sherlock MIS-протоколом. Анализ метиловых эфиров ЖК осуществляли методом газовой хроматографии в сочетании с масс-спектрометрией. После предварительной гомогенизации микробных масс бактерий липиды экстрагировали, спектры ЖК получали методом электронного удара при 70 эВ.
Результаты. Доказано, что в экстремальных условиях (низкая температура, недостаток питательных веществ, гипоксия) в популяции E. coli, Y. pseudotuberculosis и S. Typhimurium формируется фенотипическая некультивируемая генерация дормантных клеток. Сравнительный анализ изменений ЖК-спектра в дормантном фенотипе выявил определенные особенности по сравнению с вегетативными клетками, связанные со снижением индекса ненасыщенности и доминированием длинноцепочечных насыщенных ЖК (С14-С18).
Выводы. Биологическое значение выявленных трансформаций связано, по-видимому, с особой ролью этих фракций ЖК в обратимом формировании дремлющего (некультивируемого) клеточного фенотипа и как альтернативного источника углеводов в метаболически неактивном состоянии, а также в их последующей реверсии в вегетативные клетки при наступлении благоприятных условий существования.
 401-412
401-412


Чувствительность биопленок Bordetella pertussis к поливалентной коклюшной сыворотке
Аннотация
Цель работы — изучение чувствительности биопленок Bordetella pertussis к поливалентной коклюшной сыворотке (ПКС).
Материалы и методы. Интенсивность образования биопленок штаммами B. pertussis в круглодонных полистироловых 96-луночных планшетах в присутствии ПКС оценивали окрашиванием 0,1% раствором генциан-фиолетового. За титр ПКС принимали наибольшее ее разведение, подавляющее рост биопленочных культур.
Результаты. Титры ПКС, полностью подавлявшие формирование биопленок исследованными штаммами, варьировали от 1 : 1000 до 1 : 20 000. Вакцинный штамм № 475а (серовар 1.2.3) отличался наиболее высокой чувствительностью к ПКС, титр которой составлял 1 : 20 000. Вакцинный штамм № 305 (серовар 1.2.0) и штаммы, выделенные от больных коклюшем в 2001-2010 гг: № 287 (серовар 1.0.3), № 178 (серовар 1.2.0), № 317 (серовар 1.2.3), были чувствительны к ПКС в титрах 1 : 1000-1 : 2000. Вакцинный штамм № 703 (серовар 1.0.3) был устойчив ко всем исследованным разведениям сыворотки. При посеве супернатантов из лунок с биопленками на плотную питательную среду отмечен рост типичных для B. pertussis колоний. Аналогичные результаты получены при посеве супернатантов культур из лунок с отсутствием биопленок.
Заключение. Приведенные данные свидетельствуют о гетерогенности штаммов B. pertussis по чувствительности к ПКС. Рост типичных для B. pertussis колоний при посеве надосадочной жидкости культур на плотную питательную среду, при отсутствии биопленок в планшетах, свидетельствует о подавлении биопленкообразования ингибированием адгезии микробных клеток на субстрате, а не за счет бактерицидного действия сыворотки.
 413-417
413-417


Колонизационная активность клинических изолятов дрожжевых грибов рода Candida и их антибиотикочувствительность
Аннотация
Введение. Развитие микозов связывают с иммунокомпрометацией макроорганизма. Задачей исследования было изучение колонизационной активности и резистентности дрожжевых грибов рода Candida, выделенных из клинического материала в 2014 и 2019 гг. в Москве.
Материалы и методы. Диско-диффузным методом определяли антибиотикочувствительность 75 штаммов дрожжевых грибов следующих видов: C. albicans, C. parapsilosis, C. glabrata, C. krusei (Pichia kudriavzevii), C. intermedia, C. tropicalis, C. lusitaniae (Clavispora lusitaniae), C. guilliermondii (Meyerozyma guilliermondii). В 2014 г. выделены 34 штамма у людей с гиперчувствительностью в анамнезе (27 — с кожных покровов, 7 — со слизистой ротовой полости), в 2019 г выделили 41 штамм со слизистой влагалища людей с онкологическими заболеваниями. Использовали диски с флуконазолом (40 мкг), нистатином (80 мкг), клотримазолом (10 мкг), итраконазолом (10 мкг), амфотерицином В (40 мкг).
Результаты. В 2014 г. колонизационная активность убывала в ряду: C. albicans (23,53%), C. tropicalis (20,59%), C. guilliermondii (20,59%), C. parapsilosis (17,65%), C. glabrata (17,65%); в 2019 г. — C. parapsilosis (21,95%), C. albicans (17,07%), C. tropicalis (12,19%), C. guilliermondii (12,19%), C. krusei (9,76%), C. glabrata (9,76%), C. lusitaniae (9,76%), C. intermedia (7,32%). Выделенные в 2014 г. грибы обладали чувствительностью ко всем антимикотикам, за исключением 16,67% штаммов C. glabrata (флуконазол) и 14,28% штаммов C. tropicalis (нистатин). Выделенные в 2019 г. 11,11% C. parapsilosis и 40% C. tropicalis были резистентны ко всем антимикотикам; 71,43% C. albicans, 50% C. glabrata, 20% C. guilliermondii — к флуконазолу; 28,57% C. albicans — к нистатину, клотримазолу, итраконазолу, амфотерицину В; 25% C. glabrata — к амфотерицину В; C. krusei — к клотримазолу (100%), флуконазолу и нистатину (50%), итраконазолу и амфотерицину В (25%); C. lusitaniae — к флуконазолу и нистатину (100%), клотримазолу и амфотерицину В (75%), итраконазолу (50%).
Заключение. В течение 5 лет в Московском регионе расширился спектр выявляемых видов грибов за счет C. krusei, C. lusitaniae и C. intermedia (26,86% кандидозов в 2019 г). При этом дрожжевые грибы, выделенные в 2019 г, отличаются высоким количеством резистентных штаммов по сравнению с грибами, выделенными в 2014 г.
 418-423
418-423


Изучение in vitro влияния ДНК пробиотического штамма Bifidobacterium bifidum Bifidobacterium bifidum на количественный уровень и колонизационные свойства кишечных микросимбионтов
Аннотация
Цель — оценка invitro влияния ДНК, выделенной из пробиотического штамма Bifidobacteriumbifidum 791, на количественный уровень и адгезивные свойства фекальных изолятов бифидобактерий и условно-патогенных микроорганизмов разных видов.
Материалы и методы. ДНК выделяли из пробиотического штамма B. bifidum 791. Биомассу бифидобактерий отмывали от питательной среды. Взвесь бактерий в буферном растворе трижды подвергали ультразвуковой обработке с частотой 40 кГц в течение 30 мин с последующим центрифугированием. Супернатанты объединяли и очищали хроматографически на Сефарозе CL-4B. В качестве тест-культур использовали B. breve, B. bifidum, B. infantis, Staphylococcusaureus, Escherichiacolilac-, Enterococcusfaecalis, Candidaalbicans, изолированные из кишечника взрослых относительно здоровых людей.
Результаты. Раствор нуклеиновой кислоты концентрацией 3,54 мкг/мл не влиял на количественный уровень бифидобактерий (p = 0,61). Содержание ДНК в растворе 14,15-21,23 мкг/мл способствовало увеличению титров B. bifidum и B. breve на 2 lg КОЕ/мл по сравнению с контролем (p = 0,01), но не влияло на титры S. aureus, E. colilac-, E. faecalis, C. albicans (p = 0,73). Раствор ДНК повышал аутоагрегацию бифидобактерий в 1,5-2,0 раза. Способность к аутоагрегации под влиянием бифидобактериальной ДНК у S. aureus, E. faecalis, C. albicans не изменялась, у E. colilacувеличивалась в 2,3 раза (p = 0,05).
Заключение. Раствор ДНК пробиотического штамма B. bifidum 791 концентрацией 14,15-21,23 мкг/мл стимулирует размножение и аутоагрегацию B. breve, B. bifidum фекального происхождения.
 424-430
424-430


НАУКА И ПРАКТИКА
Причины и последствия несвоевременной вакцинации против коклюшной инфекции в Российской Федерации
Аннотация
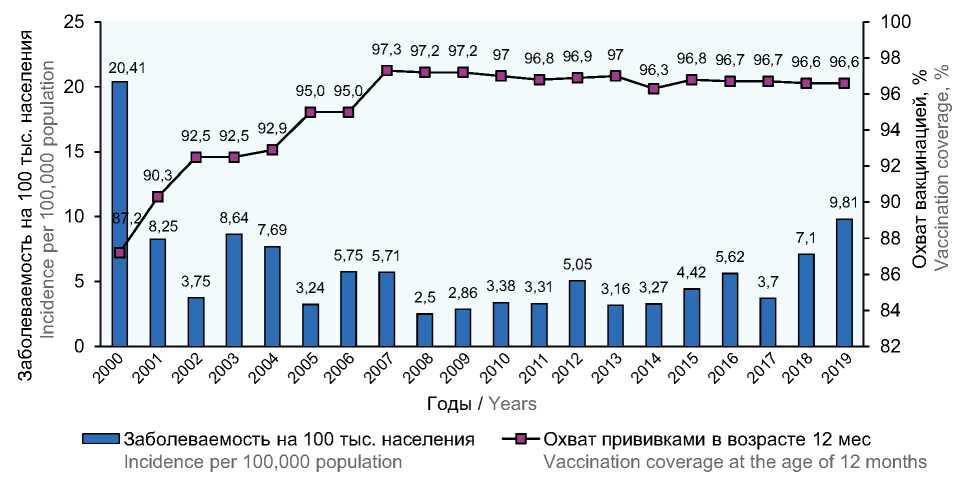
Введение. Одной из причин роста заболевания коклюшем в Российской Федерации при повсеместном охвате профилактическими прививками более 95% населения является большое количество необоснованных медицинских отводов и отказов родителей и, как следствие, несвоевременное проведение профилактических прививок против коклюшной инфекции.
Материалы и методы. Проанализировано 5101 экстренное извещение о подозрении на заболевание коклюшем у детей до 17 лет в Москве в 2012-2017 гг и 300 историй развития детей в возрасте до 14 лет в двух поликлиниках. Проведено исследование «случай-контроль» для оценки связи между заболеванием коклюшем и нарушениями в схеме иммунизации.
Результаты. Выявлено, что уровень своевременного проведения иммунизации против коклюша не превышал 5%. Среди причин несвоевременной вакцинации превалируют медицинские отводы (20%) и отказы родителей (45%). В структуре медицинских отводов основными причинами являются перинатальная энцефалопатия, врожденные пороки сердца, дисбактериоз кишечника, аллергические заболевания, анемия и некоторые хронические заболевания.
Обсуждение. Основным принципом для формирования полноценного защитного иммунитета от коклюшной инфекции является введение обязательного полного первичного курса вакцинации от коклюша с завершением 3 прививок в возрасте 10-12 мес и обязательный контроль за своевременным получением бустерной дозы не позже достижения ребенком 2 лет. Кроме того, необходимо введение дополнительных бустерных доз вакцины от коклюша в возрасте 6-7 и 12-14 лет, вакцинации взрослых каждые 10 лет. Целесообразно рассмотреть возможность введения вакцинации будущих матерей в каждую беременность на сроке 27-36 нед, вакцинации медицинского персонала и сотрудников, предоставляющих услуги по уходу за детьми.
 492-502
492-502


ОБЗОРЫ
SARS, снова SARS и MERS. Обзор животных моделей респираторных синдромов человека, вызываемых коронавирусными инфекциями
Аннотация
Крупные вспышки респираторных синдромов человека, вызываемых коронавирусными инфекциями, с начала ХХI в. стали причиной гибели более миллиона человек на планете. Несмотря на то что первая волна коронавирусной инфекции случилась еще в 2002 г, до сегодняшнего дня не существует ни од¬ной адекватной животной модели, одновременно удовлетворяющей потребности научного сообщества в воспроизведении патогенеза, клинических проявлений, иммуногенности, разработке и испытании средств специфической профилактики и терапии тяжелого острого респираторного синдрома, ближневосточного респираторного синдрома и коронавирусного заболевания 2019 г. (COVID-19).
Цель работы — представить актуальную информацию по известным животным моделям респираторных синдромов человека, вызываемых коронавирусными инфекциями, и акцентировать внимание читателя на их адекватности, заключающейся в максимально точной имитации клинических признаков и патоморфологических изменений.
 431-444
431-444


Состояние популяционного иммунитета к кори в России: систематический обзор и метаанализ эпидемиологических исследований
Аннотация
Введение. Комплексная оценка состояния популяционного иммунитета населения России к кори затруднена, т.к. отечественные работы по указанной тематике, как правило, ограничены изучением серопрева-лентности в отдельных группах разной численности. Систематический обзор и последующий метаанализ результатов работ разных авторов позволяют увеличить общий объем наблюдений и статистическую значимость исследований, что повышает достоверность выводов.
Цель работы — оценка состояния популяционного иммунитета населения России к кори на основании анализа результатов опубликованных научных работ отечественных авторов.
Материалы и методы. Проведен систематический обзор и метаанализ результатов 13 отечественных научных работ (обследовано 15 353 лица в возрасте от рождения до 79 лет), опубликованных в период с 2011 по 2020 г. и посвященных оценке состояния популяционного иммунитета к кори у населения разных регионов России.
Результаты. Установлено, что при проведении исследований основным подходом к оценке популяционного иммунитета является обследование взрослых лиц, в том числе медицинских работников, без учета прививочного анамнеза. Доля серонегативных среди лиц молодого возраста (18-30 лет) — 27,3% (95% ДИ 25,7-27,3%) и детей до 17 лет — 38,3% (95% ДИ 35,8-40,8%), родившихся после введения двукратного ре¬жима вакцинации в Национальный календарь профилактических прививок, была больше, чем в старших возрастных группах — 19,8% (95% ДИ 17,8-21,8%). Уровень коллективного иммунитета у медицинских работников как декретированного контингента — 84,5% (95% ДИ 83,7-85,3%) — оказался выше, чем среди условно здорового населения — 75,4% (95% ДИ 74,1-76,6%), что связано с более жесткими требованиями к проведению вакцинации.
Заключение. Наличие значительной доли серонегативных лиц среди детей и молодых взрослых до 30 лет в пределах, показанных в работе, является фактором риска распространения вируса кори среди населения и может быть следствием недостаточного охвата вакцинацией.
 445-457
445-457


Роль микробиоты в регуляции гомеостаза организма человека при инфекции
Аннотация
В обзоре рассмотрены регуляторные возможности микробиоты человека для сохранения его здоровья. Проблема не нова, но она расширилась с включением новых «находок» со времен И.И. Мечникова — убежденного сторонника полезной (защитной) функции нормофлоры.
Изучение интеграции метаболизма человека и населяющих его микробов выявило участие микробных метаболитов — сигнальных молекул — в обеспечении гомеостаза хозяина. Особое внимание уделяется продуктам метаболизма — ароматическим аминокислотам как регуляторам физиологических функций человека и микробов. Сигнальные молекулы регулируют микробный «кворум», иммунную систему (ее клеточные и гуморальные звенья). Не обойдены вниманием опиаты, гормональные пептиды, в частности, натрийуретический гормон, гипоталамические нонапептиды (окситоцин и вазопрессин), оказывающие как прямое антимикробное, так и опосредованное действие в организме хозяина.
Интерес исследователи проявляют и к продуктам жировой ткани — адипокинам, в частности, лептину, который оказался многоцелевым регулятором, проявляя при этом провоспалительный характер.
К разряду сигнальных молекул отнесены и цитокины, взаимодействующие с грампозитивными бактериями, что активно обсуждается в литературе.
При оценке представленного материала на различных моделях инфекций просматривается общая зако-номерность: в условиях симбиоза формируется единая регуляторная среда, в которой отмечается много-образие связей от непосредственных (прямых) взаимодействий (разрушение сигнальных молекул, индукция физиологических функций за счет наличия сходных рецепторов к лигандам и, наконец, модификация сигнальных молекул — расширение спектра действия) до косвенных воздействий, опосредованных активацией и регуляцией системы иммунитета через цитокиновую сеть и систему адипокинов. Вероятно, сочетание этого многообразия механизмов интеграции в единой регуляторной среде (микроорганизм-хозяин) и приводит к формированию гомеостаза, те. динамическому равновесию сигнальных систем микробиоты и человека в условиях ассоциативного симбиоза, где инфекция — его модельная система.
В эту концепцию хорошо вписывается разработанный нами метод межмикробного распознавания «свойчужой» в паре доминант-ассоциант и описанный треугольник: микробиота-гипоталамо-гипофизарная нейросекреция-окситоцин, органично составляющий «кишечно-мозговую ось».
 458-467
458-467


Нейтрофильные внеклеточные ловушки в борьбе с биопленкообразующими микроорганизмами: охотники или добыча?
Аннотация
В обзоре представлены современные данные о взаимоотношениях нейтрофильных внеклеточных ловушек (НВЛ) и биопленкообразующих микроорганизмов P aeruginosa, S. aureus, Candida spp., полученные в исследованиях in vitro и in vivo. До 80% микробных инфекций человека связаны с биопленкообразующими микроорганизмами. Формирование высокоспециализированных сообществ в виде биопленок является одной из основных стратегий выживания бактерий и грибов, значимо повышая их толерантность к действию агрессивных и стрессовых внешних условий, химиотерапевтических препаратов, факторов иммунной системы, способствуя их персистенции и хронизации инфекционного процесса. Образование НВЛ в процессе нетоза является одним из биологических механизмов, используемых нейтрофилами в защите от патогенов. Хемоаттрактанты биопленочного происхождения, а также выделяемые эпителиальными и иммунокомпетентными клетками, привлекают и активируют мигрирующие нейтрофилы. Однако учитывая, что в биопленках бактерии образуют достаточно крупные клеточные кластеры и агрегаты, процесс фагоцитоза порой оказывается затруднен или невозможен. В этих условиях логично предположить, что значимость НВЛ в антибиопленочном иммунитете увеличивается. Однако за счет компонентов внеклеточного биопленочного матрикса (например, экзополисахарид Psl P aeruginosa), молекул системы quorum sensing (например, quorum sensing-система LasR P. aeruginosa), ферментов (например, LasA-протеаза и LasB-эластаза P aeruginosa), токсинов (например, лейкоцидин Пантона-Валентайна и Y-гемолизин AB S. aureus) и, вероятно, других, пока не изученных, факторов микроорганизмы в биопленках способны влиять на сигнальные системы, задействованные в нетозе, на интенсивность формирования НВЛ, механизмы секвестрации и киллинга в них, порой подчиняя и используя компоненты НВЛ для собственных целей.
 468-481
468-481


Атипичность штаммов Vibrio cholerae О1 по признаку агглютинабельности
Аннотация
В обзоре проанализированы данные литературы о фенотипической изменчивости холерных вибрионов О1 серогруппы. У возбудителя холеры выделяют три типа полисахаридных структур: липополисахарид, или О-антиген, капсульный полисахарид и экзополисахарид. Ругозная форма штаммов Vibriocholerae способна синтезировать экзополисахарид, образовывать морщинистые колонии, которые могут агглютинироваться холерными сыворотками в различных сочетаниях. Экзополисахарид обладает повышенной устойчивостью к противомикробным препаратам. На специфичности липополисахарида основана серологическая классификация, в том числе холерных вибрионов, при этом только холерные вибрионы О1 и О139 серогрупп вызывают эпидемии холеры, хотя известны штаммы non-О1/non-О139 серогрупп, обладающие основными факторами вирулентности. При переходе из S-формы в R-форму липополисахарид утрачивает О-полисахарид, а центральная область начинает выполнять функцию соматического антигена, проявляя R-специфичность. В основе серологических различий штаммов холерных вибрионов лежит изменение в регуляции или структурной организации генов, кодирующих биосинтез О-антигена (rfb). В 1988-2019 гг. на территории бывшего СССР и субъектов России из объектов окружающей среды выделено 168 штаммов холерных вибрионов, атипичных по признаку агглютинабельности и при выделении отнесенных к R-варианту. Генетическая организация этих штаммов полностью не изучена. Проведено определение эволюционных взаимоотношений атипичных штаммов холерных вибрионов, выделенных из объектов окружающей среды в Сибири и на Дальнем Востоке, на основании сравнительного анализа генов «домашнего хозяйства». Проведенный анализ результатов фундаментальных и прикладных исследований свидетельствует о том, что проблема изменчивости по признаку агглютинабельности штаммов V. cholerae, выделенных от людей и из объектов окружающей среды, продолжает оставаться актуальной на современном этапе развития седьмой пандемии холеры. Атипичность штаммов холерных вибрионов О1 по данному признаку рассматривается в аспектах экологических условий их существования и молекулярно-биологической детерминации фенотипических проявлений.
 482-491
482-491


РЕЦЕНЗИИ
 503-504
503-504