Генотипирование боррелий, риккетсий и анаплазм в клещах Ixodes ricinus и Dermacentor reticulatus в Калининградской области
- Авторы: Карташов М.Ю.1,2, Волчев Е.Г.3, Кривошеина Е.И.1, Свирин К.А.1, Терновой В.А.1, Локтев В.Б.1,2,4
-
Учреждения:
- Государственный научный центр вирусологии и биотехнологии «Вектор»
- Новосибирский национальный исследовательский государственный университет
- Балтийский федеральный университет им. И. Канта
- Институт цитологии и генетики СО РАН
- Выпуск: Том 101, № 2 (2024)
- Страницы: 227-236
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://microbiol.crie.ru/jour/article/view/18542
- DOI: https://doi.org/10.36233/0372-9311-503
- EDN: https://elibrary.ru/pebbmx
- ID: 18542
Цитировать
Аннотация
Актуальность. Возбудители клещевых инфекций бактериальной и протозойной природы представляют существенную проблему для общественного здравоохранения.
Цель исследования состояла в детекции и генотипировании боррелий, риккетсий и анаплазм в клещах Ixodes ricinus и Dermacentor reticulatus, собранных на территории Калининградской области в 2021–2022 гг.
Материалы и методы. В исследование были включены 1665 клещей: I. ricinus (n = 862) и D. reticulatus (n = 803), собранных в 33 биотопах Калининградской области. Детекцию генетического материала клещевых патогенов проводили в индивидуальных клещах методом ПЦР с последующим секвенированием и филогенетическим анализом специфических последовательностей ДНК.
Результаты. Уровень инфицированности клещей I. ricinus боррелиями составил 15,5%, причём генотипирование по последовательности гена p66 показало наличие ДНК боррелий четырех видов: Borrelia afzelii, B. garinii, B. valaisiana и B. lusitaniae. В клещах D. reticulatus ДНК боррелий не выявлено. Генетический материал Rickettsia spp. был обнаружен в обоих видах клещей, причём уровень инфицированности клещей I. ricinus составил 2,6%, а D. reticulatus — 21,2%. В клещах I. ricinus обнаружены риккетсии R. helvetica, а в луговых клещах — R. raoultii при проведении их генотипирования по гену gltA. ДНК Anaplasma phagocytophilum были обнаружены как в клещах I. ricinus, так и в клещах D. reticulatus. Выявлены также случаи коинфицирования индивидуального клеща несколькими клещевыми патогенами.
Заключение. В клещах I. ricinus и D. reticulatus, собранных на территории Калининградской области, обнаружены 6 видов возбудителей клещевых инфекций бактериальной и протозойной природы, причём R. helvetica, R. raoultii и A. phagocytophilum были выявлены впервые.
Полный текст
Введение
Клещи могут быть заражены патогенами вирусной, бактериальной и протозойной природы [1–3]. Помимо достаточно хорошо изученных патогенов, к которым можно отнести вирус клещевого энцефалита и возбудителей иксодового боррелиоза, в клещах могут присутствовать другие микроорганизмы, вызывающие заболевания человека, в том числе и в европейских странах [2, 4–6]. Инфекции, переносимые клещами, являются распространённой группой зооантропонозных заболеваний в России [7, 8]. Структура и характеристика клещевых инфекций, включая генотипирование их возбудителей, на территории европейской части России изучены недостаточно [9]. В последние годы случаи клещевых инфекций человека ассоциируются с клещами Ixodes persulcatus (Schulze, 1930), I. pavlovskyi (Pomerantzev, 1946), Dermacentor reticulatus (Fabric, 1794), D. marginatus (Sulzer, 1776), D. nuttali (Olenev, 1928) в сибирских и дальневосточных регионах России [8, 10]. В европейских части России широко распространены клещи I. ricinus (Linnaeus, 1758), которые доминируют в западных регионах страны. Интересно, что появление клещей D. reticulatus отмечается в городских и пригородных биотопах [8, 11]. Так, в Томске их численность возросла более чем в 200 раз для городских биотопов, а инфицированность клещей D. reticulatus составила приблизительно 44–48% для Rickettsia spp., 0,7–0,9% для вируса клещевого энцефалита и 0,6% для Anaplasma phagocytophilum.
Ранее в I. ricinus в Ленинградской и Калининградской областях методом ПЦР были предположительно обнаружены 4 вида боррелий при уровне инфицированности 11,5% [12]. Несколько позднее в парковых зонах Санкт-Петербурга на побережье Балтийского моря были обнаружены таёжные клещи (I. persulcatus) с уровнем инфицированности 9,3% боррелиями, генотипированными как B. afzelii и B. garinii [13]. В Финляндии уровень инфицированности I. ricinus и I. persulcatus различными клещевыми патогенами достигал 30% при значительном доминировании Borrelia burgdorferi sensu lato [14]. При этом клещи I. ricinus были существенно чаще инфицированы и коинфицированы различными бактериальными и протозойными патогенами.
В Калининградской области в 2022 г. из-за укусов клещей за медицинской помощью обратились 5379 человек1. Ежегодно диагностируются только случаи вирусного клещевого энцефалита и иксодового клещевого боррелиоза у пациентов, которые традиционно ассоциируются с клещами I. ricinus: в 2022 г. зарегистрировано 3 случая клещевого энцефалита и 49 случаев клещевого боррелиоза. Циркуляция других возбудителей клещевых инфекций и их видовая принадлежность не описаны.
Целью данного исследования являлось обнаружение, изучение видовой принадлежности и генотипирование боррелий, риккетсий и анаплазм, выявляемых в иксодовых клещах, собранных в различных биотопах Калининградской области.
Материалы и методы
Сбор клещей производили с растительности методом «на флаг» в различных биотопах Калининградской области в 2021–2022 гг. Географические координаты биотопов и количество собранных в биотопах клещей представлены в Приложении на сайте журнала. Видовая идентификация клещей осуществлялась морфологическим методом [15].
Выделение нуклеиновых кислот
Клещи были дважды обработаны 70% этанолом для инактивации инфекционных агентов и промыты фосфатно-солевым буфером. Гомогенизацию полученных образцов осуществляли с использованием лабораторного гомогенизатора «TissueLyserLT» («Qiagen») в 300 мкл стерильного физиологического раствора. Выделение проводили из 100 мкл гомогената с использованием набора реагентов «АмплиПрайм РИБО-преп» («НекстБио») согласно инструкции производителя.
Проведение ПЦР
Скрининг полученных образцов на наличие генетических маркеров изучаемых патогенов осуществляли с помощью ПЦР, используя специфические праймеры (таблица), на термоциклере «Т-1000» («Bio-Rad») в 25 мкл реакционной смеси следующего состава: 10 мM Трис-HСl (pH 9,0), 50 мM KCl, 0,1% тритон Х-100, 2 мM MgCl2, 0,2 мM каждого dNTP, по 0,25 мM каждого праймера, 1,5 ед. активности HS-Taq-полимеразы («Евроген») и 1–100 нг ДНК-матрицы. При постановке ПЦР использовали следующие температурные режимы: предварительная активация полимеразы — 95ºС в течение 5 мин; 38 циклов: 95ºС — 20 с, Тотжига — 20 с, 72ºС — 1 мин; финальная элонгация при 72ºС — 4 мин.
Праймеры, использованные для амплификации фрагментов генов боррелий, риккетсий и анаплазм из иксодовых клещей
Primers using for isolation gene fragments of Borrelia, Rickettsia and Anaplasma from ixodes ticks
Праймер Primer | Структура праймера (5′→3′) Primer sequence (5′→3′) | Температура Temperature, ºС | Размер, п.н. Size, bp | Источник Reference |
Borr2rF | CGAATTAGGCAAAGACGATCC | 56 | 548 | [8] |
Borr2rR | TTTCCATAAGCTCCTGATAAGCCA | |||
CS409d | CCTATGGCTATTATGCTTGC | 56 | 769 | [16] |
RP1258n | ATTGCAAAAAGTACAGTGAACA | |||
MSP2-3f | CCAGCGTTTAGCAAGATAAGAG | 55 | 334 | [17] |
MSP2-3r | GCCCAGTAACAACATCATAAGC |
Детекцию полученных ампликонов проводили методом гель-электрофореза в 2% агарозном геле в трис-ацетатном буфере, содержащем 0,1% бромида этидия. Продукты амплификации из агарозного геля очищали с использованием набора на основе микроколонок («Биосилика»).
Секвенирование и анализ нуклеотидных последовательностей
Секвенирование по Сэнгеру проводили с использованием набора «BigDye Terminatorv.3.1 Cycle Sequencing Kit» («Applied Biosystems»). Определение нуклеотидных последовательностей осуществляли на основе капиллярного электрофореза с помощью автоматического секвенатора «3130xl Genetic Analyzer» («Applied Biosystems»). Анализ полученных нуклеотидных последовательностей проводили с использованием программы «UniproUGENE v. 1.46». Полученные нуклеотидные последовательности сравнивали с ранее опубликованными последовательностями в GenBank при помощи поискового приложения BLAST. Выравнивание нуклеотидных последовательностей осуществляли с помощью алгоритма MUSCLE в программе «MEGA Х». Филогенетический анализ нуклеотидных последовательностей проводили методом максимального правдоподобия с использованием модели эволюции Tamura-Nei с целью анализа генетических взаимоотношений/кластеризации нуклеотидных последовательностей. Показатели статистической надёжности узлов филогенетического дерева рассчитаны с помощью бутстреп-анализа с использованием 1000 случайных реплик.
Депонирование нуклеотидных последовательностей
В базу данных GenBank были депонированы нуклеотидные последовательности: фрагменты гена msp2 A. phagocytophilum (OR488786–OR488799); гена p66 борреллий: B. afzelii (OR488840–OR488890), B. garinii (OR488891–OR488929), B. valaisiana (OR488930–OR488948), B. lusitaniae (OR488949–OR488967); фрагменты гена gltA риккетсий: R. helvetica (OR496610–OR496611) и R. conorii subsp. raoultii, далее, как базионим R. raoultii (OR496612–OR496613). Исследования проводили с соблюдением правил биобезопасности, регламентированных в МУ 1.3.2569–09, СП 1.3.3118-13, СП 3.1.3310-15.
Результаты
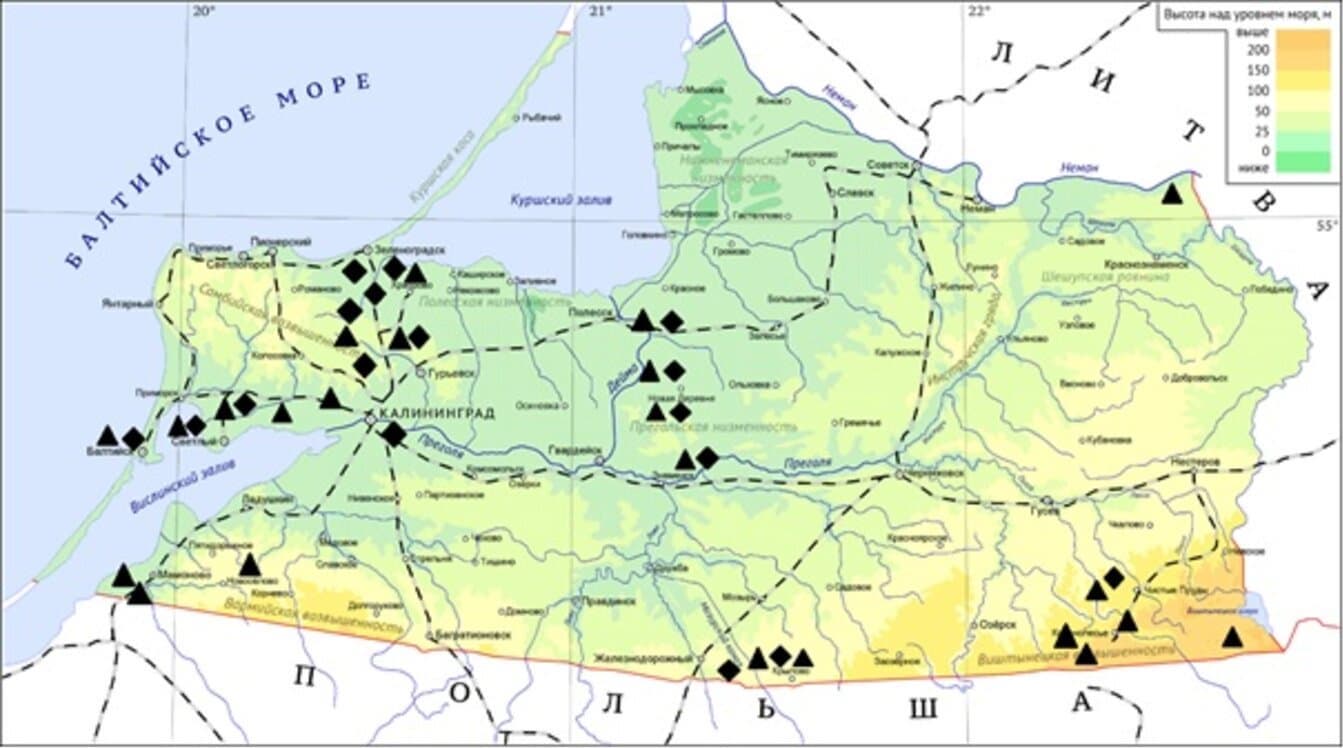
Проведён сбор и анализ 1665 индивидуальных образцов нимф и имаго иксодовых клещей видов I. ricinus (n = 862) и D. reticulatus (n = 803), собранных на территории 33 городских, пригородных и характерных природных биотопов Калининградской области (рис. 1). Исследованные биотопы подразделялись по видам клещей, собранных в них, следующим образом: 11 биотопов, в которых были отловлены только клещи I. ricinus, 9 биотопов — клещи D. reticulatus и 13 биотопов с 2 видами клещей. Совершенно необычно, что фактически половина всех собранных клещей была отнесена к луговому клещу, который был обнаружен в 2/3 исследованных биотопов и абсолютно доминировал в 9 из них.
Рис. 1. Места расположения биотопов в Калининградской области, в которых проводился сбор иксодовых клещей в 2021–2022 гг.
Fig. 1. Locations of biotopes in the Kaliningrad region, where ixodid ticks were collected in 2021–2022.
Уровень инфицированности I. ricinus боррелиями составил 15,5% (128/862; 95% ДИ 13,2–18,1%). При определении нуклеотидной последовательности фрагмента гена р66 длиной около 560 п.н. среди 128 образцов были выявлены боррелии четырех видов из комплекса B. burgdorferi s.l.: у 51 клеща выявлена ДНК B. afzelii (39,9%; 95% ДИ 31,8–48,5%), у 39 — B. garinii (30,5%; 95% ДИ 23,2–38,5%), у 19 — B. valaisiana (14,8%; 95% ДИ 9,7–22,0%), у 19 — B. lusitaniae (14,8%; 95% ДИ 9,7–22,0%). Среди изучаемых образцов клещей вида D. reticulatus генетического материала боррелий не выявлено. Филогенетический анализ показал, что боррелии, выявленные в клещах I. ricinus на территории Калининградской области, кластеризуются с прототипными изолятами, выделенными прежде всего в европейских странах (рис. 2). Анализ последовательности секвенированного фрагмента гена р66 B. afzelii выявил 6 аллелей этого гена, для изолятов B. garinii обнаружено 8 аллельных вариантов, отличающихся друг от друга по 1–14 нуклеотидным заменам, а изоляты B. valaisiana и B. lusitaniae имели 2 и 4 замены.
Рис. 2. Дендрограмма, построенная по нуклеотидной последовательности фрагмента гена p66 для выявленных изолятов боррелий. Последовательности, отмеченные чёрными квадратами, получены из клеща I. ricinus.
Fig. 2. Dendrogram of nucleotide sequences of the p66 gene fragment for detected borrelia isolates. Black squares — sequences derived from I. ricinus tick.
Уровень инфицированности риккетсиями клещей составил 11,5% (191/1665; 95% ДИ 10,2–13,1%). Среди клещей вида I. ricinus ДНК риккетсий выявлена в 22 образцах, уровень инфицированности — 2,6% (22/862; 95% ДИ 1,7–3,8%). Все выявленные изоляты риккетсий из клещей I. ricinus по фрагменту гена цитратсинтазы (gltA) были отнесены к R. helvetica. При анализе нуклеотидных последовательностей гена gltA идентифицированы два основных геноварианта R. helvetica, циркулирующие в Калининградской области. Они отличаются друг от друга 2 синонимичными нуклеотидными заменами (уровень гомологии между геновариантами составляет 99,8%). Один из геновариантов соответствует описанным ранее вариантам R. helvetica, обнаруженным в Республике Коми и Омской области [9, 18], другой геновариант отличается от известных последовательностей.
В 21,1% клещей D. reticulatus обнаружена ДНК риккетсий (169/803; 95% ДИ 18,4–24,0%), которая была генотипирована как R. raoultii. Филогенетический анализ R. raoultii показал существование двух вариантов, отличающихся одной синонимичной заменой (рис. 3). В целом эти геноварианты соответствуют широкому кругу изолятов R. raoultii, циркулирующих в Европе, России и Китае [19, 20].
Рис. 3. Дендрограмма нуклеотидных последовательностей фрагмента гена gltA выявленных изолятов риккетсий. Чёрными треугольниками отмечены последовательности, полученные из клеща D. reticulatus, чёрными квадратами — из клеща I. ricinus.
Fig. 3. Dendrogram of nucleotide sequences of the gltA gene fragment for identified Rickettsia isolates. Black triangles — sequences derived from D. reticulatus tick; black squares — sequences derived from I. ricinus tick.
Методом ПЦР ДНК A. phagocytophilum была обнаружена в 12 исследованных образцах клещей вида I. ricinus (1,4%; 95% ДИ 0,8–2,5%) и в 2 образцах клещей вида D. reticulatus (0,2%; 95% ДИ 0,1–0,9%). У выявленных изолятов A. phagocytophilum проведено определение нуклеотидных последовательностей фрагмента гена msp2 длиной примерно 340 п.н. с последующим филогенетическим анализом (рис. 4). На территории Калининградской области обнаружены 3 геноварианта A. phagocytophilum с уровнем гомологии порядка 98,6%, тождественные либо наиболее близкие изолятам A. phagocytophilum, циркулирующим в Норвегии и Польше.
Рис. 4. Дендрограмма нуклеотидных последовательностей фрагмента гена msp2 выявленных изолятов A. phagocytophilum. Чёрными треугольниками отмечены последовательности, полученные из клеща D. reticulatus, чёрными квадратами — из клеща I. ricinus.
Fig. 4. Dendrogram of nucleotide sequences of the msp2 gene fragment for identified A. phagocytophilum isolates. Black triangles — sequences derived from D. reticulatus ticks; black squares — sequence derived from I. ricinus ticks
В 2 пробах клещей содержался одновременно генетический материал B. afzelii и R. helvetica, в 1 пробе клещей — ДНК B. valaisiana и A. phagocytophilum.
Обсуждение
Результаты регулярных многолетних полевых наблюдений показывают, что основные рекреационные ландшафты Калининградской области, включая ландшафты побережья Балтийского моря, имеют сформированные популяции иксодовых клещей. При этом активность иксодид в зонах с выраженной антропогенной нагрузкой существенно выше, чем в аналогичных ландшафтах с незначительной антропогенной нагрузкой. Так, в последние годы за медицинской помощью по поводу укусов клещей обращаются 4194–7300 человек. Ежегодно диагностируется 2–16 случаев вирусного клещевого энцефалита и 35–132 случаев иксодового клещевого боррелиоза. Это многократно повышает риски контакта человека с иксодовыми клещами, что может привести к заражению человека возбудителями различных клещевых инфекций.
Клещевые боррелиозы занимают важное место в структуре инфекционной патологии в Калининградской области. В клещах Калининградской области нами были обнаружены и генотипированы B. afzelii, B. garinii и B. lusitaniae, которые считаются патогенными для человека, и B. valaisiana, патогенность которой обсуждается [21]. Уровень инфицированности (15,5%) соотносится с ранее проведёнными исследованиями на территории Ленинградской и Калининградской областей [12]. B. afzelii и B. garinii — наиболее распространённые возбудители клещевого боррелиоза у человека и наиболее часто обнаруживаются в клещах I. ricinus. Впервые на территории Калининградской области показана циркуляция B. lusitaniae. Следует отметить, что B. lusitaniae в основном распространена в странах Средиземноморского региона, таких как Португалия, Марокко и Тунис. В более северных широтах данный патоген обнаруживался в Австрии, Словакии, Украине и Латвии [22].
В клещах D. reticulatus не удалось выявить генетических маркеров боррелиоза, хотя была исследована весьма представительная выборка клещей этого вида. Ранее аналогичная ситуация была зарегистрирована в Томске, где удалось индивидуально исследовать 315 клещей этого вида, собранных в городских биотопах [11]. В Томских городских биотопах обнаружено более чем 200-кратное увеличение численности клещей D. reticulatus фактически в течение 2015 г. Именно взрывное нарастание численности D. reticulatus позволило собрать в 2016–2017 гг. значительное количество этих клещей и оценить их роль в передаче клещевых инфекций в Томске.
Риккетсии, переносимые иксодовыми клещами, являются инфекционными агентами, способными вызывать заболевание человека. На территории Калининградской области нам впервые удалось установить факт циркуляции двух видов риккетсий из группы клещевой пятнистой лихорадки: R. helvetica и R. raoultii. Зарегистрированный уровень инфицированности R. helvetica клещей I. ricinus составил 2,6%. В других странах Балтийского региона он колеблется от 5 до 10% [23]. Однако клещи D. reticulatus были инфицированы R. raoultii в 21,2% случаев. При этом в Литве и Латвии аналогичный показатель достигает 38%, в Германии — 80% [24, 25]. На территории России уровень инфицированности D. reticulatus данным видом риккетсий может варьировать в различных регионах от 21,9% до 45%. ДНК R. helvetica была найдена у клещей I. persulcatus, I. ricinus, I. pavlovskyi и I. trianguliceps в различных регионах северной Евразии [10, 26, 27]. Описаны случаи заболевания человека, при этом у пациентов с риккетсиозом, вызванным R. helvetica, наблюдалась лихорадка, редко появлялась сыпь, описаны случаи перимиокардита и менингита.
R. conorii subsp. raoultii была описана как новый вид риккетсий в 2008 г. после изучения прототипного штамма R. raoultii Kharbarovsk, выделенного в 2005 г. из клеща D. silvarum в Хабаровском крае [28]. В последующих исследованиях R. raoultii была обнаружена у клещей D. reticulatus, D. marginatus и D. nuttalli в ряде регионов азиатской части России (Омская область, Республика Бурятия), в Казахстане, в Китае и Монголии [19, 20]. Риккетсии, генетически близкие R. raoultii, выявлены в клещах Haemaphysalis hystricis в Японии и в клещах H. ornithophila, H. shimoga, H. lagrangei в Таиланде, а также в клещах D. marginatus в Грузии, Турции и в европейских странах [29].
Серологическими методами и путём выявления ДНК в крови больных подтверждена роль R. raoultii наряду с R. slovaca в качестве этиологического агента синдрома TIBOLA, который ассоциируется с клещами рода Dermacentor spp. [30]. У больных развивается астенический синдром, в четверти случаев наблюдается лихорадка (> 38ºC). У большинства пациентов эритема сохраняется до 1–2 мес. В случае локализации укуса клеща в волосистой части головы примерно у трети пациентов развивается стойкое облысение в месте заживления укуса. При этом случаев заболевания риккетсиозами человека в Калининградской области пока не описано.
Впервые выявленный в работе факт наличия генетического материала A. phagocytophilum в клещах I. ricinus и D. reticulatus показывает активную циркуляцию данного возбудителя в Калининградской области. Уровень инфицированности клещей D. reticulatus и I. ricinus (0,2 и 1,4% соответственно) соотносится с аналогичными показателями для таких стран, как Дания, Швеция, Норвегия и Германия, где патоген обнаруживается в 1–5% иксодовых клещей [23]. Филогенетический анализ показывает одновременную циркуляцию не менее 3 геновариантов A. phagocytophilum. Заболевание гранулоцитарным анаплазмозом человека (ГАЧ) впервые описано на Дальнем Востоке России ещё в 2000 г. Позднее подтверждённые случаи заболевания отмечены в Пермской, Новосибирской областях и на Алтае. Клиническое течение ГАЧ очень полиморфно: от лёгких, субклинических форм до крайне тяжёлых, летальных случаев, которые составляют 0,5–1,0% и обычно связаны с развитием вторичных инфекций. Для заболевания характерно появление головных и мышечных болей, развитие лихорадки. Менее чем у половины больных могут наблюдаться тошнота, рвота, анорексия, диарея, боли в брюшной области и суставах, кашель. В большинстве случаев у больных ГАЧ отмечают лейкопению, тромбоцитопению, а также повышенный уровень аминотрансфераз печени и С-реактивного белка в сыворотке крови. Заболевание ГАЧ на территории Калининградской области не зарегистрировано.
Высокий уровень инфицированности иксодовых клещей риккетсиями и анаплазмами в Калининградской области, наличие постоянных контактов населения с клещами позволяет ожидать появление случаев инфицирования людей риккетсиями группы клещевой пятнистой лихорадки и анаплазмами. Диагностика этих заболеваний может быть затруднена из-за несовершенства их лабораторной диагностики. Эти инфекционные агенты не культивируются классическими микробиологическими методами, а генетический материал возбудителей можно обнаружить в клиническом материале от больных в очень узком временнóм диапазоне. Это актуализирует исследования по сероэпидемиологическому мониторингу данных инфекций у населения, проживающего в Калининградской области, для уточнения их распространения в настоящее время.
Заключение
В коллекции клещей I. ricinus и D. reticulatus, собранной в 33 различных биотопах в Калининградской области в 2021–2022 гг., обнаружена ДНК 6 различных видов возбудителей клещевых инфекций бактериальной и протозойной природы. Секвенирование фрагментов геномов этих возбудителей, их филогенетический анализ позволили идентифицировать и генотипировать следующие виды возбудителей клещевых инфекций: B. afzelii, B. garinii, B. valaisiana, B. lusitaniae, R. helvetica, R. raoultii и A. phagocytophilum. При этом R. helvetica, R. raoultii и A. phagocytophilum были выявлены впервые в данном регионе как в клещах I. ricinus, так и в клещах D. reticulatus. Полученные данные подтверждают необходимость постоянного мониторинга циркуляции возбудителей боррелиозов, риккетсиозов и анаплазмоза в природных очагах клещевых инфекций в Калиниградской области, дальнейшего совершенствования методов диагностики и профилактики этих инфекций, включая выявление возможных случаев заболевания человека риккетсиозами и ГАЧ.
1 Государственный доклад «О состоянии санитарно-эпидемиологического благополучия населения в Калининградской области в 2022 году». Калининград; 2023. 238 с. URL: https://39.rospotrebnadzor.ru/sites/default/files/doklad_o_goskontrole_za_2022_kaliningradskaya.pdf
Об авторах
Михаил Юрьевич Карташов
Государственный научный центр вирусологии и биотехнологии «Вектор»; Новосибирский национальный исследовательский государственный университет
Email: valeryloktev@gmail.com
ORCID iD: 0000-0002-7857-6822
к.б.н., с.н.с. отдела молекулярной вирусологии флавивирусов и вирусных гепатитов
Россия, Кольцово; НовосибирскЕвгений Георгиевич Волчев
Балтийский федеральный университет им. И. Канта
Email: valeryloktev@gmail.com
ORCID iD: 0000-0002-7401-3678
аспирант Института живых систем
Россия, КалининградЕкатерина Ильинична Кривошеина
Государственный научный центр вирусологии и биотехнологии «Вектор»
Email: valeryloktev@gmail.com
ORCID iD: 0000-0001-5181-0415
м.н.с. отдела молекулярной вирусологии флавивирусов и вирусных гепатитов
Россия, КольцовоКирилл Андреевич Свирин
Государственный научный центр вирусологии и биотехнологии «Вектор»
Email: valeryloktev@gmail.com
ORCID iD: 0000-0001-9083-1649
м.н.с. отдела молекулярной вирусологии флавивирусов и вирусных гепатитов
Россия, КольцовоВладимир Александрович Терновой
Государственный научный центр вирусологии и биотехнологии «Вектор»
Email: valeryloktev@gmail.com
ORCID iD: 0000-0003-1275-171X
к.б.н., в.н.с., зав. отделом молекулярной вирусологии флавивирусов и вирусных гепатитов
Россия, КольцовоВалерий Борисович Локтев
Государственный научный центр вирусологии и биотехнологии «Вектор»; Новосибирский национальный исследовательский государственный университет; Институт цитологии и генетики СО РАН
Автор, ответственный за переписку.
Email: valeryloktev@gmail.com
ORCID iD: 0000-0002-0229-321X
д.б.н., профессор, г.н.с. отдела молекулярной вирусологии флавивирусов и вирусных гепатитов
Россия, Кольцово; Новосибирск; НовосибирскСписок литературы
- Charrel R.N., Attoui H., Butenko A.M., et al. Tick-borne virus diseases of human interest in Europe. Clin. Microbiol. Infect. 2004;10(12):1040–55. doi: https://doi.org/10.1111/j.1469-0691.2004.01022.x
- Defaye B., Moutailler S., Pasqualini V., Quilichini Y. A systematic review of the distribution of tick-borne pathogens in wild animals and their ticks in the mediterranean Rim between 2000 and 2021. Microorganisms. 2022;10(9):1858. doi: https://doi.org/10.3390/microorganisms10091858
- Ni X.B., Cui X.M., Liu J.Y., et al. Metavirome of 31 tick species provides a compendium of 1,801 RNA virus genomes. Nat. Microbiol. 2023;8(1):162–73. doi: https://doi.org/10.1038/s41564-022-01275-w
- Kiewra D., Krysmann A. Interactions between hard ticks (Ixodidae) and bacterial tick-borne pathogens. Ann. Parasitol. 2023;69(1):7–16. DOI: https://doi.org/0.17420/ap6901.502
- Hansford K.M., Wheeler B.W., Tschirren B., Medlock J.M. Questing Ixodes ricinus ticks and Borrelia spp. in urban green space across Europe: A review. Zoonoses Public Health. 2022;69(3):153–66. DOI: https://doi.org/10.1111/zph.12913
- Moraga-Fernández A., Muñoz-Hernández C., Sánchez-Sánchez M., et al. Exploring the diversity of tick-borne pathogens: The case of bacteria (Anaplasma, Rickettsia, Coxiella and Borrelia) protozoa (Babesia and Theileria) and viruses (Orthonairovirus, tick-borne encephalitis virus and louping ill virus) in the European continent. Vet. Microbiol. 2023;286:109892. doi: https://doi.org/10.1016/j.vetmic.2023.109892
- Alekseev A.N., Dubinina H.V., Jushkova O.V. First report on the coexistence and compatibility of seven tick-borne pathogens in unfed adult Ixodes Persulcatus Schulze (Acarina:Ixodidae). Int. J. Med. Microbiol. 2004;293(Suppl. 37):104–8. doi: https://doi.org/10.1016/s1433-1128(04)80015-9
- Карташов М.Ю., Кривошеина Е.И., Свирин К.А. и др. Генотипирование возбудителей клещевых инфекций и определение видового состава клещей, нападающих на людей в г. Новосибирске и его пригородах. Инфекция и иммунитет. 2022;12(6):1103–12. Kartashov M.Yu., Krivosheina E.I., Svirin K.A., et al. Genotyping of tick-borne pathogens and determination of human attacking tick species in Novosibirsk and its suburbs. Russian Journal of Infection and Immunity. 2022;12(6):1103–12. doi: https://doi.org/10.15789/2220-7619-GOT-1979
- Kartashov M.Yu., Glushkova L.I., Mikryukova T.P., et al. Detection of Rickettsia helvetica and Candidatus R. tarasevichiae DNA in Ixodes persulcatus ticks collected in Northeastern European Russia (Komi Republic). Ticks Tick Borne Dis. 2017;8(4):588–92. doi: https://doi.org/10.1016/j.ttbdis.2017.04.001
- Rar V., Livanova N., Tkachev S., et al. Detection and genetic characterization of a wide range of infectious agents in Ixodes pavlovskyi ticks in Western Siberia, Russia. Parasit. Vectors. 2017;10(1):258. doi: https://doi.org/10.1186/s13071-017-2186-5
- Карташов М.Ю., Микрюкова Т.П., Кривошеина Е.И., и др. Генотипирование возбудителей клещевых инфекций в клещах Dermacentor reticulatus, собранных в городских биотопах г. Томска. Паразитология. 2019;53(5):355–69. Kartashov M.Yu., Mikryukova T.P., Krivosheina E.I., et al. Genotyping of tick-borne infections in Dermacentor reticulatus ticks collected in urban foci of Tomsk. Parazitologiya. 2019;53(5):355–69. doi: https://doi.org/10.1134/S0031184719050016 EDN: https://elibrary.ru/xodhop
- Alekseev A.N., Dubinina H.V., Van De Pol I., Schouls L.M. Identification of Ehrlichia spp. and Borrelia Burgdorferi in ixodes ticks in the Baltic regions of Russia. J. Clin. Microbiol. 2101;39(6):2237–42. doi: https://doi.org/10.1128/jcm.39.6.2237-2242.2001
- Панферова Ю.А., Ваганова А.Н., Фрейлихман О.А., и др. Распространенность генетических маркеров Borrelia burgdorferi sensu lato у кровососущих клещей в парковых зонах Санкт-Петербурга. Инфекция и иммунитет. 2020;10(1): 175–9. Panferova Yu.A., Vaganova A.N., Freilikhman O.A., et al. Prevalence of Borrelia burgdorferi sensu lato genetic markers in blood-sucking ticks in suburban park zones in Saint Petersburg. Russian Journal of Infection and Immunity. 2020;10(1):175–9. doi: https://doi.org/10.15789/2220-7619-POB-806
- Laaksonen M., Klemola T., Feuth E., et al. Tick-Borne pathogens in Finland: comparison of Ixodes ricinus and I. persulcatus in sympatric and parapatric areas. Parasit. Vectors. 2018;11(1):556. doi: https://doi.org/10.1186/s13071-018-3131-y
- Филиппова Н.А. Иксодовые клещи подсемейства Ixodinae. Ленинград;1977. Filippova N.A. Ixodid Ticks Subfamily Ixodinae. Leningrad;1977.
- Roux V., Rydkina E., Eremeeva M., Raoult D. Citrate synthase gene comparison, a new tool for phylogenetic analysis, and its application for the rickettsiae. Int. J. Syst. Bacteriol. 1977;47(2):252–61. doi: https://doi.org/10.1099/00207713-47-2-252
- Levin M.L., Ross D.E. Acquisition of different isolates of Anaplasma phagocytophilum by Ixodes scapularis from a model animal. Vector Borne Zoonotic. Dis. 2004;4(1):53–9. doi: https://doi.org/10.1089/153036604773082997
- Igolkina Y.P., Rar V.A., Yakimenko V.V., et al. Genetic variability of Rickettsia spp. in Ixodes persulcatus/Ixodes trianguliceps sympatric areas from Western Siberia, Russia: identification of a new Candidatus Rickettsia species. Infect. Genet. Evol. 2015;34:88–93. doi: https://doi.org/10.1016/j.meegid.2015.07.015
- Speck S., Derschum H., Damdindorj T., et al. Rickettsia raoultii, the predominant Rickettsia found in Mongolian Dermacentor nuttalli. Ticks Tick Borne Dis. 2012;3(4):227–31. doi: https://doi.org/10.1016/j.ttbdis.2012.04.001
- Wen J., Jiao D., Wang J.H., et al. Rickettsia raoultii, the predominant Rickettsia found in Dermacentor silvarum ticks in China–Russia border areas. Exp. Appl. Acarol. 2014; 63(4):579–85. doi: https://doi.org/10.1007/s10493-014-9792-0
- Strle F., Stanek G. Clinical manifestations and diagnosis of Lyme borreliosis. Curr. Probl. Dermatol. 2009;37:51–110. DOI: https://doi.org/10.1159/000213070
- Norte A.C., Boyer P.H., Castillo-Ramirez S., et al. The population structure of Borrelia lusitaniae is reflected by a population division of its Ixodes vector. Microorganisms. 2021;9(5):933. DOI: https://doi.org/10.3390/microorganisms9050933
- Quarsten H., Henningsson A., Krogfelt K.A., et al. Tick-borne diseases under the radar in the North Sea Region. Ticks Tick Borne Dis. 2023;14(4):102185. doi: https://doi.org/10.1016/j.ttbdis.2023.102185
- Arz C., Król N., Imholt C., et al. Spotted fever group rickettsiae in ticks and small mammals from grassland and forest habitats in Central Germany. Pathogens. 2023;12(7):933. doi: https://doi.org/10.3390/pathogens12070933
- Răileanu C., Tauchmann O., Silaghi C. Sympatric occurrence of Ixodes ricinus with Dermacentor reticulatus and Haemaphysalis concinna and the associated tick-borne pathogens near the German Baltic coast. Parasit. Vectors. 2022;15(1):65. doi: https://doi.org/10.1186/s13071-022-05173-2
- Shpynov S., Fournier P.E., Rudakov N., et al. Detection of members of the genera Rickettsia, Anaplasma, and Ehrlichia in ticks collected in the Asiatic part of Russia. Ann. NY Acad. Sci. 2006;1078:378–83. doi: https://doi.org/10.1196/annals.1374.075
- Igolkina Y., Bondarenko E., Rar V., et al. Genetic variability of Rickettsia ssp. in Ixodes persulcatus ticks from continental and island areas of the Russian Far East. Ticks Tick Borne Dis. 2016;7(6):1284–9. doi: https://doi.org/10.1016/j.ttbdis.2016.06.005
- Mediannikov O., Matsumoto K., Samoylenko I., et al. Rickettsia raoultii sp. nov., a spotted fever group rickettsia associated with Dermacentor ticks in Europe and Russia. Int. J. Syst. Evol. Microbiol. 2008;58(Pt. 7):1635–9. doi: https://doi.org/10.1099/ijs.0.64952-0
- Guccione C., Colomba C., Iaria C., Cascio A. Rickettsiales in the WHO European Region: an update from a One Health perspective. Parasit. Vectors. 2023;16(1):41. doi: https://doi.org/10.1186/s13071-022-05646-4
- Oteo J.A., Aránzazu P. Tick-borne rickettsioses in Europe. Ticks Tick Borne Dis. 2012;3(5-6):271–8. doi: https://doi.org/10.1016/j.ttbdis.2012.10.035
Дополнительные файлы