Изоляция и генетический анализ вируса Чикунгунья из комаров Aedes aegypti и Aedes albopictus, отловленных в Центральной Америке
- Авторы: Игнатьев Г.М.1, Оксанич А.С.1, Казакова Е.В.2, Самарцева Т.Г.1, Отрашевская Е.В.2, Уйба С.В.3, Трухин В.П.2
-
Учреждения:
- Научно-исследовательский институт вакцин и сывороток им. И.И. Мечникова
- Санкт-Петербургский научно-исследовательский институт вакцин и сывороток
- Латиноамериканский институт биотехнологии «Мечников»
- Выпуск: Том 100, № 5 (2023)
- Страницы: 310-318
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://microbiol.crie.ru/jour/article/view/18477
- DOI: https://doi.org/10.36233/0372-9311-354
- EDN: https://elibrary.ru/uwguml
- ID: 18477
Цитировать
Аннотация
Введение. Ареал обитания комаров родов Aedes spp., Culex spp., Culiseta spp. распространяется на Южную и Центральную Америку, включая Никарагуа. Мониторинг за распространением комаров-переносчиков и оценка их инфицированности арбовирусами могут предоставить информацию о возможности появления новых или увеличении случаев уже регистрируемых заболеваний, изменении инфекционности вирусов для человека при смене переносчика возбудителя.
Целью настоящей работы были выделение и идентификация арбовирусов, принадлежащих к родам Flavivirus и Alphavirus, из комаров видов A. albopictus, A. aegypti, Culiseta spp., Culex spp., отловленных в лесах Никарагуа.
Материалы и методы. Комары A. albopictus, A. aegypti, Culiseta spp., Culex spp. были отловлены в 2021 г. в сухой сезон в лесной зоне в Никарагуа в четырех разных локациях. Комаров объединяли в пулы по 5–8 особей (всего 236 пулов). Методом полимеразной цепной реакции с обратной транскрипцией пулы анализировали на наличие вирусов Чикунгунья (ВЧ), денге, Зика и жёлтой лихорадки. Положительные пулы инокулировали в культуру клеток С6/36 с целью получения изолятов и их дальнейшего секвенирования.
Результаты. Вирус денге был выявлен только в комарах Aedes spp.: в 7 пулах — A. aegypti, в 1 — A. albopictus. ВЧ также был выявлен только в комарах Aedes spp.: в 3 пулах — A. aegypti, в 1 — A. albopictus. Секвенирование нуклеотидных последовательностей генов 6К, Е1, Е2 и NS1 ВЧ, выделенного из комаров A. albopictus, показало, что по сравнению с аналогичными последовательностями генов из изолятов ВЧ, выделенных из комаров A. aegypti, в области гена белка 6К обнаружено 4 нуклеотидных и столько же аминокислотных замен, в области Е1 — 16 нуклеотидных замен, 10 из которых приводили к аминокислотным заменам, в области Е2 — 14 нуклеотидных и 11 аминокислотных замен, в области NS1 — 33 нуклеотидные и 19 аминокислотных замен.
Полный текст
Введение
Комары родов Aedes spp., Culex spp., Culiseta spp. являются переносчиками ряда возбудителей вирусных заболеваний: лихорадки денге, Зика, жёлтой лихорадки, Чикунгунья, Венесуэльского энцефаломиелита лошадей, Синдбис, относящихся к семействам Flaviviridae (род Flavivirus) и Togaviridae (род Alphavirus) [1–6]. Ареал обитания комаров родов Aedes spp., Culex spp., Culiseta spp. распространяется на Южную и Центральную Америку, включая Никарагуа [2, 3, 7–10]. Мониторинг за распространением комаров-переносчиков и оценка их инфицированности могут дать информацию о возможности появления новых заболеваний или увеличения случаев уже регистрируемых, а смена переносчика возбудителя может приводить к изменениям инфекционности вирусов для человека [5]. Выделение вирусов непосредственно от переносчиков, отловленных в естественных ареалах обитания, и изучение выделенных штаммов необходимы в процессе разработки средств диагностики, профилактики и лечения заболеваний, вызываемых альфа- и флавивирусами.
Целью данной работы было выделение и идентификация арбовирусов, принадлежащих к родам Flavivirus и Alphavirus, из комаров видов A. albopictus, A. aegypti, Culiseta spp., Culex spp., отловленных в лесах Никарагуа.
Материалы и методы
Комары
Комары были отловлены в 2021 г. в сухой сезон в лесной зоне Никарагуа в четырех разных локациях с координатами:
- локация 1 — 12.325527N 85.974662W;
- локация 2 — 12.323326N 85.974275W;
- локация 3 — 11.908210N 85.932490W;
- локация 4 — 11.903555N 85.938758W.
Среди отловленных комаров были представители родов Aedes spp. (A. albopictus, A. aegypti), Culiseta spp. и Culex spp. После определения видов комары были разделены на пулы по 5–8 особей одного вида, отловленных в одной локации. В общей сложности было создано 236 пулов. Каждый пул был гомогенизирован до получения суспензии в объёме 300 мкл среды Лейбовица L-15 («Gibco», «Thermo Fisher Scientific») рН 7,4 с использованием керамических шариков и гомогенизатора «SpeedMill Plus» («Analytik Jena»). Из гомогената каждого пула было отобрано по 140 мкл для выделения РНК, которую экстрагировали с использованием набора реагентов «QIAamp Viral RNA» («Qiagen»). При постановке полимеразной цепной реакции (ПЦР) с обратной транскрипцией (ОТ) использовали протоколы для каждого возбудителя. Те пулы, в которых были получены положительные результаты на какой-либо из тестируемых вирусов, были использованы для последующего выделения вируса на клетках.
Выделение вируса
Оставшийся объём суспензии комаров (200 мкл) фильтровали через фильтр PES 0,45 мкм. Полученным фильтратом проводили заражение монослоя клеток С6/36, выращенных в 24-луночных планшетах. Инфицирование проводили в объеме 100 мкл с использованием цельного препарата и разведения 1 : 10. Через 7 дней после инфицирования 100 мкл супернатанта использовали для следующего пассажа. Всего от первого заражения проведено 5 последовательных пассажей. После заражения клетки ежедневно осматривали на наличие признаков цитопатического действия.
Молекулярно-генетическое исследование
Молекулярно-генетическое исследование методом ОТ-ПЦР проводили по следующей методике. Из 140 мкл суспензии комаров с помощью комплекта реагентов «QIAamp Viral RNA» («Qiagen») выделяли РНК согласно инструкции производителя. Далее с использованием обратного праймера pNS1CHVrev2-3 для вируса Чикунгунья (ВЧ; область гена NS1); смеси обратных праймеров к вирусу денге panDVrev1 и panDVrev2 (область 3’-UTR), общих для всех 4 типов вируса (табл. 1); обратного праймера для вируса Зика pZVrev [9]; обратного праймера вируса жёлтой лихорадки pYFVrev (табл. 2) [11] и набора реагентов для ОТ («Синтол») на матрице вирусной РНК проводили реакцию ОТ и получали кДНК. На первом этапе смешивали 2 мкл обратных праймеров (10 пкмоль/мкл) с 6 мкл выделенной РНК и прогревали смесь при 95оС 5 мин. После чего охлаждали пробирки при комнатной температуре 2 мин и добавляли 22 мкл смеси для ОТ (9 мкл деионизированной воды, 12 мкл 2,5-кратного буфера для ОТ («Синтол»), 1 мкл MMLV-ревертазы («Синтол»)) и инкубировали при 42оС, 30 мин. Для инактивации ревертазы смесь прогревали в течение 5 мин при 95оС.
Таблица 1. Нуклеотидные последовательности праймеров и зондов для выявления РНК ВЧ и вируса денге в полевых образцах методом ОТ-ПЦР в реальном времени
Table 1. Nucleotide sequences of primers and probes for detection of CHIKV and dengue virus RNA in collected samples using real-time RT-PCR
Олигонуклеотид Oligonucleotide | Нуклеотидная последовательность, 5’–3’ Nucleotide sequence, 5’–3’ | Размер ПЦР-продукта PCR product size |
ВЧ (область гена NS1) | CHIKV (the NS1 gene region) | ||
pNS1CHVfor | GTGTGCTGTTCTCAGTAGGGTCAACG | 218 п.н. | bp |
pNS1CHVrev | GTCTGCGTGGTGGGTTACCGC | |
zNS1CHVfor | FAM-GGCTACGTCGTTAAGAGAATAACGATGAGCCC-BHQ1 | |
Вирус денге (область 3’-UTR) | Dengue virus (the 3’-UTR region) | ||
panDVfor | GACTAGYGGTTAGAGGAGACCC | 190 п.н. | bp |
panDVrev1 | CGTTCTGTGCCTGGAATGATG | |
panDVrev2 | CGCTCTGTGCCTGGATTGATG | |
zDVfor | FAM-GCATATTGACGCTGGGARAGACCAGAG-BHQ1 | |
Примечание. Y — либо С, либо Т; R — либо А, либо G.
Note. Y — either C or T; R — either A or G.
Таблица 2. Нуклеотидные последовательности праймеров для амплификации РНК вирусов Зика и жёлтой лихорадки методом ОТ-ПЦР с электрофоретической детекцией
Table 2. Nucleotide sequences of primers for amplification of Zika and yellow fever virus RNA using RT-PCR and electrophoresis detection
Олигонуклеотид Oligonucleotide | Нуклеотидная последовательность, 5’–3’ Nucleotide sequence, 5’–3’ | Размер ПЦР-продукта PCR product size |
Зика (область гена NS5) | Zika (the NS5 gene region) | ||
pZVfor | CCGCGCCATCTGGTATATGT | 450 п.н. | bp |
pZVrev | CTCCACTGACTGCCATTCGT | |
Жёлтая лихорадка (область гена E) | Yellow fever (the E gene region) | ||
pYFVfor | TACCCTGGAGCAAGACAAGT | 465 п.н. | bp |
pYFVrev | GCTTTTCCATACCCAATGAA | |
Для вирусов Зика и жёлтой лихорадки проводили ПЦР с детекцией продуктов амплификации в агарозном геле с использованием неоригинальных праймеров других авторов [9, 11], которые представлены в табл. 2. Амплификацию проводили по следующей программе: 95оС — 1 мин 30 с; 30 циклов: 95оС — 20 с, 55оС — 15 с, 72оС — 30 с; 72оС — 10 мин.
ПЦР в реальном времени проводили на ВЧ и вирус денге с использованием оригинальных праймеров и зондов. Амплификацию проводили на приборе «DTprime» («ДНК-Технология») по следующей программе: 95оС — 1 мин 30 с; 40 циклов: 95оС — 15 с, 55оС — 40 с.
Для получения фрагментов генов 6К, E1, Е2 и NS1 ВЧ и их секвенирования использовали олигонуклеотиды собственной разработки и методику, описанные ранее [12].
Все ПЦР-продукты перед секвенированием очищали из геля с использованием набора реагентов «Cleanup Standard» (#BC022, «Евроген») и клонировали в векторе «pGEM-T Easy» («Promega») в соответствии с инструкцией производителя. Затем отбирали клоны, выделяли из них плазмиды и секвенировали по Сэнгеру с использованием стандартных праймеров для секвенирования T7 и SP6. Полученные нуклеотидных последовательностей выравнивали с помощью программы «MEGA11»1.
Филогенетический анализ
Филогенетический анализ проводили с использованием метода молекулярного датирования с помощью пакета программ «BEAST v. 1.10.4» и приложения «Beauty v. 1.10.4»2. При построении деревьев применяли алгоритм нуклеотидных замен HKY3 со строгими молекулярными часами. Анализ проводили с построением 10 млн деревьев и отбирали каждое 1000-е дерево с использованием программного обеспечения «MEGA11». Множественное выравнивание проводили с использованием генетических последовательностей фрагментов геномов ВЧ (E2, 6K, E1), изолированных в разных регионах мира из комаров (30 последовательностей). Позиция в геноме фрагмента, по которому проводили филогенетический анализ, составила 8574–11 303 нт (позиции указаны по прототипному штамму 1959 г., номер GenBank KX262990). Также в филогенетическое дерево было добавлено 8 нуклеотидных последовательностей ВЧ, изолированных от человека, 3 из которых были получены от больных в Никарагуа в 2014 и 2015 гг. и 4 представляли собой референсные последовательности вируса.
Инфицированность комаров определяли, как описано ранее [10, 13].
Результаты и обсуждение
В результате отлова в четырех локациях были собраны комары трех родов Aedes spp., Culex spp., Culiseta spp. Как следует из представленных в табл. 3 данных, в наибольшем количестве были представлены комары рода Aedes spp. — 954 особи: 604 (67%) особи A. aegypti, 314 (33%) особи A. albopictus. При исследовании 105 пулов комаров A. aegypti в 7 пулах была определена РНК вируса денге, в 3 пулах — РНК ВЧ. РНК вирусов Зика и жёлтой лихорадки не обнаружена. Не было отмечено одновременной детекции РНК ВЧ и вируса денге. При исследовании 54 пулов комаров A. albopictus в 1 пуле была выявлена РНК вируса денге, в 1 пуле — РНК ВЧ. РНК вирусов Зика и жёлтой лихорадки также не была обнаружена. Одновременной детекции РНК ВЧ и вируса денге не отмечено. В 46 пулах комаров рода Culex spp. и в 31 пуле комаров рода Culiseta spp. РНК детектируемых вирусов не выявлено.
Таблица 3. Род и количество отловленных комаров
Table 3. Genus and number of captured mosquitoes
Вид комаров Mosquito species | Количество особей Number of mosquitoes | Количество пулов Number of pools | Результаты ПЦР (положительные/отрицательные) PCR results (positive/negative) | |||
вирус Денге dengue virus | ВЧ CHIKV | вирус жёлтой лихорадки yellow fever virus | вирус Зика Zika virus | |||
Aedes spp. | 954 | 159 | 8/151 | 4/155 | 0/159 | 0/159 |
A. aegypti | 640 | 105 | 7/98 | 3/102 | 0/105 | 0/105 |
A. albopictus | 314 | 54 | 1/53 | 1/53 | 0/54 | 0/54 |
Culex spp. | 278 | 46 | 0/46 | 0/46 | 0/46 | 0/46 |
Culiseta spp. | 188 | 31 | 0/31 | 0/31 | 0/31 | 0/31 |
Для ВЧ комары положительного пула A. albopictus были отловлены в локации 1, а положительных пулов комаров A. aegypti — в локации 4. РНК вируса денге была определена в пулах комаров A. aegypti, отловленных в локации 2, и Aedes albopictus, отловленных в локации 2.
Минимальный уровень инфицирования комаров A. aegypti по вирусу денге составил 10,0, по ВЧ — 4,6. Минимальный уровень инфицирования комаров A. albopictus по вирусу денге и ВЧ составил 3,0. На основании полученных результатов можно предположить, что комары рода Aedes spp. инфицированы вирусом денге и ВЧ.
Показатель минимальной инфицированности комаров, безусловно, является важным показателем, но зависит от количества отловленных комаров (объём исследуемой выборки) и количества комаров в пуле, что влияет на чувствительность используемого метода. В ряде работ по исследованиям минимальной инфицированности комаров альфа- и флавивирусами этот показатель колебался от 0 до 12, что могло свидетельствовать только о потенциальной опасности заражения именно этим вирусом от этого комара [10, 13]. Возможность одновременного протекания лихорадок денге и Чикунгунья была показана ранее, а исследование серологических маркеров флави- и альфавирусов продемонстрировало наличие антител к вирусу денге и ВЧ [9, 14]. Для выделения вирусов использовали положительные по результатам ОТ-ПЦР пулы комаров — 8 пулов с вирусом денге и 4 пула с ВЧ.
Для выделения вирусов из полученных пулов комаров использовали клетки C6/36. Для каждого пула было проведено 5 последовательных пассажей. В клетках, заражённых образцами, содержащими ВЧ (по результатам ОТ-ПЦР), нарушение монослоя клеток — развитие цитопатического действия — регистрировалось на 2–3-м пассаже. При проведении 5-го пассажа 100% цитопатический эффект регистрировался на 72 ч. Для образцов, содержащих вирусы денге (по результатам ПЦР), цитопатический эффект не был столь выраженным. На каждом пассаже контроль за подлинностью изолятов и отсутствием перекрёстной контаминации проводился с использованием ОТ-ПЦР. По окончании выделения изолятов их секвенировали. В результате были получены изоляты, содержащие ВЧ, вирусы денге 1-го и 2-го типов. В отношении вирусов денге определяли только тип вируса из-за коротких фрагментов ПЦР-продуктов.
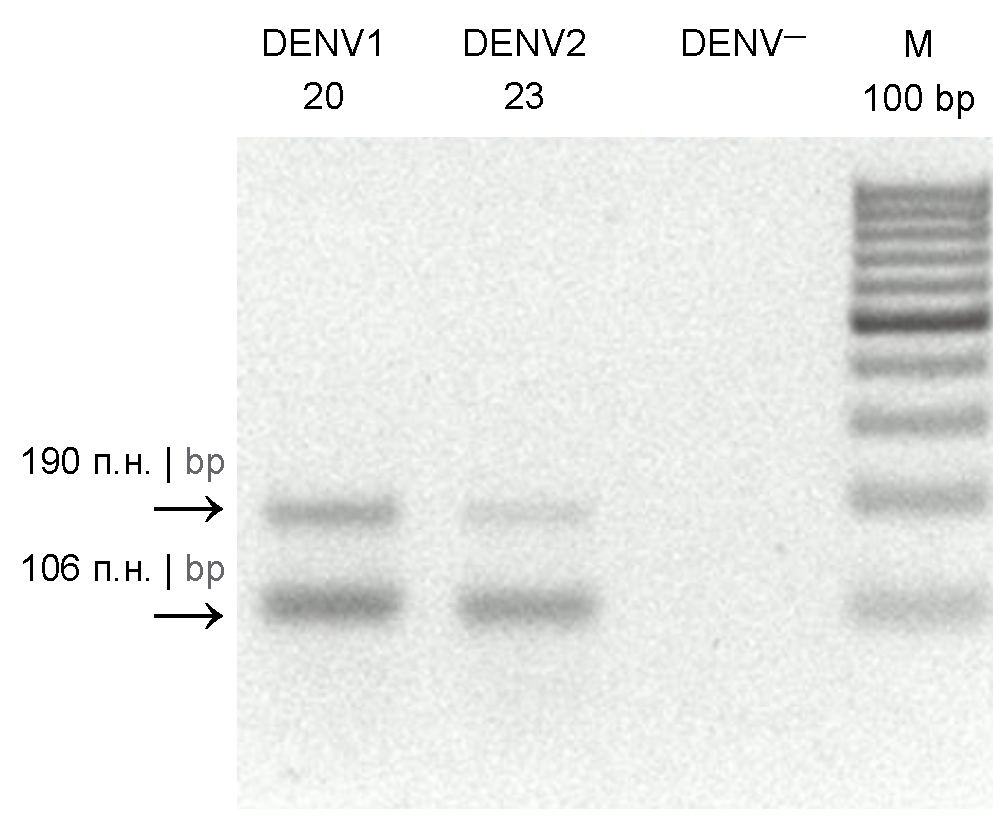
Как видно из электрофореграммы ампликонов (рис. 1), полученных с использованием универсальных праймеров ко всем 4 типам вируса денге, при амплификации образуются 2 продукта длиной 190 и 106 п.н. Как показало секвенирование фрагментов, они оба являются специфическими [15].
Рис. 1. Электрофорез ПЦР-продуктов в 2% агарозном геле. DENV1 20 и DENV2 23 — ампликоны вирусов денге 1-го и 2-го типов, полученные в 20 и 23 пулах соответственно; DENV— — отрицательный контроль ПЦР на вирус денге; М 100 bp — весовой ДНК-маркер.
Секвенирование нуклеотидных последовательностей генов 6К, Е1, Е2 и NS1 ВЧ из комаров A. albopictus (1 пул, локация 1) показало, что это был тот же штамм, который был изолирован в 2018 г. в этой же локации [12]. По сравнению с аналогичными последовательностями генов из изолятов ВЧ, выделенных из комаров A. aegypti (3 пула, локация 4), в области гена белка 6К было обнаружено 4 нуклеотидных и столько же аминокислотных замен, в области Е1 — 16 нуклеотидных замен, 10 из которых приводили к аминокислотным заменам, в области Е2 — 14 нуклеотидных и 11 аминокислотных замен и в области NS1 — 33 нуклеотидные и 19 аминокислотных замен (табл. 4). Три изолята, выделенные из комаров A. aegypti, не имели аминокислотных замен относительно друг друга. Выделенный штамм был депонирован в базе данных генетических последовательностей GenBank (NCBI) под номером OQ320495.
Таблица 4. Перечень нуклеотидных и аминокислотных замен в областях генов 6К, Е1, Е2 и NS1 у изолятов ВЧ, выделенных из комаров A. albopictus и A. aegypti, отловленных в разных локациях Никарагуа
Table 4. Nucleotide and amino acid substitutions in 6K, E1, E2, and NS1 gene regions in CHIKV isolates recovered from A. albopictus and A. aegypti mosquitoes captured in different locations in Nicaragua
Замены A. albopictus > A. aegypti | Substitutions A. albopictus > A. aegypti | |||||||
ген белка 6К | 6K protein gene | ген белка E1 | E1 protein gene | ген белка E2 | E2 protein gene | ген белка NS1 | NS1 protein gene | ||||
Н | N | А | Н | N | А | Н | N | А | Н | N | А |
A37G A54T C107T T176C | E13K F18L L36P A59V | G28A T79A G150A C441T T443C C579G G633A T683C C852T G955A G968T G979A A1081G C1106T C1217T T1308C | T10A M27L – – A148V – – T228M – K319E I323S K327E A361T V369A V406A – | C145T A406G T541G T543C A545G C558T G662A A760G G775A C914T C944T G1019A T1082C G1146A | H49Y K136E C181G C181G Q182R – R221K M254V G259R A305V A315V R340H V361A – | C7T T21C C253T A293G G307A T389C T489C T498G A540G T581C A699G A890G C1014T A1047G A1067G T1085C G1114A T1176C C1249T T1366A G1489A G1491A A1493T G1512A A1580T C1587T A1619C G1622C A1623G T1625G T1626A C1627G C1628G | P3S – R85C K98R A103T M130T – – – L194S – Y297C – – Q356R L362P A372T – R417C W456R A497T A497T E498V – E527V – N540T R541P R541P I542R I542R P543G P543G |
Σ Н: 4 | Σ А: 4 | Σ Н: 16 | Σ А: 10 | Σ Н: 14 | Σ А: 11 | Σ Н: 33 | Σ А: 19 |
Примечание. Н — нуклеотидная замена; А — аминокислотная замена. Позиция нуклеотидной или аминокислотной замены указана от начала гена.
Note. N — nucleotide substitution; A — amino acid substitution. The position of a nucleotide or amino acid substitution is shown from the beginning of a gene.
При анализе нуклеотидных и аминокислотных замен они в большей мере не соответствовали обычно изучаемым заменам, характерным для изучаемого региона [7]. Такие существенные различия могут быть связаны с тем, что основная масса изолятов ВЧ была выделена другими авторами из сывороток крови больных людей и в редких случаях — из комаров. Кроме того, основные изоляты, выделенные из комаров, были отловлены в городских агломерациях и редко — в удалённых от городов локациях, что было реализовано в настоящей работе. Различия в нуклеотидных последовательностях изолятов ВЧ во всех 4 генах можно объяснить также разной локацией отловленных комаров и разным видом комаров, в которых был выявлен вирус.
Таким образом, при выделении изолятов вирусов из комаров видов Aedes spp., Culex spp. и Culiseta spp., отловленных в лесах Никарагуа, были обнаружены ВЧ и вирусы денге 1-го и 2-го типов. Анализ некоторых генов ВЧ показал высокое генетическое разнообразие между вирусом, выделенным из комаров вида A. albopictus и A. aegypti.
Филогенетический анализ нуклеотидных последовательностей (рис. 2) показал, что наиболее близким родственником изолированного ВЧ является вирус, выделенный от человека в Африке в 2011 г. (номер GenBank KJ679577). Предполагаемое время жизни общего предка этих штаммов составляет 21 год (95% HPD 10–35). Также исследуемый изолят вошел в кластер с прототипными штаммами, выделенными в 1952–1986 гг. в Танзании и Африке.
Рис. 2. Филогенетическое дерево фрагментов генома E2, 6K, E1 ВЧ. В узлах дерева отмечена апостериорная вероятность > 0,75 и возраст группы. Выделен исследуемый вирус. Шкала показывает длину ветвей в годах.
1 Tamura K., Stecher G., Kumar S. MEGA11: Molecular Evolutionary Genetics Analysis Version 11. Mol. Biol. Evol. 2021;38(7):3022–3027. DOI: 10.1093/molbev/msab120
2 Drummond A.J., Rambaut A., Shapiro B., Pybus O.G. Bayesian coalescent inference of past population dynamics from molecular sequences. Mol. Biol. Evol. 2005;22(5):1185–1192.
DOI: 10.1093/molbev/msi103
3 Hasegawa M., Kishino H., Yano T. Dating of the human-ape splitting by a molecular clock of mitochondrial DNA. J. Mol. Evol. 1985;22(2):160–174. DOI: 10.1007/BF02101694
Об авторах
Георгий Михайлович Игнатьев
Научно-исследовательский институт вакцин и сывороток им. И.И. Мечникова
Email: oksanich@yahoo.com
ORCID iD: 0000-0002-9731-3681
д.м.н., профессор, главный сотрудник лаб. молекулярной биотехнологии НИИ вакцин и сывороток им. И.И. Мечникова
Россия, МоскваАлексей Сергеевич Оксанич
Научно-исследовательский институт вакцин и сывороток им. И.И. Мечникова
Автор, ответственный за переписку.
Email: oksanich@yahoo.com
ORCID iD: 0000-0002-8600-7347
к.б.н., в.н.с. лаб. молекулярной биотехнологии НИИ вакцин и сывороток им. И.И. Мечникова
Россия, МоскваЕлена Владимировна Казакова
Санкт-Петербургский научно-исследовательский институт вакцин и сывороток
Email: oksanich@yahoo.com
ORCID iD: 0000-0002-0218-6641
зам. директора по управлению персоналом и организационному проектированию Санкт-Петербургского НИИ вакцин и сывороток
Россия, Санкт-ПетербургТатьяна Геннадьевна Самарцева
Научно-исследовательский институт вакцин и сывороток им. И.И. Мечникова
Email: oksanich@yahoo.com
ORCID iD: 0000-0003-3264-6722
н.с. лаб. молекулярной биотехнологии НИИ вакцин и сывороток им. И.И. Мечникова
Россия, МоскваЕлена Викторовна Отрашевская
Санкт-Петербургский научно-исследовательский институт вакцин и сывороток
Email: oksanich@yahoo.com
ORCID iD: 0000-0002-2491-4072
ведущий сотрудник лаб. молекулярной биотехнологии НИИ вакцин и сывороток им. И.И. Мечникова
Россия, Санкт-ПетербургСтанислав Валентинович Уйба
Латиноамериканский институт биотехнологии «Мечников»
Email: oksanich@yahoo.com
ORCID iD: 0000-0001-9246-3915
генеральный директор Латиноамериканского института биотехнологий «Мечников»
Никарагуа, МанагуаВиктор Павлович Трухин
Санкт-Петербургский научно-исследовательский институт вакцин и сывороток
Email: oksanich@yahoo.com
ORCID iD: 0000-0002-6635-363X
директор Санкт-Петербургского НИИ вакцин и сывороток
Россия, Санкт-ПетербургСписок литературы
- Kraemer M.U.D., Sinka M.E., Duda K.A., et al. The global compendium of Aedes aegypti and Aedes albopictus occurrence. Sci. Data. 2015;2:150035. DOI: http://doi.org/10.1038/sdata.2015.35
- Ponce P., Morales D., Argoti A., Cevallos V.E. First report of Aedes (Stegomyia) albopictus (Skuse) (Diptera: Culicidae), the Asian tiger mosquito, in Ecuador. J. Med. Entomol. 2018;55(1):248–9. DOI: http://doi.org/10.1093/jme/tjx165
- Hermanns K., Marklewitz M., Zirkel F., et al. Agua Salud alphavirus defines a novel lineage of insect-specific alphaviruses discovered in the New World. J. Gen. Virol. 2020;101(1):96–104. DOI: https://doi.org/10.1099/jgv.0.001344
- Guzman M.G., Halstead S.B., Artsob H., et al. Dengue: a continuing global threat. Nat. Rev. Microbiol. 2010;8(12 Suppl.):S7–16. DOI: http://doi.org/10.1038/nrmicro2460
- Vega-Rua A., Zouache K., Caro V., et al. High efficiency of temperate Aedes albopictus to transmit Chikungunya and dengue viruses in the Southeast of France. PLoS One. 2013;8(3):e59716. DOI: http://doi.org/10.1371/journal.pone.0059716
- Lundstrom J.O., Hesson J.C., Schafer M.L., et al. Sindbis virus polyarthritis outbreak signalled by virus prevalence in the mosquito vectors. PLoS Negl. Trop. Dis. 2019;13(8):e0007702. DOI: https://doi.org/10.1371/journal.pntd.0007702
- Villero-Wolf Y., Mattar S., Puerta-González A., et al. Genomic epidemiology of Chikungunya virus in Colombia reveals genetic variability of strains and multiple geographic introductions in outbreak, 2014. Sci. Rep. 2019;9(1):9970. DOI: https://doi.org/10.1038/s41598-019-45981-8
- Cevallos V., Ponce P., Waggoner J.J., et al. Zika and Chikungunya virus detection in naturally infected Aedes aegypti in Ecuador. Acta Trop. 2018;177:74–80. DOI: http://doi.org/10.1016/j.actatropica.2017.09.029
- Waggoner J.J., Gresh L., Vargas M.J., et al. Viremia and clinical presentation in Nicaraguan patients infected with Zika virus, Chikungunya virus, and Dengue virus. Clin. Infect. Dis. 2016;63(12):1584–90. DOI: http://doi.org/10.1093/cid/ciw589
- da Costa C.F., da Silva A.V., do Nascimento V.A., et al. Evidence of vertical transmission of Zika virus in field-collected eggs of Aedes aegypti in the Brazilian Amazon. PLoS Negl. Trop. Dis. 2018;12(7):e0006594. DOI: https://doi.org/10.1371/journal.pntd.0006594
- Eldadah Z.A., Asher D.M., Godec M.S., et al. Detection of flaviviruses by reverse-transcriptase polymerase chain reaction. J. Med. Virol. 1991;33(4):260–7. DOI: https://doi.org/10.1002/jmv.1890330410
- Игнатьев Г.М., Каа К.В., Оксанич А.С. и др. Индикация и идентификация вирусов денге и Чикунгунья в комарах рода Aedes spp., отловленных в центральной Америке. Журнал микробиологии, эпидемиологии и иммунобиологии. 2020;97(3):227–32. Ignatyev G.M., Kaa K.V., Oksanich A.S., et al. Indication and identification of dengue and Chikungunya viruses in Aedes spp. Mosquitoes captured in Central America. Journal of Microbiology, Epidemiology and Immunobiology. 2020;97(3):227–32 DOI: https://doi.org/10.36233/0372-9311-2020-97-3-4 EDN: https://elibrary.ru/ufhtab
- Čabanová V., Tichá E., Bradbury R.S., et al. Mosquito surveillance of West Nile and Usutu viruses in four territorial units of Slovakia and description of a confirmed autochthonous human case of West Nile fever, 2018 to 2019. Euro Surveill. 2021;26(19):2000063. DOI: https://doi.org/10.2807/1560-7917.ES.2021.26.19.2000063
- Отрашевская Е.В., Казакова Е.В., Жиренкина Е.Н. и др. Ретроспективный серологический анализ распространения флавивирусных лихорадок и лихорадки Чикунгунья в Никарагуа; авидность специфических антител, как инструмент дифференциальной диагностики. Журнал микробиологии, эпидемиологии и иммунобиологии. 2022;99(2):215–24. Atrasheuskaya A.V., Kazakova E.V., Zhirenkina E.N., et al. The study of flaviviruses and Chikungunya virus seroprevalence in Nicaragua – virus-specific antibody avidity assay as a tool for differential diagnosis. Journal of Microbiology, Epidemiology and Immunobiology. 2022;99(2):215–24. DOI: https://doi.org/10.36233/0372-9311-196 EDN: https://elibrary.ru/tyopaj
- Shurtleff A.C., Beasley D.W., Chen J.J., et al. Genetic variation in the 3′ non-coding region of dengue viruses. Virology. 2001;281(1):75–87. DOI: https://doi.org/10.1006/viro.2000.0748
Дополнительные файлы