Исследование протективных свойств иммунодоминантных белков ортопоксвирусов при различных способах иммунизации
- Авторы: Зрелкин Д.И.1, Зубкова О.В.1, Ожаровская Т.А.1, Попова О.1, Воронина Д.В.1, Голдовская П.П.1, Вавилова И.В.1, Чугунова А.С.1, Должикова И.В.1, Щербинин Д.Н.1, Щебляков Д.В.1, Логунов Д.Ю.1, Гинцбург А.Л.1
-
Учреждения:
- Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
- Выпуск: Том 102, № 1 (2025)
- Страницы: 18-30
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://microbiol.crie.ru/jour/article/view/18755
- DOI: https://doi.org/10.36233/0372-9311-643
- EDN: https://elibrary.ru/ONKJVE
- ID: 18755
Цитировать
Аннотация
Введение. Всемирная организация здравоохранения в 2022 г. объявила оспу обезьян чрезвычайной ситуацией в области здравоохранения. Вирус оспы обезьян (MPV) принадлежит к роду Orthopoxvirus семейства Poxviridae. Ортопоксвирусы во время репликации образуют 2 отдельные формы вирусных частиц: экзоцитозом выделяется оболочечный внеклеточный вирион (EEV), а зрелый внутриклеточный вирион (IMV) высвобождается в результате лизиса клеток. У этих двух форм вирионов отличаются наборы поверхностных белков, что обусловливает их различия в иммуногенности и инфекционности.
Цель работы — оценка иммуногенной и протективной активности 9 поверхностных антигенов вируса осповакцины.
Материал и методы. Геномы рекомбинантных аденовирусов человека 2-го серотипа, несущих поверхностные антигены вируса осповакцины, получали методом гомологичной рекомбинации в бактериальных клетках с последующей сборкой аденовирусных частиц в клетках НЕК293. Иммуногенные и протективные свойства полученных рекомбинантных аденовирусов изучали на мышах BALB/c. Сыворотки крови после иммунизации животных исследовали методом иммуноферментного анализа на наличие антител к вирусу осповакцины. Протективные свойства оценивали на летальной модели инфекции мышей после интраназального заражения вирусом осповакцины штамма Western Reserve.
Результаты. Наиболее иммуногенными и протективными антигенами вируса осповакцины в составе рекомбинантных аденовирусов человека 2-го серотипа были гликопротеин В5 оболочечного внеклеточного вириона и мембранно-ассоциированный белок Н3 зрелого внутриклеточного вириона. При изучении защитной эффективности антигенов показана 100% эффективность В5 и Н3 при интраназальной иммунизации.
Заключение. При использовании панели рекомбинантных аденовирусных векторов, несущих гены поверхностных белков вируса осповакцины, показано, что оптимальная защита может быть достигнута с помощью комбинации антигенов оболочечного и зрелого вирионов. Данный подход может быть использован при разработке новых поливалентных вакцин против различных вирусных инфекций.
Ключевые слова
Полный текст
Введение
Ортопоксвирусы (ОПВ) относятся к семейству Poxviridae, подсемейству Chordopoxvirinae, роду Orthopoxvirus, который содержит 13 видов: Orthopoxvirus abatinomacacapox, Orthopoxvirus akhmetapox, Orthopoxvirus camelpox, Orthopoxvirus cowpox, Orthopoxvirus ectromelia, Orthopoxvirus monkeypox, Orthopoxvirus raccoonpox, Orthopoxvirus skunkpox, Orthopoxvirus taterapox, Orthopoxvirus vaccinia, Orthopoxvirus variola, Orthopoxvirus volepox и неофициально классифицированный вирус оспы Аляски1. Виды делятся на 2 родственные клады: ОПВ «Старого Света» (евразийские и африканские) и североамериканские ОПВ [1]. Многие из этих вирусов могут вызывать серьёзные заболевания у домашних животных, а также зоонозные инфекции у человека. Заражение людей чаще всего происходит при разведении скота, контакте с домашними животными, а также при торговле экзотическими животными в результате непосредственного контакта с ними. При попадании в неэндемичные регионы энзоотические ОПВ могут представлять угрозу для местных и эндемичных видов [2–4].
ОПВ разных видов антигенно и иммунологически близки друг к другу. Вакцинация против натуральной оспы, к примеру, обеспечивает перекрёстную защиту и от других представителей рода [5]. Однако после глобального искоренения натуральной оспы в 1980 г. многие страны начали постепенно прекращать плановую вакцинацию от этого заболевания [6]. В результате на сегодняшний день значительная часть населения лишена иммунной защиты к ОПВ. Именно это обстоятельство объясняет учащение в различных регионах мира вспышек, среди которых особо выделяется оспа обезьян. Произошедшая в 2022 г. глобальная вспышка была признана Всемирной организацией здравоохранения (ВОЗ) чрезвычайной ситуацией в области общественного здравоохранения, имеющей международное значение [7]. Продолжающаяся эпидемия оспы обезьян в странах Африки может привести к ускоренной вирусной эволюции и адаптации к передаче зоонозного заболевания от человека к человеку [8]. Несмотря на существующие вакцинные препараты, ВОЗ рекомендовала разработку менее реактогенных вакцин для повышения эффективности и длительности защиты с целью контроля текущей вспышки.
ОПВ имеют большой и сложный протеом, содержащий более 200 белков, из которых более 30 относятся к структурным [9, 10]. Во время инфекции вирус существует в двух антигенно различных инфекционных формах [11–13]. Внутриклеточные зрелые вирионы (IMV) являются основными инфекционными вирусными частицами и играют ключевую роль в передаче вируса от человека к человеку. Поверхностная мембрана этой формы содержит по меньшей мере 11 белков: A14.5 (~10 кДа), E10 (12 кДа), I5 (13 кДа), A13 (14 кДа), A27 (14 кДа), A9 (~18 кДа), A14 (17–25 кДа), A17 (23–29 кДа), L1 (25–29 кДа), D8 (34 кДа) и H3 (35 кДа) [9–13]. Внеклеточные оболочечные вирионы (EEV) образуются из IMV и имеют дополнительную липопротеиновую мембрану, отвечающую за распространение вируса внутри организма [12]. Поверхностные белки EEV и IMV обеспечивают инфекционность ОПВ и служат основными мишенями для индукции протективного иммунитета [14, 15]. Поскольку антитела, нейтрализующие IMV, не нейтрализуют EEV, считается, что для максимальной защиты необходима иммунизация антигенами обеих этих форм [16].
Иммунодоминантными белками, на которые вырабатываются антитела, в том числе вируснейтрализующие, являются два гликопротеина EEV — А33 и В5, а также белки IMV: L1, H3, D8 и комплекс из 3 белков незрелого вириона А14, А17 и D13 либо комплекс А14, А17 и А27 зрелого вириона [14, 17–19]. Белки А33 и В5 играют роль в образовании оболочечного вириона и последующей инфекции [14]. Среди поверхностных белков зрелого вириона 3 белка опосредуют прикрепление вируса к клетке-хозяину. Белок D8 образует димеры на вирусной мембране и обеспечивает инфекционность вириона за счёт связывания с хондроитинсульфатом клеточной мембраны [20]. Белки A27 и H3 связывают гепарансульфат. А27 — мажорный белок мембраны, необходим для образования оболочечного внеклеточного вириона и участвует в прикреплении вируса к клетке и последующем слиянии вирусной и клеточной мембран. А27 формирует комплекс с трансмембранными белками А14 и А17, которые являются важными структурными элементами мембраны зрелого вириона. А17 также необходим для проникновения вируса в клетку и служит якорем для А27 [21]. Н3 связывается с поверхностью клетки через гепарансульфаты и, как и белки D8 и A27, участвует в проникновении вируса в клетку. Н3 является основным белком при развитии иммунного ответа в организме человека [22]. L1 — трансмембранный белок, который необходим для формирования зрелых вирионов и участвует в проникновении вируса в клетку [23].
Хотя большинство этих антигенов (A27, L1, B5 и A33) были изучены в составе различных поливалентных вакцин [18, 24, 25], некоторые иммунодоминантные белки не были включены в эти исследования. Кроме того, при высокой иммуногенности ОПВ сами по себе антигены обладают низкой иммуногенностью. Вакцинация очищенными белками или ДНК, кодирующими белки вируса осповакцины, требует многократной иммунизации для индукции протективного иммунного ответа [24, 26, 27]. В отличие от ДНК-вакцин и субъединичных вакцин, было показано, что вакцинация рекомбинантными аденовирусами (rAd) способствует формированию как напряжённого гуморального и клеточного иммунного ответа, так и защитного иммунитета после однократной иммунизации [28–30]. Учитывая важность быстрой индукции защитного иммунитета в условиях потенциальной вспышки, мы изучили возможность однократной иммунизации rAd, экспрессирующими антигены EEV и IMV вируса осповакцины.
Целью данной работы являлась оценка иммуногенной и протективной активности 9 поверхностных антигенов вируса осповакцины. Для реализации данной цели были сконструированы rAd, несущие гены поверхностных белков зрелого (D8, H3, L1, А14, А17, А27 и D13) и внеклеточного (А33 и В5) вирионов вируса осповакцины. Далее проводили исследование индивидуальных иммуногенных и протективных свойств полученных аденовирусов при интраназальном и внутримышечном способах иммунизации. Данный подход может использоваться при разработке новых поливалентных вакцин против различных вирусных инфекций.
Материалы и методы
Культуры клеток и вирусы
Клетки линии Vero E6 (почка зелёной мартышки) культивировали в среде DMEM («Cytiva»), содержащей 4% фетальной сыворотки крупного рогатого скота («Gibco»), 25 000 ЕД пенициллина и 25 мг стрептомицина («Панэко») при 5% CO2. Клетки линии НЕК293 (почка эмбриона человека) культивировали в среде DMEM («Cytiva»), содержащей 10% фетальной сыворотки крупного рогатого скота («Gibco»), 25 000 ЕД пенициллина и 25 мг стрептомицина («Панэко») при 5% CO2.
Вирус осповакцины штамм Western Reserve (VACV WR) (GenBank #OP584857.1) накапливали в клетках Vero E6. Аликвоты вируссодержащей среды хранили при –80ºС. Биологическую активность вируса определяли стандартным методом титрования на культуре клеток путём подсчёта бляшек [31].
Получение рекомбинантных аденовирусов
rAd конструировали с использованием технологии, описанной ранее [32]. Гены антигенов вируса осповакцины были амплифицированы с генома VACV WR (GenBank #OP584857.1) с использованием праймеров, указанных в табл. 1, и клонированы под контроль промотора цитомегаловируса человека. Плазмидные векторы с геномом rAd человека 2-го серотипа (rAd2) и целевым антигеном получали методом гомологичной рекомбинации в бактериальных клетках. rAd собирали и накапливали в клетках НЕК293. Очистку и концентрирование вирусов проводили методом ультрацентрифугирования в градиенте плотности хлорида цезия в соответствии со стандартной методикой [33]. Количество вирусных частиц определяли стандартным спектрофотометрическим методом [34].
Таблица 1. Последовательности праймеров для амплификации генов вируса осповакцины
Table 1. Primer sequences for amplification of vaccinia virus genes
Название | Name | Последовательность | Sequence |
A33-F | CACCGGCGGTCGACAGATCTGCCACCATGATGACACCAGAAAACGACG |
A33-R | GATATCTCTAGATTAACAAAAATACTTTCTAACTTCTTGTG |
H3-F | ACTAAGCTTATATGGCGGCGGCGAAAACT |
H3-R | ATCTAGATATCTG TTAGATAAATGCGGTAAC |
B5-F | CACCGGCGGTCGACAGATCTGCCACCATGAAAACGATTTCCGTTGTTACG |
B5-R | TCTAGATTACGGTAGCAATTTATGGAACTTATA |
D8-F | CACCGGCGGTCGACAGATCTGCCACCATGCCGCAACAACTATCTCCTATTAA |
D8-R | GATATCGCTAGCTTACTAGTTTTGTTTTTCTCGCGAATATCG |
A14-F | CACCGGCGGTCGACAGATCTGCCACCATGGACATGATGCTTATGATTGG |
A14-R | GATATCTCTAGATTATTAGTTCATGGAAATATCGCTATG |
A27-F | CACCGGCGGTCGACAGATCTGCCACCATGGACGGAACTCTTTTCCC |
A27-R | TCTAGATTATTACTCATATGGGCGCCGTC |
L1-F | CACCGGCGGTCGACAGATCTGCCACCATGGGTGCCGCGGCAAGCAT |
L1-R | GATATCTCTAGATTATCAGTTTTGCATATCCGTGGTAGC |
A17-F | CACCGGCGGTCGACAGATCTGCCACCATGAGTTATTTAAGATATTACAATATG |
A17-R | GATATCTCTAGATTATTAATAATCGTCAGTATTTAAACTG |
D13-F | CACCGGCGGTCGACAGATCTGCCACCATGAATAATACTATCATTAATTCTTTG |
D13-R | ACTAGTTTATTAGTTATTATCTCCCATAATCTTG |
Животные
Мыши инбредной линии BALB/c, самцы и самки массой тела 16–18 г, были получены из питомника НПП «Питомник лабораторных животных г. Пущино» ФИБХ РАН. Животные содержались на базе вивария НИЦЭМ им. Н.Ф. Гамалеи в соответствии с требованиями по содержанию лабораторных животных и имели свободный доступ к корму и воде. Авторы подтверждают соблюдение институциональных и национальных стандартов по использованию лабораторных животных в соответствии с «Consensus Author Guidelines for Animal Use» (IAVES, 23.07.2010). Протокол исследования одобрен Комитетом по биомедицинской этике НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (протокол № 34 от 16.01.2023).
Иммунизация и заражение животных
Пятинедельным мышам BALB/c интраназально под лёгким ингаляционным наркозом или внутримышечно вводили rAd в дозе 2 × 1010 вирусных частиц. Повторно те же аденовирусы вводили в той же дозе через 21 день. Образцы сыворотки собирали на 28-й день после 1-й иммунизации. Иммунизированные мыши были подвергнуты интраназальному заражению VACV WR в дозе 16 ЛД50 (5 × 104 БОЕ) спустя 35 дней после 1-й иммунизации. В течение 14 дней после заражения проводили ежедневный осмотр животных и фиксировали клинические симптомы оспенной инфекции (снижение двигательной активности, сгорбленность, взъерошенность шерсти, конъюнктивит), изменение массы тела и гибель. Животных умерщвляли, если они теряли более 25% массы тела.
Иммуноферментный анализ
Титр специфических IgG-антител к вирусу осповакцины в образцах сыворотки определяли с помощью иммуноферментного анализа. 96-луночные планшеты сенсибилизировали VACV WR (105 БОЕ/планшет), разведённым в карбонат-бикарбонатном буфере (рН 9,6), в течение ночи при 4ºC. Образцы сыворотки двукратно серийно разводили до 1 : 102 400, добавляли в заблокированные 96-луночные планшеты и инкубировали при 37ºC в течение 1 ч. Затем планшеты промывали и в каждую лунку добавляли вторичные антитела, конъюгированные с комплексом рекомбинантного стрептавидина с пероксидазой хрена. Инкубировали в течение 1 ч при 37ºC. После этого в планшеты вносили тетраметилбензидина гидрохлорид. Реакцию останавливали добавлением H2SO4, поглощение (450 нм) считывали с помощью планшетного фотометра «Multiskan FC» («ThermoFisher»). За конечный титр принимали наибольшее разведение сыворотки, значение оптической плотности в которой в 2 раза и более превышало значение в соответствующем разведении сыворотки крови интактных (неиммунизированных) мышей.
Статистическая обработка данных
Статистическую обработку данных и построение диаграмм проводили в программе «GraphPad Prism 8». Статистическую значимость различий между исследуемыми группами определяли с помощью Т-критерия Вилкоксона для зависимых выборок или U-критерия Манна–Уитни для независимых выборок. Различия считали достоверными при p < 0,05.
Результаты
Дизайн и получение rAd, экспрессирующих гены поверхностных антигенов
Основными иммунодоминантными белками вируса осповакцины являются 2 гликопротеина оболочечного внеклеточного вириона — А33 и В5, а также белки зрелого внутриклеточного вириона: D8, H3, L1, А14, А17, А27 и D13. Указанные антигены обладают высокой степенью гомологии между разными видами ОПВ (табл. 2) [35–37].
Таблица 2. Гомология между белками разных видов ОПВ
Table 2. Homology between proteins of different orthopoxvirus species
Антиген вируса осповакцины VACV antigen | Антиген (% гомологии) | Antigen (% homology) | ||
Orthopoxvirus monkeypox | Orthopoxvirus cowpox | Orthopoxvirus variola | |
L1 | M1 (98,4%) | CPVX099 (98,4%) | M1 (99,2%) |
H3 | H3 (93,83%) | CPVX112 (94,46%) | I3 (93,85%) |
D8 | E8 (94,41%) | CPVX125 (97,37%) | F8 (93,09%) |
D13 | E13 (98,91%) | CPVX131 (98,73%) | N3 (98,91%) |
A14 | А15 (100%) | CPVX146 (100%) | A14 (97,78%) |
A17 | А18 (97,55%) | CPVX150 (95,59%) | A17 (97,55%) |
A27 | А29 94,55%) | CPVX162 (95,45%) | A30 (93,64%) |
A33 | А35 (92,47%) | CPVX168 (91,49%) | A36 (89,25%) |
B5 | В6 (96,53%) | CPVX199 (93,69%) | B7 (92,74%) |
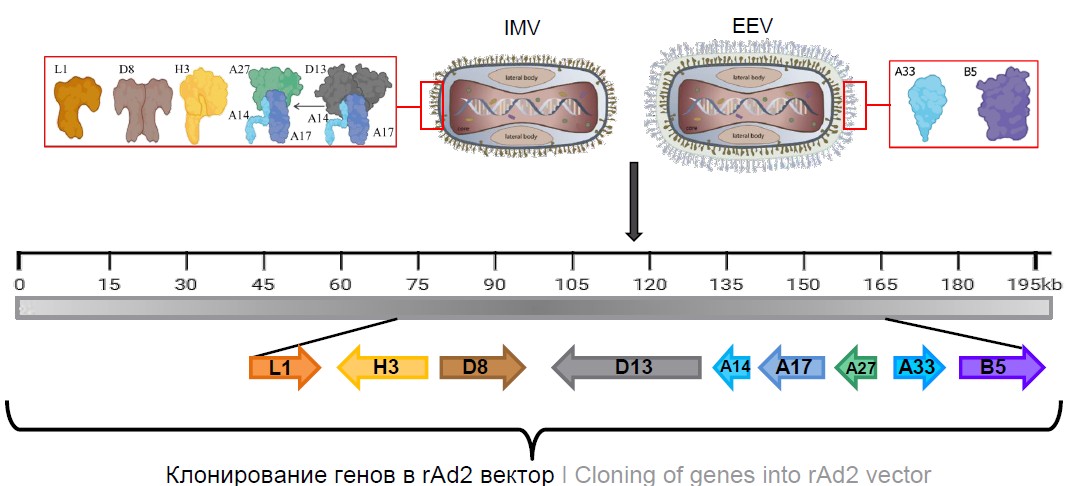
Гены описанных выше белков были получены из генома вируса осповакцины и клонированы в геном rAd2 под контроль промотора цитомегаловируса человека (рис. 1). Геном rAd2 несет делецию области Е1, которая делает аденовирус дефектным по репликации (в этот сайт делеции клонируется экспрессионная кассета с целевым геном). Для увеличения пакующей ёмкости дополнительно проводили делецию области Е3.
Рис. 1. Схема получения rAd, экспрессирующих поверхностные антигены вируса осповакцины.
L1 — миристоилированный белок; H3 — мембранно-ассоциированный белок p35 IMV; D8 — трансмембранный карбоангидразоподобный белок; D13 — белок мембраны IMV; А14 — структурный трансмембранный белок p16 IMV; А17 — трансмембранный белок IMV (фактор морфогенеза); А27 — белок мембраны IMV; В5 — мембранный гликопротеин типа I; А33 — мембранный гликопротеин типа II.
Fig. 1. Scheme for the production of recombinant adenoviruses expressing surface antigens of the vaccinia virus.
L1 — myristoylated protein; H3 — membrane-associated protein p35 IMV; D8 — transmembrane carbonic anhydrase-like protein; D13 — IMV membrane protein; A14 — structural transmembrane protein p16 IMV; A17 — transmembrane protein IMV (morphogenesis factor); A27 — membrane protein IMV; B5 — type I membrane glycoprotein; A33 — type II membrane glycoprotein.
Таким образом, нами были получены 9 rAd2, 2 из которых несли поверхностные антигены оболочечного вириона (rAd2-B5 и rAd2-A33), а 7 — антигены зрелого вириона (rAd2-H3, rAd2-L1, rAd2-D8, rAd2-D13, rAd2-A14, rAd2-A17 и rAd2-A27).
Векторы rAd2 индуцируют гуморальный иммунный ответ in vivo
Для оценки иммуногенности сконструированных rAd (rAd2-A33, rAd2-B5, rAd2-H3, rAd2-L1, rAd2-D8, rAd2-D13, rAd2-A14, rAd2-A17, rAd2-A27) мышам внутримышечно или интраназально вводили аденовирусы в дозе 2 × 1010 вирусных частиц однократно или двукратно. Титры специфических IgG-антител к вирусу осповакцины определяли методом иммуноферментного анализа на 28-е сутки после иммунизации (рис. 2, 3).
Рис. 2. Иммуногенность rAd, экспрессирующих поверхностные антигены вируса осповакцины, после однократной (а) и двукратной (б) внутримышечной иммунизации.
На рисунках указана достоверность при p < 0,05; *p < 0,0001. К– — контроль.
Fig. 2. Immunogenicity of recombinant adenoviruses expressing surface antigens of the vaccinia virus after single (a) and double (b) intramuscular immunization.
The figures show the confidence at p < 0.05; *p < 0.0001. C– — control.
Рис. 3. Иммуногенность rAd, экспрессирующих поверхностные антигены вируса осповакцины, после двукратной интраназальной иммунизации.
На рисунке указана достоверность при p < 0,05; *p < 0,0001. К– — контроль.
Fig. 3. Immunogenicity of recombinant adenoviruses expressing surface antigens of the vaccinia virus after two intranasal immunizations.
The figure shows the confidence at p < 0.05; *p < 0.0001. C– — control.
Однократная внутримышечная иммунизация приводила к формированию специфических IgG-антител у мышей, которым вводили rAd2-B5, rAd2-H3, rAd2-D8, rAd2-D13 и rAd2-A14. Значения титров в этих группах имели значимые отличия от контрольной группы, где титры составляли менее 1 : 50 (рис. 2, а). Высокий уровень IgG-антител обнаружен в группе мышей, иммунизированных rAd2-H3 (средние геометрические титры (СГТ) 1 : 3676). Введение rAd2-B5 приводило к индукции IgG-антител с СГТ = 1 : 348,2. Минимальный уровень IgG-антител наблюдали для групп rAd2-D8 (СГТ = 1 : 100), rAd2-A14 (СГТ = 1 : 107,2) и rAd2-D13 (СГТ = 1 : 57,43) без достоверных различий между группами. Двукратная иммунизация привела к значительному росту уровня IgG-антител по сравнению с однократной только для групп rAd2-H3 (СГТ = 1 : 14703) и rAd2-B5 (СГТ = 1 : 2111) (рис. 2, б). Существенных различий между другими группами не обнаружено.
При однократной интраназальной иммунизации специфические IgG-антитела в сыворотке крови не были детектированы ни в одной группе. При двукратной интраназальной иммунизации специфические IgG-антитела обнаружены в сыворотке крови животных, которым вводили rAd2-B5 и rAd2-H3. Значения титров в этих группах имели значимые отличия от контрольной группы, где титры составляли менее 1 : 50 (рис. 3). Высокий уровень антител обнаружен в группе мышей, иммунизированных rAd2-H3 (СГТ = 1 : 1902,73). Введение rAd2-B5 приводило к индукции IgG-антител с СГТ = 1 : 183,4.
Протективная эффективность rАд2 in vivo
Следующим шагом была проверка защитной эффективности антигенов. Через 35 дней от начала двукратной иммунизации мышей заражали патогенным штаммом WR в дозе 16 ЛД50 (5 × 104 БОЕ). Инфицирующая доза была выбрана на основании предварительных экспериментов по определению ЛД50 in vivo [38]. Выживаемость и изменение массы тела регистрировали в течение 14 дней после заражения.
Как и ожидалось, в контрольной группе ярко выраженные клинические признаки заболевания с потерей массы тела более 13% проявлялись уже с 4-го дня. Как показано на рис. 4, все контрольные животные быстро теряли массу и умирали на 5‒8-й день после заражения.
Рис. 4. Протективность rAd, экспрессирующих поверхностные антигены вируса осповакцины, после внутримышечной (а, б) или интраназальной (в, г) иммунизации на модели летальной инфекции у мышей.
а, в — динамика веса (на графике указаны среднее значение и стандартная ошибка среднего значения); б, г — выживаемость. К– — контроль.
Fig. 4. The protective efficacy of recombinant adenovirus vectors expressing the surface antigens of the vaccinia virus after intramuscular (a, b) or intranasal (c, d) immunization in a mouse model of lethal infection.
a, c — weight dynamics (the graph shows the average value and the standard error of the average value); b, d — survival. C– — control.
При внутримышечной иммунизации rAd2-B5, экспрессирующим гликопротеин В5 EEV, мы наблюдали 20% защиту животных от летальной инфекции (рис. 4, а, б). Двукратная внутримышечная иммунизация rAd2-D8, экспрессирующим гликопротеин D8 IMV, обеспечила 40% выживаемость животных. Животные, иммунизированные rAd2, экспрессирующими другие поверхностные антигены, потеряли 25% от своего первоначального веса в течение 5‒7 дней после заражения. По результатам исследования сделан вывод о том, что при использовании внутримышечного способа введения одного антигена недостаточно для защиты.
Интересно, что интраназальная иммунизация значительно уменьшала тяжесть инфекции и защищала животных как от летального исхода, так и от потери веса (рис. 4, в, г). В частности, при иммунизации rAd2-B5 мы наблюдали 100% защитную эффективность. Стоит отметить, что в группе животных, иммунизированных rAd2-B5, незначительную потерю веса (не более 3%) на 3‒5-й дни наблюдали только у половины животных. В группе rAd2-H3 выживаемость составила 87,5% (пала 1 мышь из 8). Кроме того, на 5-й день у 1 животного потеря веса была около 15% с постепенным восстановлением к 14-му дню. В группах rAd2-A33, rAd2-L1, rAd2-D8 и rAd2-D13 выживаемость составила 75%. Временная потеря веса к 5-му дню для групп не превышала 25%. У животных из групп rAd2-A17 и rAd2-A27 наблюдали 50% летальность при потере веса не более 15%. Животные, иммунизированные rAd2-A14, потеряли 21% от своего первоначального веса в течение 5 дней после заражения. Выживаемость в этой группе составила всего 25%.
Эти данные свидетельствуют о том, что rAd2-B5 и rAd2-H3 являются оптимальными векторами для защиты от интраназального заражения вирусом осповакцины, демонстрируя важность B5 и H3 в качестве протективных антигенов в этой модели ортопоксвирусной инфекции. Поэтому далее мы проверили эффективность сочетанной иммунизации (внутримышечно + интраназально) для индукции как системного, так и местного ответа.
Мышам внутримышечно вводили rAd2-B5 или rAd2-H3 в дозе 2 × 1010 вирусных частиц, через 21 день тот же аденовирусный вектор вводили интраназально. Через 35 дней от начала иммунизации животных заражали патогенным штаммом WR в дозе 16 ЛД50 (5 × 104 БОЕ). Выживаемость и изменение массы тела регистрировали в течение 14 дней после заражения (рис. 5).
Рис. 5. Протективность rAd2-B5 и rAd2-H3 после сочетанной иммунизации (внутримышечно + интраназально) на модели летальной инфекции у мышей.
а — динамика веса; б — выживаемость. К– — контроль.
Fig. 5. The protective efficacy of recombinant adenovirus vectors rAd2-B5 and rAd2-H3 after combined immunization (im+in) in a mouse model of lethal infection.
a — weight dynamics; b — survival. C– — control.
Сочетанная иммунизация rAd2-B5 или rAd2-H3 обеспечивала 100% защиту животных от летальной инфекции. В группе животных, внутримышечно и интраназально иммунизированных rAd2-B5, потеря веса не была зарегистрирована. Однако в группе rAd2-H3 на 6-й день у 2 животных из 8 потеря веса была около 23% с постепенным восстановлением к 14-му дню.
Обсуждение
С момента использования вируса осповакцины в прошлом столетии сопутствующая вакцинация больше не проводится. Несмотря на ликвидацию натуральной оспы, мир продолжает сталкиваться с ортопоксвирусными инфекциями, которые требуют активных действий. Серьёзные побочные эффекты после вакцинации вирусом осповакцины подчеркнули необходимость разработки более безопасных вакцинных препаратов для борьбы с актуальными ортопоксвирусными инфекциями, такими как оспа обезьян.
Российские учёные внесли большой вклад в разработку противооспенных вакцин [39–41]. В настоящее время наименее реактогенной и безопасной является недавно разработанная вакцина «ОртопоксВак» научного центра «Вектор» Роспотребнадзора для профилактики ортопоксвирусных инфекций, которая представляет из себя штамм Л-ИВП вируса осповакцины с 6 нарушенными генами вирулентности [42].
Высокая степень гомологии в центральной области генома вирусов оспы обезьян и осповакцины, составляющая 96,3%, указывает на их генетическое сходство [35–37]. В частности, гены MPV A35, B6, M1, E8, H3, A15, A18, A29 и E13 демонстрируют значительную консервативность с ортологичными генами ОПВ, включая вирусы осповакцины и натуральной оспы [24].
Для разработки ортопоксвирусных вакцин использованы несколько технологий: живая вакцина, аттенуированный вирус с дефектом репликации, вакцина на основе ДНК и субъединичные вакцины. У каждой из них есть свои недостатки, такие как серьёзные нежелательные явления при применении живой вакцины, более низкая иммуногенность у аттенуированных нереплицирующихся вакцин и ДНК-вакцин, а также длительный цикл разработки рекомбинантных белков [24, 26, 43, 44].
rAd обладают рядом ключевых свойств, что делает их хорошими кандидатами для разработки векторных вакцин. rAd физически и генетически стабильны, эффективно индуцируют врождённый и адаптивный иммунный ответ при различных способах введения, в том числе при доставке через поверхности слизистых оболочек [45]. Последнее является значительным преимуществом перед другими типами вакцин, т. к. эффективность вакцинации зависит от места введения и привлечения антигенпрезентирующих клеток [46]. Внутримышечная иммунизация приводит к стимуляции системного иммунного ответа, но не обеспечивает эффективный барьерный иммунитет. При этом интраназальная иммунизация может вызвать гуморальный и клеточный иммунитет как на слизистых оболочках, так и системно [47]. Таким образом, разработка мукозальных вакцин позволит удовлетворить потребности в более эффективной защите от патогенов, проникающих через слизистые оболочки.
Аденовирусная технология представляет собой универсальную платформу для быстрой разработки и внедрения вакцин для борьбы с вирусными инфекциями, обладающими в том числе пандемическим потенциалом. В этом исследовании мы разработали панель рекомбинантных репликативно-дефектных векторов на основе аденовируса человека 2-го серотипа, кодирующих поверхностные белки вируса осповакцины. Два белка внеклеточного оболочечного вириона (A33 и B5) и 7 белков внутриклеточного зрелого вириона (L1, D8, H3, A14, A17, A27, D13) были выбраны для клонирования в геном rAd2. Мы оценили иммуногенность 9 поверхностных белков EEV и IMV, большинство из которых в предыдущих исследованиях показали свою эффективность [15, 17, 19, 24, 26, 27]. Однако в нашем исследовании из 9 поверхностных антигенов только В5 и Н3 индуцировали иммунный ответ у мышей при системном и интраназальном введении. Мы предполагаем, что это может быть связано с тем, что оба белка B5 и H3 являются гликопротеинами и содержат эпитопы, которые распознаются клетками иммунной системы более эффективно, чем у белков других типов. По данным литературы, in silico предсказаны B- и Т-клеточные эпитопы для иммунодоминантных белков MPV (M1, H3, E8, A29, A35 и B6) [48].
В экспериментах по исследованию протективности rAd нами продемонстрирована эффективность интраназальной иммунизации. Интраназальная иммунизация rAd2-B5, экспрессирующим гликопротеин В5 EEV, обеспечила наилучшую защиту (100%) с наименьшей потерей веса и быстрым восстановлением. Интраназальная иммунизация rAd2-H3, экспрессирующим гликопротеин Н3 IMV, обеспечила 87,5% защиту. Другие поверхностные белки: EEV А33, IMV L1, D8 и D13 защищали животных от летальной инфекции на 75%. Введение rAd с антигенами IMV А17, А27 и А14 обеспечивало только частичную защиту от VACV на 25–50% в зависимости от антигена. Эффективность сочетанной иммунизации (внутримышечно + интраназально) rAd2-B5 или rAd2-H3 составила 100%. Полученные нами данные согласуются с результатами других исследований, в которых было показано, что для защиты от интраназального заражения наиболее важен специфический иммунитет к поверхностным антигенам EEV [49]. Антитела, специфические к B5, играют важную роль в борьбе с лёгочной или внутримозговой инфекцией [50]. Белок Н3 активирует дендритные клетки, что приводит к секреции таких цитокинов, как интерлейкины-12р70, -10, -6 и фактор некроза опухоли-α, что в дальнейшем индуцирует пролиферацию CD8+-Т-лимфоцитов, тем самым уничтожая инфицированные вирусом клетки [51].
Полученные результаты демонстрируют защитный потенциал выбранных антигенов и дают ценную информацию для последующей разработки эффективных и безопасных поливалентных вакцин против ОПВ. Наше исследование подтверждает, что B5 и Н3 обладают наибольшим защитным потенциалом, а в комбинации с другими поверхностными белками зрелого вириона могут обеспечить максимальную эффективность. Необходимо дальнейшее изучение иммуногенного и протективного потенциала различных комбинаций антигенов. Эта работа закладывает прочный фундамент для последующей оптимизации векторных вакцин, подтверждая целесообразность объединения различных поверхностных антигенов EEV и IMV, что позволит достичь максимальной защиты против ОПВ, включая вирус оспы обезьян.
Заключение
В данной работе создана панель rAd, несущих гены поверхностных белков вируса осповакцины, и проведена оценка их иммуногенности и эффективности. В ходе нашего исследования установлено, что на модели летальной инфекции, вызываемой VACV WR, гликопротеины B5 и Н3 демонстрируют наибольшую защиту при интраназальной иммунизации. Кроме того, сочетание с другими антигенами может не только усилить иммунный ответ, но и сформировать перекрёстный иммунитет к другим представителям рода Orthopoxvirus, вызывающим инфекции у людей. Эти результаты дают представление о защитном механизме поливалентных векторных вакцин и основу для дальнейшей разработки и внедрения таких препаратов, направленных на усиление защиты против ОПВ.
1 ICTV. Subfamily: Chordopoxvirinae. Genus: Orthopoxvirus. URL: https://ictv.global/report/chapter/poxviridae/poxviridae/orthopoxvirus
Об авторах
Денис Игоревич Зрелкин
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: aleza4striker@yandex.ru
ORCID iD: 0000-0003-0899-8357
м. н. с. лаб. иммунобиотехнологии
Россия, МоскваОльга Вадимовна Зубкова
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Автор, ответственный за переписку.
Email: olga-zubkova@yandex.ru
ORCID iD: 0000-0001-7893-8419
канд. биол. наук, в. н. с. лаб. иммунобиотехнологии
Россия, МоскваТатьяна Андреевна Ожаровская
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: t.ozh@yandex.ru
ORCID iD: 0000-0001-7147-1553
канд. биол. наук, с. н. с. лаб. иммунобиотехнологи
Россия, МоскваОльга Попова
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: olga.popova31@yandex.ru
ORCID iD: 0000-0003-3248-1227
м. н. с. лаб. иммунобиотехнологии
Россия, МоскваДарья Владимировна Воронина
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: daryavoronin2009@yandex.ru
ORCID iD: 0000-0001-6629-744X
м. н. с. лаб. иммунобиотехнологии
Россия, МоскваПолина Павловна Голдовская
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: goldovskaya00@mail.ru
ORCID iD: 0009-0000-1965-0482
лаборант-исследователь лаб. иммунобиотехнологии
Россия, МоскваИрина Викторовна Вавилова
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: vavilovairinav@yandex.ru
ORCID iD: 0009-0008-6272-0368
м. н. с. лаб. иммунобиотехнологии
Россия, МоскваАнастасия Сергеевна Чугунова
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: 170297_97@mail.ru
ORCID iD: 0009-0009-5964-6045
лаборант-исследователь лаб. иммунобиотехнологии
Россия, МоскваИнна Вадимовна Должикова
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: dolzhikova@gamaleya.org
ORCID iD: 0000-0003-2548-6142
канд. биол. наук, зав. лаб. государственной коллекции вирусов
Россия, МоскваДмитрий Николаевич Щербинин
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: dim284@inbox.ru
ORCID iD: 0000-0002-8518-1669
канд. биол. наук лаб. молекулярной биотехнологии
Россия, МоскваДмитрий Викторович Щебляков
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: sdmitriyv@mail.ru
ORCID iD: 0000-0002-1289-3411
канд. биол. наук, в. н. с., зав. лаб. иммунобиотехнологии
Россия, МоскваДенис Юрьевич Логунов
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: logunov@gamaleya.org
ORCID iD: 0000-0003-4035-6581
д-р биол. наук, академик РАН, зав. лаб. клеточной микробиологии
Россия, МоскваАлександр Леонидович Гинцбург
Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи
Email: gintsburg@gamaleya.org
ORCID iD: 0000-0003-1769-5059
д-р биол. наук, академик РАН, директор
Россия, МоскваСписок литературы
- Emerson G.L., Li Y., Frace M.A., et al. The phylogenetics and ecology of the orthopoxviruses endemic to North America. PLoS One. 2009;4(10):e7666. DOI: https://doi.org/10.1371/journal.pone.0007666
- McInnes C.J., Wood A.R., Thomas K., et al. Genomic characterization of a novel poxvirus contributing to the decline of the red squirrel (Sciurus vulgaris) in the UK. J. Gen. Virol. 2006;87(Pt. 8):2115–25. DOI: https://doi.org/10.1099/vir.0.81966-0
- Smits J.E., Tella J.L., Carrete M., et al. An epizootic of avian pox in endemic short-toed larks (Calandrella rufescens) and Berthelot’s pipits (Anthus berthelotti) in the Canary Islands, Spain. Vet. Pathol. 2005;42:59–65. DOI: https://doi.org/10.1354/vp.42-1-59
- Thiel T., Whiteman N.K., Tirapé A., et al. Characterization of canarypox-like viruses infecting endemic birds in the Galápagos islands. J. Wildl. Dis. 2005;41(2):342–53. DOI: https://doi.org/10.7589/0090-3558-41.2.342
- Voigt E.A., Kennedy R.B., Poland G.A. Defending against smallpox: a focus on vaccines. Expert Rev. Vaccines. 2016;15(9):1197–211. DOI: https://doi.org/10.1080/14760584.2016.1175305
- Henderson D.A. The eradication of smallpox – an overview of the past, present, and future. Vaccine. 2011;29(Suppl. 4):D7–9. DOI: https://doi.org/10.1016/j.vaccine.2011.06.080
- Nuzzo J.B., Borio L.L., Gostin L.O. The WHO declaration of monkeypox as a global public health emergency. JAMA. 2022; 328(7): 615–7. DOI: https://doi.org/10.1001/jama.2022.12513
- WHO. Executive board, 154th session. Provisional agenda item 18 "Smallpox eradication: destruction of variola virus stocks"; 2024.
- Rothenburg S., Yang Z., Beard P., et al. Monkeypox emergency: Urgent questions and perspectives. Cell. 2022;185(18):3279–81. DOI: https://doi.org/10.1016/j.cell.2022.08.002
- Zhang R.R., Wang Z.J., Zhu Y.L., et al. Rational development of multicomponent mRNA vaccine candidates against mpox. Emerg. Microbes Infect. 2023;12(1):2192815. DOI: https://doi.org/10.1080/22221751.2023.2192815
- Galinski M.S. Paramyxoviridae: transcription and replication. Adv. Virus Res. 1991;39:129–62. DOI: https://doi.org/10.1016/S0065-3527(08)60794-0
- Curran J., Kolakofsky D. Replication of paramyxoviruses. Adv. Virus Res. 1999;54:403–22. DOI: https://doi.org/10.1016/S0065-3527(08)60373-5
- Law M., Smith G.L. Antibody neutralization of the extracellular enveloped form of vaccinia virus. Virology. 2001;280(1):132–42. DOI: https://doi.org/10.1006/viro.2000.0750
- Riccardo V., Pablo G.C. Neutralization determinants on poxviruses. Viruses. 2023;15(12):2396. DOI: https://doi.org/10.3390/v15122396
- Moss B. Smallpox vaccines: targets of protective immunity. Immunol. Rev. 2011;239(1):8–26. DOI: https://doi.org/10.1111/j.1600-065X.2010.00975.x
- Lustig S., Fogg C., Whitbeck J.C., et al. Combinations of polyclonal or monoclonal antibodies to proteins of the outer membranes of the two infectious forms of vaccinia virus protect mice against a lethal respiratory challenge. J. Virol. 2005;79(21):13454–62. DOI: https://doi.org/10.1128/JVI.79.21.13454-13462.2005
- Mucker E.M., Golden J.W., Hammerbeck C.D., et al. A nucleic acid-based orthopoxvirus vaccine targeting the vaccinia virus L1, A27, B5, and A33 proteins protects rabbits against lethal rabbitpox virus aerosol challenge. J. Virol. 2022;96(3):e0150421. DOI: https://doi.org/10.1128/JVI.01504-21
- Gilchuk I., Gilchuk P., Sapparapu G., et al. Cross-neutralizing and protective human antibody specificities to poxvirus infections. Cell. 2016;167(3):684–94.e9. DOI: https://doi.org/10.1016/j.cell.2016.09.049
- Sakhatskyy P., Wang S., Chou T.W., Lu S. Immunogenicity and protection efficacy of monovalent and polyvalent poxvirus vaccines that include the D8 antigen. Virology. 2006;355(2):164–74. DOI: https://doi.org/10.1016/j.virol.2006.07.017.
- Niles E.G., Seto J. Vaccinia virus gene D8 encodes a virion transmembrane protein. J. Virol. 1988;62(10):3772–8. DOI: https://doi.org/10.1128/jvi.62.10.3772-3778.1988
- Takahashi T., Oie M., Ichihashi Y. N-terminal amino acid sequences of vaccinia virus structural proteins. Virology. 1994;202(2): 844–52. DOI: https://doi.org/10.1006/viro.1994.1406
- Chertov O.Yu., Telezhinskaya I.N., Zaitseva E.V., et al. Amino acid sequence determination of vaccinia virus immunodominant protein p35 and identification of the gene. Biomed. Sci. 1991;2(2):151–4.
- Franke C.A., Wilson E.M., Hruby D.E. Use of a cell-free system to identify the vaccinia virus L1R gene product as the major late myristylated virion protein M25. J. Virol. 1990;64(12):5988–96. DOI: https://doi.org/10.1128/jvi.64.12.5988-5996.1990
- Hooper J., Custer D., Thompson E. Four-gene-combination DNA vaccine protects mice against a lethal vaccinia virus challenge and elicits appropriate antibody responses in nonhuman primates. Virology. 2003;306(1):181–95. DOI: https://doi.org/10.1016/S0042-6822(02)00038-7
- Golden J.W., Zaitseva M., Kapnick S., et al. Polyclonal antibody cocktails generated using DNA vaccine technology protect in murine models of orthopoxvirus disease. Virol. J. 2011;8:441. DOI: https://doi.org/10.1186/1743-422X-8-441
- Berhanu A., Wilson R.L., Kirkwood-Watts D.L., et al. Vaccination of BALB/c mice with Escherichia coli-expressed vaccinia virus proteins A27L, B5R, and D8L protects mice from lethal vaccinia virus challenge. J. Virol. 2008;82(7):3517–29. DOI: https://doi.org/10.1128/JVI.01854-07
- Fogg C., Lustig S., Whitbeck J.C., et al. Protective immunity to vaccinia virus induced by vaccination with multiple recombinant outer membrane proteins of intracellular and extracellular virions. J. Virol. 2004;78(19):10230–7. DOI: https://doi.org/10.1128/JVI.78.19.10230-10237.2004
- Logunov D.Y., Dolzhikova I.V., Zubkova O.V., et al. Safety and immunogenicity of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine in two formulations: two open, non-randomised phase 1/2 studies from Russia. Lancet. 2020;396(10255):887–97. DOI: https://doi.org/10.1016/S0140-6736(20)31866-3
- Dolzhikova I.V., Zubkova O.V., Tukhvatulin A.I., et al. Safety and immunogenicity of GamEvac-Combi, a heterologous VSV- and Ad5-vectored Ebola vaccine: An open phase I/II trial in healthy adults in Russia. Hum. Vaccin. Immunother. 2017;13(3):613–20. DOI: https://doi.org/10.1080/21645515.2016.1238535
- Tukhvatulin A.I., Dolzhikova I.V., Shcheblyakov D.V., et al. An open, non-randomised, phase 1/2 trial on the safety, tolerability, and immunogenicity of single-dose vaccine «Sputnik Light» for prevention of coronavirus infection in healthy adults. Lancet Reg. Health Eur. 2021;11:100241. DOI: https://doi.org/10.1016/j.lanepe.2021.100241
- Yakimovich A., Mercer J. High-content analyses of vaccinia plaque formation. In: Mercer J., eds. Vaccinia Virus. Methods in Molecular Biology, Volume 2023. New York;2019:237–53. DOI: https://doi.org/10.1007/978-1-4939-9593-6_15
- Ожаровская Т.А., Попова О., Зубкова О.В. и др. Разработка и характеристика векторной системы на основе аденовируса обезьян 25-го серотипа. Вестник РГМУ. 2023;(1):4–11. DOI: https://doi.org/10.24075/vrgmu.2023.006 Ozharovskaia T.A., Popova O., Zubkova O.V., et al. Development and characterization of a vector system based on the simian adenovirus type 25. Bulletin of RSMU. 2023;(1):4–11. DOI: https://doi.org/10.24075/brsmu.2023.006
- Su Q., Sena-Esteves M., Gao G. Purification of the recombinant adenovirus by cesium chloride gradient centrifugation. Cold Spring Harb. Protoc. 2019;2019(5). DOI: https://doi.org/10.1101/pdb.prot095547
- Maizel J.V., White D.O., Scharff M.D. The polypeptides of adenovirus: I. Evidence for multiple protein components in the virion and a comparison of types 2, 7A, and 12. Virology. 1968;36(1):115–25. DOI: https://doi.org/10.1016/0042-6822(68)90121-9
- Shchelkunov S.N., Totmenin A.V., Safronov P.F., et al. Analysis of the monkeypox virus genome. Virology. 2002;297(2):172–94. DOI: https://doi.org/10.1006/viro.2002.1446
- Antoine G., Scheiflinger F., Dorner F., Falkner F.G. The complete genomic sequence of the modified vaccinia Ankara strain: comparison with other orthopoxviruses. Virology. 1998;244(2): 365–96. DOI: https://doi.org/10.1006/viro.1998.9123
- Diaz-Cánova D., Mavian C., Brinkmann A., et al. Genomic sequencing and phylogenomics of cowpox virus. Viruses. 2022;14(10):2134. DOI: https://doi.org/10.3390/v14102134
- Zrelkin D.I., Goldovskaia P.P., Kan V.Y. Determination of threshold value of protective level of antibodies to one of members of orthopoxvirus genus. In: Scientific Research of the SCO Countries: Synergy and Integration. Beijing;2024. DOI: https://doi.org/10.34660/INF.2024.87.21.085
- Максютов Р.A., Якубицкий С.Н., Колосова И.В., Щелкунов С.Н. Сравнение кандидатных вакцин нового поколения против ортопоксвирусных инфекций человека. Acta Naturae. 2017;9(2):93–99. Maksyutov R.A., Yakubitskyi S.N., Kolosova I.V., Shchelkunov S.N. Comparing new-generation candidate vaccines against human orthopoxvirus infections. Acta Naturae. 2017;9(2):88–93. DOI: https://doi.org/10.32607/20758251-2017-9-2-88-93 EDN: https://elibrary.ru/yyylkl
- Стовба Л.Ф., Чухраля О.В., Черникова Н.К. и др. Безопасность и иммуногенность вакцины третьего поколения IMVAMUNE® на основе вируса вакцины, штамм MVA. БИОпрепараты. Профилактика, диагностика, лечение. 2023;23(1):26–41. Stovba L.F., Chukhralya O.V., Chernikova N.K., et al. Safety and immunogenicity of IMVAMUNE®, a third-generation vaccine based on the modified vaccinia Ankara (MVA) strain. Biological Products. Prevention, Diagnosis, Treatment. 2023;23(1):26–41. DOI: https://doi.org/10.30895/2221-996X-2023-23-1-26-41 EDN: https://elibrary.ru/tjwrhx
- Щелкунов С.Н., Сергеев А.А., Титова К.А. и др. Увеличение протективности противооспенной вакцины. Медицинская иммунология. 2022;24(1):201–6. Shchelkunov S.N., Sergeev A.A., Titova K.A., et al. Increasing protectivity of the smallpox vaccine. Medical Immunology (Russia). 2022;24(1):201–6. DOI: https://doi.org/10.15789/1563-0625-IPO-2203 EDN: https://elibrary.ru/asgrmi
- Щелкунов С.Н., Якубицкий С.Н., Титова К.А. и др. Аттенуированный и высокоиммуногенный вариант вируса осповакцины. Acta Naturae. 2024;16(2):82–9. Shchelkunov S.N., Yakubitskiy S.N., Titova K.A., et al. An attenuated and highly immunogenic variant of the vaccinia virus. Acta Naturae. 2024;16(2):82–9. DOI: https://doi.org/10.32607/actanaturae.27384 EDN: https://elibrary.ru/kcsbnp
- Payne L.G., Kristensson K. Extracellular release of enveloped vaccinia virus from mouse nasal epithelial cells in vivo. J. Gen. Virol. 1985;66(Pt. 3):643–6. DOI: https://doi.org/10.1099/0022-1317-66-3-643
- Kenner J., Cameron F., Empig C., et al. LC16m8: аn attenuated smallpox vaccine. Vaccine. 2006;24(47-48):7009–22. DOI: https://doi.org/10.1016/j.vaccine.2006.03.087
- Gao J., Mese K., Bunz O., Ehrhardt A. State‐of‐the‐art human adenovirus vectorology for therapeutic approaches. FEBS Lett. 2019;593(24):3609–22. DOI: https://doi.org/10.1002/1873-3468.13691
- Hervouet C., Luci C., Bekri S., et al. Antigen-bearing dendritic cells from the sublingual mucosa recirculate to distant systemic lymphoid organs to prime mucosal CD8 T cells. Mucosal Immunol. 2014;7(2):280–91. DOI: https://doi.org/10.1038/mi.2013.45
- Holmgren J., Czerkinsky C. Mucosal immunity and vaccines. Nat. Med. 2005;11(4 Suppl.):S45–53. DOI: https://doi.org/10.1038/nm1213
- Wang Y., Yang K., Zhou H. Immunogenic proteins and potential delivery platforms for mpox virus vaccine development: а rapid review. Int. J. Biol. Macromol. 2023;245:125515. DOI: https://doi.org/10.1016/j.ijbiomac.2023.125515
- Kaufman D.R., Goudsmit J., Holterman L., et al. Differential antigen requirements for protection against systemic and intranasal vaccinia virus challenges in mice. J. Virol. 2008;82(14):6829–37. DOI: https://doi.org/10.1128/JVI.00353-08
- Agrawal S., Gupta S., Agrawal A. Vaccinia virus proteins activate human dendritic cells to induce T cell responses in vitro. Vaccine. 2009;27(1):88–92. DOI: https://doi.org/10.1016/j.vaccine.2008.10.031
- Monath T.P., Caldwell J.R., Mundt W., et al. ACAM2000 clonal Vero cell culture vaccinia virus (New York City Board of Health strain) — a second-generation smallpox vaccine for biological defense. Int. J. Infect. Dis. 2004;8(Suppl. 2):S31–44. DOI: https://doi.org/10.1016/j.ijid.2004.09.002
Дополнительные файлы