Заболеваемость хроническими вирусными гепатитами и анализ генетического разнообразия вирусов гепатитов В и С среди населения Хабаровска
- Авторы: Котова В.О.1, Базыкина Е.А.1, Балахонцева Л.А.1, Троценко О.Е.1, Кузнецова А.В.2
-
Учреждения:
- Хабаровский научно-исследовательский институт эпидемиологии и микробиологии
- Центр по профилактике и борьбе со СПИД и инфекционными заболеваниями
- Выпуск: Том 102, № 1 (2025)
- Страницы: 91-101
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://microbiol.crie.ru/jour/article/view/18640
- DOI: https://doi.org/10.36233/0372-9311-578
- EDN: https://elibrary.ru/zdffei
- ID: 18640
Цитировать
Аннотация
Введение. Изучение генотипического разнообразия вирусов гепатитов имеет большое значение при проведении анализа эпидемиологической обстановки на конкретной территории, позволяя отслеживать возможные пути передачи инфекции, появление и распространение новых вариантов вирусов.
Цель — оценить динамику заболеваемости хроническими формами вирусных гепатитов В (ХГВ) и С (ХГС) на территории Хабаровского края за 2013–2023 гг., провести анализ генетического разнообразия вирусов гепатитов В (HBV) и С (HCV), циркулирующих в Хабаровске.
Материалы и методы. Ретроспективный анализ заболеваемости ХГВ и ХГС по Хабаровскому краю проведён за 11 лет по данным отчётов Управления Роспотребнадзора по Хабаровскому краю. Выполнен серологический и молекулярно-генетический анализ 112 образцов плазмы крови пациентов с диагнозом «хронический вирусный гепатит», проживающих на территории Хабаровска.
Результаты. В Хабаровском крае с 2013 по 2023 г. заболеваемость ХГС снизилась с 50,0 до 44,6 случая на 100 тыс. населения, а ХГВ — с 10,2 до 8,2. ДНК HBV обнаружена в 21 из 36 образцов плазмы крови пациентов с выявленными серологическими маркерами HBV. Среди 17 исследованных образцов генотип D HBV обнаружен в 15 случаях, представленный субгенотипами D1 и D2, субтип А2 — в 2 образцах. Мутаций лекарственной устойчивости не обнаружено. РНК HCV выявлена в 54 из 78 проб плазмы крови с положительным результатом иммуноферментного анализа на наличие антител (IgG + IgM) к HCV. На территории Хабаровска установлена циркуляция субтипов HCV — 1b, 1а, 3а, 2а, 2с с преобладанием субтипа 1b.
Заключение. Заболеваемость ХГС и ХГВ в Хабаровском крае за 11-летний период наблюдения имела ярко выраженную тенденцию убыли. Результаты исследования дополняют существующие представления о циркуляции геновариантов HBV и HCV на территории России.
Ключевые слова
Полный текст
Введение
Проблема парентеральных вирусных гепатитов В и С остаётся одной из приоритетных задач мирового здравоохранения в связи с высокой частотой развития хронических форм болезни и возможностью формирования неблагоприятных исходов в виде цирроза печени и гепатоцеллюлярной карциномы. Согласно оценкам Всемирной организации здравоохранения (ВОЗ), в мире вирусом гепатита С (HCV) поражены 50 млн человек, количество инфицированных вирусом гепатита В (HBV) составляет 254 млн человек1. В апреле 2016 г. на Ассамблее ВОЗ было принято решение о глобальной ликвидации вирусных гепатитов как проблемы общественного здравоохранения к 2030 г.2
Реализация национального проекта «Здоровье» по вакцинопрофилактике гепатита В в России способствовала снижению заболеваемости острыми формами инфекции. За последние 10 лет (с 2014 по 2023 г.) заболеваемость острым гепатитом В снизилась в 4 раза — с 1,32 до 0,33 случая на 100 тыс. населения. С 2014 г. в России отмечается ежегодное снижение заболеваемости острым гепатитом С. В 2023 г. она составила 1393 больных, или 0,95 случая на 100 тыс. населения, что ниже среднемирового показателя на 27,5%, но при этом в сравнении с 2022 г. заболеваемость увеличилась на 26%. Наряду со снижением заболеваемости острыми формами гепатитов В и С на территории России продолжают регистрироваться высокие уровни новых случаев хронических форм вирусных гепатитов (ХВГ). Всего в 2023 г. зарегистрировано более 58,9 тыс. случаев ХВГ (в 2022 г. — 43,3 тыс. случаев). Показатели заболеваемости ХВГ резко отличаются по субъектам РФ (от 0,9 до 127,86 случая на 100 тыс. населения), что во многом зависит от качества проводимой диагностики и полноты регистрации данной группы заболеваний3. Подобная тенденция прослеживается и на территории Хабаровского края, входящего в состав Дальневосточного федерального округа4.
В последнее время большое внимание уделяется изучению генотипической вариабельности вирусов гепатитов. Заболевания, вызванные различными генотипами, могут значительно отличаться по клиническому течению и исходам [1–3].
В настоящее время идентифицированы 10 генотипов вируса гепатита В (HBV) (обозначаются буквами от А до J). Генотипы A–D, F, H и I делят на 35 субгенотипов (для остальных генотипов субтипы не установлены) [4, 5]. Генотипы отличаются длиной генома, размером открытого для чтения региона и трансляцией белка, а также развивающимися под влиянием терапии мутациями [6, 7]. Изоляты вируса гепатита С (HCV) подразделяют на 8 генотипов [8] и 93 подтверждённых субтипа. Современная классификация HCV включает 9 межгенотипных рекомбинантных форм5. Для каждого генотипа характерны определённая частота встречаемости и географическая зона распространения.
По результатам молекулярно-генетических исследований, проводимых в разные годы в России, установлено, что на территории страны циркулируют 3 генотипа HBV — D, А и С с доминированием генотипа D и 4 субтипа HCV — 1а, 1b, 2 и 3а, из которых субтипы 1b и 3а являются преобладающими [9–12].
Изучение генотипического разнообразия вирусных гепатитов имеет большое значение при проведении анализа эпидемиологической обстановки на каждой конкретной территории, позволяя отслеживать возможные пути передачи инфекции, появление и распространение новых вариантов вирусов, идентифицировать завозные случаи инфекции. Всё это является важным аспектом при своевременном планировании необходимых санитарно-эпидемиологических мероприятий.
Современные молекулярно-биологические методы исследования позволяют не только проводить оценку генетического разнообразия HBV и HCV на отдельных территориях, но и определять характер клинически значимых мутаций в P-гене ДНК HBV и регионах NS3/NS5A/NS5B HCV, ассоциированных с возможной резистентностью к терапии препаратами прямого противовирусного действия.
Цель исследования — оценить динамику заболеваемости ХГВ и ХГС за 2013–2023 гг., провести анализ генетического разнообразия HBV и HCV, циркулирующих среди пациентов Хабаровска с диагнозом «хронический вирусный гепатит».
Материалы и методы
Ретроспективный анализ заболеваемости ХГС и ХГВ проводили с использованием данных, предоставленных Управлением Роспотребнадзора по Хабаровскому краю, за период с 2013 по 2023 г. (11 лет). Значения заболеваемости ХВГ в России взяты из Государственного доклада «О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2023 г.».
Среднемноголетний темп прироста (ТСР) рассчитывали с использованием метода наименьших квадратов, доверительный интервал — методом углового преобразования Фишера. Полученную тенденцию расценивали:
- как стабильную при ТСР = ± 1%;
- слабо выраженную — при ТСР = ± 1,1–3,0%;
- умеренную — при ТСР = ± 3,1–5,0%;
- выраженную — при ТСР = ± 5,1–7,0%;
- ярко выраженную — при ТСР = ± 7% и выше [13].
С целью изучения генетического разнообразия HBV и HCV, циркулирующих среди населения Хабаровского края, исследованы образцы плазмы крови 112 пациентов с диагнозом «хронический вирусный гепатит», собранные на базе Центра по профилактике и борьбе со СПИД и инфекционными заболеваниями (n = 50) и лаборатории Хабаровского НИИ эпидемиологии и микробиологии (n = 62) в 2022–2023 гг. Исследование проводилось при добровольном информированном согласии пациентов или их законных представителей. Протокол исследования одобрен Комитетом по этике Хабаровского НИИ эпидемиологии и микробиологии (протокол № 9 от 01.11.2022). Наличие маркеров вирусных гепатитов В и С определяли методом иммуноферментного анализа с помощью тест-систем производства ЗАО «Вектор-Бест».
Нуклеиновые кислоты выделяли из 100 мкл плазмы крови с использованием комплекта реагента «АмплиПрайм РИБО-преп» (ЦНИИ Эпидемиологии Роспотребнадзора). Анализ на выявление ДНК HBV, РНК HCV, определение вирусной нагрузки в положительных пробах и генотипа HCV проводили методом полимеразной цепной реакции (ПЦР) с гибридизационно-флуоресцентной детекцией в режиме реального времени с применением коммерческих наборов: «АмплиСенс HBV-FL», «АмплиСенс HBV-Монитор-Fl», «АмплиСенс HСV-FL», «АмплиСенс HСV-Монитор-Fl», «АмплиСенс HСV-1/2/3» (ЦНИИ Эпидемиологии Роспотребнадзора) на приборе «Rotor Gene Q» («Qiagen»).
Для генотипирования HBV и HCV использовали метод двухступенчатой ПЦР со специфическими праймерами («Синтол») к консервативному участку перекрывающихся генов S и P, кодирующих поверхностный белок и ДНК-полимеразу HBV, и к NS5В-региону HCV [14, 15].
Дополнительно для пациентки с ХГС, получающей препараты прямого противовирусного действия, был проведён анализ нуклеотидной последовательности гена NS5 HCV, полученной по методике, описанной M. Rajhi и соавт. [16].
Фрагментное секвенирование по методу Сэнгера проводили при помощи набора реагентов «BigDye Terminator v3.1 Cycle Sequencing Kits» («Applied Biosystems/Life Technologies») на ДНК-анализаторе «ABI3500» («Applied Biosystems/Life Technologies»).
Выравнивание полученных нуклеотидных последовательностей осуществляли в программе «BioEdit v. 7.1.9».
Филогенетический анализ выполняли с помощью программы «MEGA v. 7.0» путём построения филогенетических деревьев методом ближайших соседей [17]. Нуклеотидные дистанции рассчитывали по методу Кимуры. Для оценки статистической достоверности филогенетических связей использовали bootstrap-анализ для 1000 независимых построений каждого филогенетического дерева.
В качестве референс-штаммов для проведения филогенетического анализа использовали последовательности той же области генома HBV и HСV из России и других стран мира, представленные в GenBank6.
Для выявления мутаций лекарственной устойчивости применяли программное обеспечение geno2pheno7.
В международную базу GenBank депонированы 14 полученных и проанализированных нуклеотидных последовательностей участков геномов HBV (№ PP100729–PP100742) и 44 участков геномов HСV (№ PP111728–PP111748, PP100743–PP100765). На российской платформе агрегации информации о геномах вирусов VGARus зарегистрированы 10 последовательностей участка генома HBV и 35 последовательностей участка генома HСV.
Результаты
Проведённые исследования показали, что заболеваемость ХГС в Хабаровском крае с 2013 по 2023 г. снизилась с 50,0 (95% ДИ 46,2–54,0) до 44,6 (95% ДИ 41,0–48,3) случая на 100 тыс. населения и имела выраженную тенденцию убыли (ТСР = –6,5%). Более значительные изменения регистрировались в Хабаровском крае в отношении заболеваемости ХГВ, которая имела ярко выраженную тенденцию убыли (ТСР = –11,6%), снизившись более чем в 2 раза — с 10,2 (95% ДИ 8,5–12,0) случая на 100 тыс. населения в 2013 г. до 4,5 (95% ДИ 3,4–5,7) случая на 100 тыс. населения в 2021 г.
В Хабаровске заболеваемость как ХГС, так и ХГВ на протяжении всего периода наблюдения была выше, чем в Хабаровском крае: в 2023 г. для ХГС — 56,7 (95% ДИ 50,9–62,8) случая на 100 тыс. населения (на 27,1% выше, чем в Хабаровском крае), для ХГВ — 13,3 (95% ДИ 10,6–16,3) случая на 100 тыс. населения (на 62,2% выше, чем в Хабаровском крае). В многолетней динамике заболеваемость ХГС и ХГВ в Хабаровске имела более выраженную, в сравнении с краевой, тенденцию убыли (ТСР = –11,6% — для заболеваемости ХГС и ТСР = –12,2% — для заболеваемости ХГВ) (рис. 1).
Рис. 1. Многолетняя заболеваемость ХГС и ХГВ в Хабаровском крае и Хабаровске.
Fig. 1. Long-term incidence of chronic viral hepatitis C and B in the Khabarovsk krai and Khabarovsk city.
Снижение заболеваемости ХВГ после 2019 г. совпало с началом пандемии COVID-19, во время которой вводились ограничительные мероприятия с целью снижения распространения SARS-CoV-2 среди населения. В 2022 и 2023 гг., когда ограничения были постепенно сняты, стал фиксироваться рост заболеваемости ХГС на 20,5 и 45,7% в Хабаровском крае и на 21,4 и 44,6% в Хабаровске соответственно. Заболеваемость ХГВ в Хабаровском крае и Хабаровске в 2022 г. увеличилась на 17,8 и 41,2% соответственно, а в 2023 г. — на 54,7 и 84,7%, что, вероятно, связано с увеличением числа обращений пациентов в медицинские организации, в том числе для проведения лабораторных исследований, достигнув уровня 2019 г.
Серологический и молекулярно-генетический анализ проведен для 112 образцов плазмы крови жителей Хабаровска с диагнозом «хронический вирусный гепатит». Возраст обследованных пациентов составил в среднем 51 год. Среди обследованных были 51 женщина (45,5%; 95% ДИ 36,9–55,2%) и 61 мужчина (54,5%; 95% ДИ 45,8–64,1%).
В результате проведённого исследования HBsAg был обнаружен в 36 из 112 образцов плазмы крови (32,1%; 95% ДИ 23,7–40,9%). Антитела к HCV обнаружены в 78 образцах (69,6%; 95% ДИ 61,2–78,1%). Микст-инфекцию ХГВ + ХГС имели 2 (1,8%; 95% ДИ 0,2–5,4%) пациента.
ДНК HBV выявлена в 21 (58,3%; 95% ДИ 41,7–73,4%) из 36 образцов плазмы крови пациентов с выявленными маркерами ХГВ. Во всех ДНК-положительных пробах был определён уровень вирусной нагрузки. У 19 (90,5%; 95% ДИ 74,0–98,8%) пациентов он был низкий (менее 104 МЕ/мл), у 2 (9,5%; 95% ДИ 1,2–26,0%) — средний (104–106 МЕ/мл).
При обследовании 78 пациентов из Хабаровска с положительным результатом иммуноферментного анализа на наличие антител (IgG + IgM) к HCV РНК вируса выявлена в 54 (69,2%; 95% ДИ 42,9–64,9%) образцах плазмы крови. Во всех РНК-положительных пробах определён уровень вирусной нагрузки. У 39 (72,2%; 95% ДИ 59,4–83,1%) пациентов он был низкий (менее 8 × 105 МЕ/мл), у 15 (27,8%; 95% ДИ 16,9–40,6%) — высокий (более 8 × 105 МЕ/мл). Предварительное генотипирование HCV, проведённое с использованием набора «АмплиСенс HСV-1/2/3», показало, что на территории Хабаровска среди обследованных пациентов наиболее распространён генотип 1 HCV, выявленный у 31 больного (57,4%; 95% ДИ 43,7–69,8%). Генотип 3 HCV обнаружен у 14 пациентов (25,9%; 95% ДИ 15,3–38,4%). В 8 случаях (14,8%; 95% ДИ 6,8–25,6%) выявлен генотип 2, у 1 пациента (1,9%; 95% ДИ 0,1–7,2%) генотип определить не удалось.
Для определения генотипа, выяснения происхождения и возможного родства вариантов HBV и HCV с изолятами из других регионов России и стран ближнего и дальнего зарубежья получены 17 нуклеотидных последовательностей участка генома HBV и 53 — участка NS5B HCV удовлетворительного качества, пригодные для проведения дальнейшего анализа.
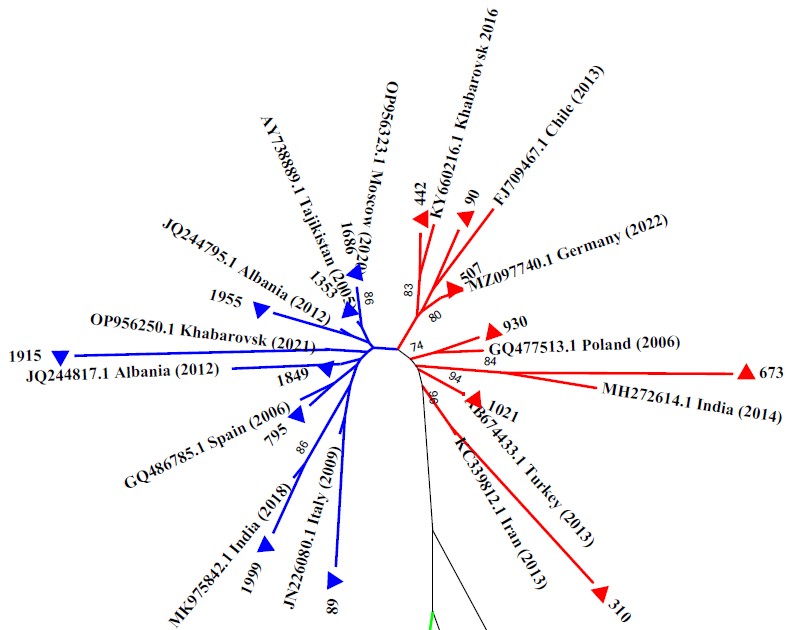
В результате молекулярно-генетического анализа HBV у 15 пациентов (88,2%; 95% ДИ 68,9–98,7%) определён генотип D, у 2 — генотип А (11,8%; 95% ДИ 1,3–31,1%). Филогенетические отношения между исследованными образцами и референсными последовательностями представлены на рис. 2.
Рис. 2. Результат филогенетического анализа нуклеотидных последовательностей фрагмента генома HBV, циркулирующего среди населения Хабаровска.
Филогенетическое дерево построено с помощью метода ближайших соседей. Последовательности HBV, изученные в данной работе, выделены треугольниками. Референс-последовательности HBV обозначены номерами GenBank. Указаны значения bootstrap-индекса, превышающие 70%. Синие линии — субтип D2; красные — субтип D1; зелёные — субтип А2.
Fig. 2. Results of phylogenetic analysis of partial genomic nucleotide sequences of HBV circulating among population of the Khabarovsk city.
Phylogenetic tree was constructed using the neighbor-joining method. HBV sequences evaluated in current work are marked with triangles. HBV reference sequences are specified by their GenBank accession numbers. Bootstrap index values exceeding 70% are indicated. Blue lines — sub-genotype D2; red lines — sub-genotype D1; green lines — sub-genotype A2.
На филограмме штаммы HBV генотипа D, полученные нами, и нуклеотидные последовательности штаммов, взятые из GenBank, разделились на две отдельные монофилетические группы, различающиеся по субтипам: D1 и D2, которые были определены в 7 (46,7%) и 8 (53,3%) образцах соответственно.
Полученные нуклеотидные последовательности (№ 442, 507, 90) сгруппировались с генетически близкими последовательностями субтипа D1 из Чили (FJ709467.1), Германии (MZ0977440.1), а также со штаммом (KY660216.1), который уже был зафиксирован на территории Хабаровского края в 2016 г. Четыре образца (№ 930, 673, 1021, 310) образовали отдельные клады со штаммами субтипа D1 из Польши (GQ477513.1), Индии (MH272614.1), Турции (AB674433.1) и Ирана (КС339812.1).
Полученные нуклеотидные последовательности субтипа D2 распределились между штаммами HBV данного субгенотипа, выявленными в России (в Москве — ОР956323.1 и Хабаровске — ОР956250.1), и штаммами из Индии (MK975842.1), Италии (JN226080.1), Испании (GQ486785.1), Албании (JQ244817.1, JQ244795.1), Ирана (KC339865.1), Таджикистана (AY738889).
Два штамма, выделенные на территории Хабаровска (образцы № 1125, 1877), сгруппировались на филогенетическом дереве, образуя один общий кластер с референс-штаммами субтипа А2. При этом образец № 1877 обладал большим генетическим сходством с штаммом HBVсубгенотипа А2, серотипа adw2 из Кубы (KM606811.1), а образец № 1125 — со штаммом из Польши (GQ477462.1).
Нуклеотидные последовательности участка Р-гена HBV, полученные в ходе настоящего исследования, были протестированы на наличие основных мутаций, ассоциированных с возникновением лекарственной устойчивости. Проведённый анализ показал, что все 17 штаммов HBV чувствительны к следующим противовирусным препаратам: ламивудину, адефовиру, энтекавиру, телбивудину, тенофовиру, т. е. мутаций устойчивости не обнаружено.
Филогенетические отношения между нуклеотидными последовательностями, полученными в результате прямого секвенирования NS5B области генома HCV, и референсными последовательностями отображены на рис. 3.
Рис. 3. Результат филогенетического анализа нуклеотидных последовательностей области NS5B генома HCV, циркулирующего среди населения Хабаровска.
Филогенетическое дерево построено с помощью метода ближайших соседей. Последовательности HBV, изученные в данной работе, выделены треугольниками. Референс-последовательности HBV обозначены номерами GenBank. Указаны значения bootstrap-индекса, превышающие 70%. Синие линии — субтип 3a; красные — субтип 1b; зелёные — субтип 2a; чёрные — субтип 1а; сиреневые — субтип 2с.
Fig. 3. Result of phylogenetic analysis of NS5B region nucleotide sequences of HCV circulating among population of the Khabarovsk city.
Phylogenetic tree was constructed using the neighbor-joining method. HCV sequences evaluated in current work are marked with triangles. HCV reference sequences are specified by their GenBank accession numbers. Bootstrap index values exceeding 70% are indicated. Blue lines — subtype 3a; red lines — subtype 1b; green lines — subtype 2a; black lines — subtype 1a; violet lines — subtype 2c.
Образец № 57, для которого при предварительном генотипировании с использованием диагностической тест-системы «АмплиСенс HСV-1/2/3» не был получен результат, образовал единый кластер с изолятами, принадлежавшими субтипу 1а и выделенными в разные годы в США (KT734609.1, OK392383), где данный геновариант является эндемичным, а также в Швеции (MH510449.1), на Украине (OQ979420), в Швейцарии (EU255927.1), Нидерландах (KU563369.1), но при этом близкородственных штаммов для него не выявлено.
На филогенетическом дереве 31 из 54 исследуемых штаммов равномерно распределились между референсными последовательностями HСV субтипа 1b, представленными в международной базе данных GenBank (Греция, Франция, США, Бельгия, Испания, Тайвань, Япония, Вьетнам, Бразилия, Индонезия, Тунис). Филогенетический анализ 13 образцов, отнесённых по результатам ПЦР-генотипирования к генотипу 3, показал, что все полученные нами нуклеотидные последовательности кластеризуются на одной ветви филогенетического дерева с ранее полученными последовательностями той же области генома вариантов субтипа 3а, выделенных в разные годы в различных регионах России и мира.
Филогенетический анализ 8 образцов, отнесённых по результатам предварительного генотипирования к генотипу 2, выявил формирование 2 кластеров. Один образец (№ 81) с высоким уровнем bootstrap-поддержки (100%) образовал единый кластер с изолятами, принадлежавшими субтипу 2с, но при этом близкородственных штаммов для него не выявлено. Семь штаммов сгруппировались на филогенетическом дереве, образуя один общий кластер с изолятами HCV субтипа 2а, зарегистрированными в GenBank, которые были выделены на территории России — в Новосибирской области в 2002 г. (GQ388000.1), Республике Саха (Якутия) (КТ 378626.1) в 2014 г., Ленинградской области (AF388438.1) в 2014 г., а также во Франции (MG453401.1) в 2014 г.
Для образца № 76 от пациентки с ХГС, получающей препараты прямого противовирусного действия, дополнительно был проведён анализ нуклеотидной последовательности гена NS5AHCV на наличие мутаций, ассоциированных с возникновением лекарственной устойчивости. В результате исследования была выявлена мутация Y93H, обусловливающая резистентность вируса к следующим препаратам: Daclatasvir, который входил в схему лечения пациентки, а также к Elbasvir, Ledipasvir, Ombitasvir, Velpatasvir. При анализе нуклеотидной последовательности региона NS5B мутаций лекарственной устойчивости в данном образце не обнаружено.
Обсуждение
Современная эпидемиологическая ситуация по вирусному гепатиту как в Хабаровском крае, так и в среднем по России характеризуется увеличением среди населения общего числа больных с хроническими формами. В целом по Хабаровскому краю за 2013–2023 г. кривые заболеваемости населения ХГС и ХГВ имели однонаправленные тенденции к снижению8. Несмотря на это, уровень заболеваемости ХГС в Хабаровском крае, достигший 44,6 случая на 100 тыс. населения в 2023 г., превысил среднероссийский, составлявший 31,6 случая на 100 тыс. населения. В то же время показатель заболеваемости населения Хабаровского края ХГВ оказался несколько ниже среднероссийского уровня — 8,2 и 8,4 случая на 100 тыс. населения соответственно.
Следует отметить, что резкое снижение заболеваемости ХГС и ХГВ, зафиксированное в 2020 г., в том числе для ХГС — в 1,7 раза с 43,0 (95% ДИ 39,5–46,6) до 24,8 (95% ДИ 22,2–27,8) и для ХГВ — почти в 2 раза с 9,8 (95% ДИ 8,2–11,6) до 5,0 (95% ДИ 3,8–6,3) случая на 100 тыс. населения, отчасти объясняется уменьшением обращаемости населения за медицинской помощью в период пандемии COVID-19.
На протяжении многих лет значительный вклад в развитие эпидемического процесса ХВГ в регионе оказывает наиболее крупный населённый пункт — г. Хабаровск, являющийся столицей края, где в 2023 г. проживало 61,1% (95% ДИ 57,1–65,1%) пациентов с ХГС и 78,1% (95% ДИ 69,7–85,4%) пациентов с ХГВ от всех случаев с впервые выявленной инфекцией в субъекте. Более высокую заболеваемость ХГС в краевой столице отчасти можно связать с большей доступностью лабораторного освидетельствования, в отличие от удалённых от краевого центра северо-восточных территорий, где регистрация заболеваемости ХВГ отсутствует либо является спорадической, например, в районе Полины Осипенко, Николаевском, Охотском, Тугуро-Чумиканском и Аяно-Майском районах.
В ходе молекулярно-генетического исследования установлены генотипы и субгенотипы HBV и HCV, циркулирующие среди больных хроническими формами инфекции в Хабаровске.
Результаты филогенетического анализа субтипов D1 и D2 из Хабаровска и базы данных GenBank показали формирование нескольких кластеров, что может свидетельствовать о разном происхождении и независимом распространении штаммов HBV, циркулирующих на исследуемой территории. Низкое сходство изученных нами штаммов со штаммами из России, возможно, обусловлено невысокой долей российских вариантов вируса, представленных в международной базе данных GenBank.
В ходе исследования были выявлены некоторые различия в распространении генетических вариантов HBV и HCV, отмеченных в данной работе среди жителей Хабаровска, и исследовании, проведённом нами в 2017–2018 гг. среди коренного населения Нанайского района Хабаровского края [18, 19]. Так, анализ частоты встречаемости подгенотипов D1, D2 и D3 HBV показал, что среди пациентов сельского района незначительно преобладал субгенотип D3 (51,3%; 95% ДИ 35,8–66,7%), а субгенотипы D2 и D1 были определены в 46,1% (95% ДИ 30,9–61,7%) и 2,6% случаях, соответственно. Необходимо отметить, что в настоящем исследовании среди городских пациентов не было выявлено ни одного случая инфицирования субгенотипом D3, что опровергает результаты описанных ранее исследований, согласно которым частота встречаемости субгенотипа D1 убывает с 45% в европейской части России до 12% в Дальневосточном регионе [20]. Отчасти это можно объяснить небольшой выборкой исследуемых образцов. Данный факт требует дальнейшего изучения.
Результаты настоящего исследования показали, что на территории Хабаровска среди обследованных пациентов наиболее распространён субвариант 1b HCV, выявленный по результатам филогенетического анализа в 58,5% случаев, в то время как на территории Нанайского района Хабаровского края зафиксировано преобладание субтипа 3а (45,0%).
Филогенетический анализ, проведённый по NS5В-региону HCV 53 исследованных образцов крови жителей Хабаровска, первоначально протипированных в ПЦР, представил следующее соотношение субтипов: 1в — 31 (58,5%; 95% ДИ 45,2–71,4%), 3а — 13 (24,5%; 95% ДИ 14,0–37,0%), 2а — 7 (13,2%; ДИ 5,5–23,5%), в единичных случаях выявлены субтипы 1а и 2с (1,9%). По итогам филогенетического анализа изолят № 57, нетипируемый обычным методом ПЦР, удалось отнести к субтипу1а.
В целом полученные данные о циркуляции геновариантов HBV и HCV среди жителей Хабаровска согласуются с данными других исследователей о доминировании на территории России генотипа D HBV и субтипов 1b и 3а HCV.
Следует отметить важность регулярного пополнения информации о генотипах/субтипах вирусов гепатитов, выявленных в субъектах РФ, в международной (GenBank) и российской (VGARus) базах данных. Это значительно расширит возможности для молекулярно-генетического мониторинга за циркулирующими генетическими вариантами вирусов на конкретной территории, а также для проведения анализа заболеваемости этими инфекциями в целом по России, что в конечном итоге может усилить действенность эпидемиологического надзора за вирусными гепатитами. Кроме того, благодаря использованию современных молекулярно-биологических методов диагностики и проведению филогенетического анализа, стало возможным прогнозировать развитие неблагополучных тенденций в эпидемиологической ситуации, а также подтвердить или опровергнуть наличие эпидемиологической связи между предполагаемым источником HCV или HBV и заболевшими при расследовании факта внутрисемейного инфицирования, групповых заболеваний, случаев внутрибольничного инфицирования или профессионального заражения вирусным гепатитом.
Заключение
Несмотря на снижение в Хабаровском крае случаев выявления острых форм парентеральных вирусных гепатитов, регистрация ХВГ остается на высоком уровне. Наиболее неблагоприятная ситуация с заболеваемостью ХГВ и ХГС в Хабаровском крае наблюдается в Хабаровске.
В результате изучения генетического разнообразия вирусов HBV и HСV на территории Хабаровска выявлена циркуляция двух генотипов HBV: D и А. Среди исследованных образцов генотип D HBV обнаружен в 88,2% случаев и представлен субгенотипами D1 и D2. На долю субтипа А пришлось 11,8%. Молекулярно-генетическое исследование HСV, циркулирующего на территории Хабаровска, выявило циркуляцию субтипов 1b, 1а, 3а, 2а, 2с с преобладанием субтипа 1b.
При анализе нуклеотидных последовательностей участка гена Р HBV основных мутаций лекарственной устойчивости к противовирусным препаратам не обнаружено.
1 World Health Organization. Hepatitis B, Fact Sheet. URL: https://www.who.int/news-room/fact-sheets/detail/hepatitis-b (дата обращения: 07.05.2024); World Health Organization. Hepatitis C, Fact Sheet. URL: https://www.who.int/news-room/fact-sheets/detail/hepatitis-c (дата обращения: 07.05.2024).
2 World Health Organization. Sixty-ninth world health assembly provisional agenda item 15.1. Draft global health sector strategies. Viral hepatitis, 2016–2021. URL: http://apps.who.int/gb/ebwha/pdf_files/WHA69/A69_32-en.pdf?ua=1 (дата обращения: 07.05.2024).
3 Государственный доклад «О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2022 году». М.; 2023. URL: https://clck.ru/3FcJ5X
4 Доклад Управления Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека по Хабаровскому краю «О состоянии санитарно-эпидемиологического благополучия населения в Хабаровском крае в 2022 году». URL: https://clck.ru/3FcHrj
5 International Committee on Taxonomy of Viruses (ICTV), 2022
URL: https://talk.ictvonline.org/ictv_wikis/flaviviridae/w/sg_flavi/56/hcv-classification (дата обращения: 15.05.2024).
6 URL: https://www.ncbi.nlm.nih.gov/genbank
7 URL: http://hbv.geno2pheno.org/index.php
8 Доклад Управления Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека по Хабаровскому краю «О состоянии санитарно-эпидемиологического благополучия населения в Хабаровском крае в 2022 году». URL: https://clck.ru/3FcHrj
Об авторах
Валерия Олеговна Котова
Хабаровский научно-исследовательский институт эпидемиологии и микробиологии
Автор, ответственный за переписку.
Email: kotova.valeriya@mail.ru
ORCID iD: 0000-0001-9824-7025
с. н. с., зав. лаб. эпидемиологии и профилактики вирусных гепатитов и СПИДа
Россия, ХабаровскЕлена Анатольевна Базыкина
Хабаровский научно-исследовательский институт эпидемиологии и микробиологии
Email: alyonaf@yandex.ru
ORCID iD: 0000-0002-5695-6752
м. н. с. лаб. эпидемиологии и профилактики вирусных гепатитов и СПИДа
Россия, ХабаровскЛюдмила Анатольевна Балахонцева
Хабаровский научно-исследовательский институт эпидемиологии и микробиологии
Email: adm@hniiem.ru
ORCID iD: 0000-0002-3209-7623
руководитель Дальневосточного окружного Центра по профилактике и борьбе со СПИД
Россия, ХабаровскОльга Евгеньевна Троценко
Хабаровский научно-исследовательский институт эпидемиологии и микробиологии
Email: trotsenko_oe@hniiem.ru
ORCID iD: 0000-0003-3050-4472
д-р мед. наук, директор
Россия, ХабаровскАнна Валерьевна Кузнецова
Центр по профилактике и борьбе со СПИД и инфекционными заболеваниями
Email: cpbsiz.khv@mail.ru
ORCID iD: 0000-0003-3729-4092
канд. мед. наук, главный врач
Россия, ХабаровскСписок литературы
- Sunbul M. Hepatitis B virus genotypes: global distribution and clinical importance. World J. Gastroenterol. 2014;20(18): 5427–34. DOI: https://doi.org/10.3748/wjg.v20.i18.5427
- Kmet Lunacek N., Poljak M., Meglic-Volkar J., et al. Epidemiological, virological and clinical characteristics of hepatitis B virus genotypes in chronically infected persons in Slovenia. Hepat. Mon. 2017;17(3):e43838. DOI: https://doi.org/10.5812/hepatmon.43838
- Martinez M.A., Franco S. Therapy implications of hepatitis C virus genetic diversity. Viruses. 2020;13(1):41. DOI: https://doi.org/10.3390/v13010041
- Kramvis A. Genotypes and genetic variability of hepatitis B virus. Intervirology. 2014;57(3-4):141–50. DOI: https://doi.org/10.1159/000360947
- Lin C.L., Kao J.H. Hepatitis B virus genotypes and variants. Cold Spring Harb. Perspect. Med. 2015;5(5):a021436. DOI: https://doi.org/10.1101/cshperspect.a021436
- Kramvis A., Kew M., François G. Hepatitis B virus genotypes. Vaccine. 2005;23(19):2409–23. DOI: https://doi.org/10.1016/j.vaccine.2004.10.045
- Kramvis A., Kew M.C. Relationship of genotypes of hepatitis B virus to mutations, disease progression and response to antiviral therapy. J. Viral. Hepat. 2005;12(5):456–64. DOI: https://doi.org/10.1111/j.1365-2893.2005.00624.x
- Borgia S.M., Hedskog C., Parhy B., et al. Identification of a novel hepatitis C virus genotype from Punjab, India: expanding classification of hepatitis C virus into 8 genotypes. J. Infect Dis. 2018;218(11):1722–9. DOI: https://doi.org/10.1093/infdis/jiy401
- Герасимова В.В., Левакова И.А., Бичурина М.А., Максимова Н.Р. Молекулярно-эпидемиологические особенности вирусного гепатита В. Инфекция и иммунитет. 2015;5(4):297–302. Gerasimova V.V., Levakova I.A., Bichurina M.A., Maksimova N.R. Molecular-epidemiological features of hepatitis B virus. Russian Journal of Infection and Immunity. 2015;5(4):297–302. EDN: https://elibrary.ru/vizekb
- Кашникова А.Д., Быстрова Т.Н., Полянина А.В., Залесских А.А. Молекулярно-генетический мониторинг как компонент эпидемиологического надзора за гепатитом С. Здоровье населения и среда обитания — ЗНиСО. 2022;30(11):76–81. Kashnikova A.D., Bystrova T.N., Polyanina A.V., Zalesskikh A.A. Genetic monitoring as a component of hepatitis C surveillance. Public Health and Life Environment — PH&LE. 2022;30(11):76–81. DOI: https://doi.org/10.35627/2219-5238/2022-30-11-76-81 EDN: https://elibrary.ru/kmaums
- Хорькова Е.В., Лялина Л.В., Микаилова О.М. и др. Актуальные вопросы эпидемиологического надзора за хроническими вирусными гепатитами B, C, D и гепатоцеллюлярной карциномой на региональном уровне. Здоровье населения и среда обитания — ЗНиСО. 2021;29(8):76–84. Khorkova E.V., Lyalina L.V., Mikailova O.M., et al. Current issues of epidemiological surveillance of chronic viral hepatitis B, C, D and hepatocellular carcinoma at the regional level. Public Health and Life Environment — PH&LE. 2021;29(8):76–84. DOI: https://doi.org/10.35627/2219-5238/2021-29-8-76-84 EDN: https://elibrary.ru/mhcuqj
- Соболева Н.В., Карлсен А.А., Кожанова Т.В. и др. Распространенность вируса гепатита С среди условно здорового населения Российской Федерации. Журнал инфектологии. 2017;9(2):56–64. Soboleva N.V., Karlsen A.A., Kozhanova T.V., et al. The prevalence of the hepatitis c virus among the conditionally healthy population of the Russian Federation. Journal Infectology. 2017;9(2):56–64. DOI: https://doi.org/10.22625/2072-6732-2017-9-2-56-64 EDN: https://elibrary.ru/yskwxr
- Колпаков С.Л. Методология изучения эпидемического процесса статистическими и аналитическими методами. Владивосток;2023. Kolpakov S.L. Methodology of Epidemic Process Evaluation Using Statistical and Analytical Methods. Vladivostok;2023. EDN: https://elibrary.ru/fvbtsb
- Кюрегян К.К., Михайлов М.И. Молекулярно-биологические основы контроля вирусных гепатитов. М.;2013. Kyuregyan K.K., Mikhailov M.I. Molecular Biological Basis of Viral Hepatitis Control. Моscow;2013. EDN: https://elibrary.ru/duejiv
- Rajhi M., Ghedira K., Chouikha A., et al. Phylogenetic analysis and epidemic history of hepatitis C virus genotype 2 in Tunisia, North Africa. PLoS One. 2016;11(4):e0153761. DOI: https://doi.org/10.1371/journal.pone.0153761
- Кичатова В.С., Карлсен А.А., Исаева О.В. и др. Лекарственно-резистентные варианты ВГС субтипа 1в, циркулирующие на территории Российской Федерации: анализ аминокислотных мутаций в белках NS5A и Core. Журнал инфектологии. 2018;10(4):30–6. Kichatova V.S., Karlsen A.A., Isaeva O.V., et al. Drug resistant variants of hepatitis c virus genotype 1B in Russia: analysis of amino acid substitutions in NS5A and core proteins. Journal Infectology. 2018;10(4):30–6. DOI: https://doi.org/10.22625/2072-6732-2018-10-4-30-36 EDN: https://elibrary.ru/vvmeki
- Tamura K., Stecher G., Peterson D., et al. MEGA6: Molecular Evolutionary Genetics Analysis version 6.0. Mol. Biol. Evol. 2013; 30(12):2725–9. DOI: https://doi.org/10.1093/molbev/mst197
- Котова В.О., Балахонцева Л.А., Базыкина Е.А. и др. Молекулярно-генетическая характеристика хронического вирусного гепатита В среди пациентов Нанайского района Хабаровского края. Дальневосточный журнал инфекционной патологии. 2018;(35):15–21. Kotova V.O., Bakakhontseva L.A., Bazykina E.A., et al. Molecular-genetic characteristics of chronic viral hepatitis B in patients of the Nanaysky district of the Khabarovsk region. Far Eastern Journal of Infectious Pathology. 2018;(35):15–21. EDN: https://elibrary.ru/yqxrwp
- Котова В.О., Балахонцева Л.А., Базыкина Е.А. и др. Генетическое разнообразие вируса гепатита С среди населения Нанайского района Хабаровского края. Инфекция и иммунитет. 2021;11(1):148–56. Kotova V.O., Balakhontseva L.A., Bazykina E.A., et al. Genetic diversity of hepatitis c virus in Nanaian region, Khabarovsk territory. Russian Journal of Infection and Immunity. 2021;11(1):148–56. DOI: https://doi.org/10.15789/2220-7619-GDO-1265 EDN: https://elibrary.ru/enfery
- Чуланов В.П., Неверов А.Д., Карандашова И.В. и др. Молекулярно-генетические исследования в эпидемиологии вирусных гепатитов: достижения и перспективы. Эпидемиология и инфекционные болезни. Актуальные вопросы. 2014;(2):28–34. Chulanov V.P., Neverov A.D., Karandashova I.V., et al. Molecular genetic studies in the epidemiology of viral hepatitis: progress and prospects. Epidemiology and Infectious Diseases. Current Items. 2014;(2):28–34. EDN: https://elibrary.ru/rzaabv
Дополнительные файлы