Молекулярно-генетические детерминанты вирулентности Streptococcus agalactiae, выделенных у беременных и новорождённых Санкт-Петербурга и Ленинградской области в 2010–2023 годах
- Авторы: Шалепо К.В.1, Хуснутдинова Т.А.1, Будиловская О.В.1, Крысанова А.А.1, Сапожников К.В.1, Савичева А.М.1, Коган И.Ю.1
-
Учреждения:
- Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта
- Выпуск: Том 101, № 2 (2024)
- Страницы: 217-226
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://microbiol.crie.ru/jour/article/view/18582
- DOI: https://doi.org/10.36233/0372-9311-501
- EDN: https://elibrary.ru/qnunfe
- ID: 18582
Цитировать
Аннотация
Введение. Колонизация репродуктивных органов беременных стрептококками группы В (СГВ; Streptococcus agalactiae) может приводить к тяжёлой перинатальной и неонатальной патологии. В современных условиях требуется не только антибактериальная профилактика антенатального инфицирования плода в родах, но и вакцинопрофилактика. Изучение молекулярно-генетических детерминант вирулентности циркулирующих штаммов СГВ в популяции необходимо для понимания эпидемиологии СГВ-инфекций и разработки альтернативных подходов к их профилактике
Цель: определение молекулярно-генетических детерминант вирулентности Streptococcus agalactiae, выделенных у беременных и новорождённых, и мониторинг типов капсульных полисахаридов и профилей пилей клинических изолятов СГВ.
Материалы и методы. В исследование были включены клинические изоляты СГВ (n = 420), выделенные у беременных и новорождённых в 2010–2023 гг. Для выделения S. agalactiae использовали бактериологический метод; тип капсульных полисахаридов, пилей, принадлежность штаммов к гипервирулентному сиквенс-типу ST-17 определяли методом полимеразной цепной реакции.
Результаты. В течение 13 лет наблюдения отмечено доминирование Iа, III и V генотипов капсульных полисахаридов СГВ как у беременных, так и у новорождённых. Частота встречаемости Ib генотипа увеличилась с 0,7 до 6,7%, V генотипа — с 12,1 до 24,4%, а распространённость III генотипа значимо снизилась — с 41,1 до 21,1%. У 6 беременных и 2 новорождённых был обнаружен гипервирулентный сиквенс-тип ST-17. Однако признаков неонатальной инфекции у этих детей не было. Более половины всех клинических изолятов S. agalactiae имели пили генотипов PI-1 + PI-2a, PI-2a и PI-1 + PI-2b. Распределение типов пилей не изменилось за весь период наблюдения.
Заключение. Мониторинг генотипов капсульных полисахаридов и пилей СГВ необходим для разработки эффективных профилактических вакцин.
Полный текст
Введение
Стрептококки группы В (СГВ), единственным представителем которых являются Streptococcus agalactiae, — грамположительные кокки, образующие короткие цепочки, факультативные анаэробы, способные проявлять β-гемолитическую активность. Обычно являются комменсальными организмами и колонизируют желудочно-кишечный тракт и нижний репродуктивный тракт примерно у 20–30% женщин [1]. В России этот показатель достигает 16,3% [2].
При колонизации СГВ обычно симптомы отсутствуют. Однако СГВ у взрослых могут провоцировать пиелонефрит, артрит, развитие абсцессов, мастит, эндокардит, септицемию и др. S. agalactiae являются распространённой причиной воспалительных заболеваний урогенитального тракта женщин и основным этиологическим агентом инфекций раннего неонатального периода. Наибольшую актуальность они приобретают в этиологии перинатальных инфекций, т.к. могут вызывать инфекции мочеполовых путей, преждевременные роды, мертворождение, хориоамнионит, послеродовый сепсис и ряд неблагоприятных исходов для матери и ребёнка: неонатальный сепсис, менингит или пневмонию. Чаще всего инфицирование плода происходит внутриутробно, когда СГВ восходящим путем попадают из влагалища в амниотическую жидкость, но возможно инфицирование во время прохождения плода через родовые пути матери (интранатально).
Инфекции новорождённых, вызванные СГВ, клинически подразделяются на ранние, развившиеся в сроки до 6-го дня жизни ребёнка, и поздние, развившиеся через 7–89 дней после рождения [3].
Сложный патогенез заболевания у матери и ребёнка, ассоциированного с S. аgalactiae, связан с большим арсеналом факторов вирулентности этого микроорганизма, который может широко варьировать от бессимптомного носительства до развития инвазивной инфекции.
В патогенез СГВ-инфекции вносят вклад более 20 различных факторов вирулентности микроорганизма. К ним относятся адгезины, ферменты и другие белки, которые могут широко варьировать в зависимости от штамма микроба. Важную роль в прикреплении микроорганизма к клетке хозяина играют молекулы клеточной адгезии. Специфические адгезины опосредуют колонизацию S. agalactiae к различным рецепторам, присутствующим на поверхности эпителия слизистых оболочек, обеспечивая его передачу новорождённым при их прохождении через родовые пути матери. Эти белки необходимы микроорганизму на начальном этапе колонизации и способствуют инвазии в эпителиальные и эндотелиальные клетки хозяина, а также принимают участие в образовании биоплёнок. Пили являются важным фактором вирулентности и патогенности СГВ и представляют собой длинные нитевидные белковые структуры, состоящие из ковалентно связанных белковых субъединиц, прикрепленные к клеточной стенке, выступающие за пределы капсулы, которая покрывает бактериальную поверхность [4].
Многие факторы вирулентности СГВ влияют на способность каждого штамма колонизировать определённый биотоп или вызывать развитие тяжёлого заболевания. Одним из ключевых факторов вирулентности является капсульный полисахарид СГВ (CPS), впервые выявленный доктором Ребеккой Лансфилд в 1930-х гг. На сегодняшний день известно 10 уникальных серотипов CPS (Ia, Ib, II–IX) [1, 5], при этом на 6 из них (Ia, Ib, II–V) во всём мире приходится 98% [1].
Существует несколько подходов для определения серотипов S. agalactiae. Тест на преципитацию по Лансфилд (метод латекс-агглютинации) считается стандартным методом определения серотипов СГВ. К молекулярно-биологическим методам, основанным на анализе ДНК, относят генотипирование СГВ на основе ПЦР в реальном времени, мультиплексный ПЦР-анализ для прямой идентификации капсульного типа (от Ia до IX) S. agalactiae и полногеномное секвенирование. Серотипирование изолятов СГВ важно для понимания локальной эпидемиологии и мониторинга изменения генотипа CPS.
Помимо различия серотипов, СГВ также можно кластеризовать генетически с помощью мультилокусного типирования последовательностей. Это осуществляется путём секвенирования 7 генов «домашнего хозяйства» для любого штамма СГВ, и комбинация этих 7 геномных локусов создаёт тип последовательности (sequence type — ST) [6]. Среди глобальной и экологически разнообразной выборки штаммов были обнаружены 4 основных типа последовательностей: ST-1, ST-17, ST19 и ST23 [6]. Из них ST-1 и ST-19 были в основном связаны с бессимптомным носительством СГВ, ST-23 был распространён как среди бессимптомных носителей, так и среди случаев инвазивного заболевания, а штаммы ST-17 серотипа III были связаны с неонатальными инвазивными инфекциями [6].
В мире существует несколько подходов к проведению антенатального скрининга на СГВ. Во-первых, это универсальный скрининг на S. agalactiae на поздних сроках беременности (35–37 нед) с применением метода культуральной диагностики. Другой подход основан на наличии акушерских факторов риска развития инфекции (роды при сроке беременности < 37 нед, безводный промежуток более 18 ч, температура тела выше 38ºC). Универсальный антенатальный скрининг на СГВ применяется в США и Канаде [7]. Скрининг на основе факторов риска, используемый в Швеции и Великобритании, более осторожен, поскольку женщин тестируют только в том случае, если у них проявляются симптомы заболевания, связанные с СГВ, например, преждевременные роды, или если у них в анамнезе были неблагоприятные исходы беременности [5].
В России с 2021 г. действует Приказ МЗ РФ № 1130н от 20.10.2020 «Об утверждении Порядка оказания медицинской помощи по профилю "акушерство и гинекология"», в соответствии с которым необходим скрининг беременных на наличие СГВ в сроки 35–37 нед беременности. Согласно этому приказу, исследуется отделяемое влагалища или одновременно влагалища и прямой кишки и проводится бактериологическое исследование с целью выделения S. agalactiae. При выделении СГВ назначаются антибактериальные препараты в родах с целью антибиотикопрофилактики антенатального инфицирования плода.
В настоящее время разработаны меры профилактики ранних СГВ-инфекций, основанные на парентеральном введении антибиотиков во время родов женщинам с высоким риском передачи микроорганизма новорождённым. Если эффективность этого метода не вызывает сомнений, то выбор женщин, которым показана антибиотикопрофилактика, является предметом дискуссий.
Несмотря на то, что антибиотикопрофилактика является хорошим методом предотвращения вертикальной передачи инфекции, вызванной S. agalactiae, и снижения частоты заболеваемости у новорождённых, существует опасность развития резистентности S. agalactiae к антибиотикам.
В настоящее время в качестве профилактики развития инвазивных форм СГВ-инфекции у новорождённых считается вакцинация как беременных женщин, так и женщин, планирующих беременность. Данная стратегия основана на способности материнских IgG проникать через плаценту и обеспечивать иммунную защиту не только от раннего начала заболевания, но также от позднего начала заболевания и послеродовых осложнений, связанных со СГВ. СГВ занимает экологические ниши (например, нижние отделы желудочно-кишечного тракта и слизистая оболочка влагалища), которые относительно инертны с иммунологической точки зрения. Фактически, значительная часть женщин, колонизированных СГВ, имеет низкие концентрации IgG к CPS в сыворотке крови, и эти женщины представляют высокий риск раннего инфицирования новорождённых [6]. Разработка безопасной и эффективной вакцины, которую можно вводить во время беременности или до неё, остаётся основной целью, поскольку современные терапевтические стратегии профилактики на основе антибиотиков не устраняют все случаи инвазивных инфекций, вызванных СГВ.
Разработка вакцин нацелена на детерминанты S. agalactiae, колонизирующих вагинальный биотоп и способных к инвазии. Самой перспективной из них был признан CPS, на основе которого учёными из США и Южной Африки в 2013 г. была разработана трёхвалентная вакцина, которая успешно проходит клинические испытания [9].
В 2017 г. были начаты клинические испытания поливалентной вакцины, направленной на серотипы Ia, Ib, II, III и V СГВ. В это же время было отмечено увеличение роста числа инфекций, вызванных серотипом IV СГВ, поэтому этот серотип был добавлен в состав шестивалентной вакцины. Эта вакцина позволила охватить 98% неонатальных инфекций, вызванных СГВ.
Новая шестивалентная конъюгированная СГВ-вакцина (GBS6) направлена на серотипы Ia, Ib, II, III, IV и V СГВ [10], которые распространены во всём мире. Моновалентные, бивалентные и трёхвалентные вакцины против серотипов Ia, Ib, II, III и V СГВ ранее изучались у небеременных и беременных женщин. Было показано, что эти вакцины безопасны и вызывают поствакцинальное увеличение антител к СГВ у младенцев и вакцинированных лиц. Однако пока не существует лицензированных вакцин против инфекции, вызванной СГВ [10]. Задачу также осложняет доля бескапсульных штаммов СГВ, которая достигает 10% в некоторых популяциях.
Другой перспективной мишенью являются поверхностные белки и белки пилей СГВ.
В 2024 г. был проведён большой систематический обзор всех существующих кандидатов на вакцину против СГВ. Все кандидаты вакцин против СГВ продемонстрировали хорошие данные по иммуногенности и безопасности для небеременных и беременных женщин. Наиболее многообещающими вакцинами-кандидатами является поливалентная вакцина на основе CPS или вакцина на основе поверхностных субъединичных белков широкого спектра действия. В целом обнаружение этих молекулярных факторов вирулентности СГВ определяет несколько перспективных мишеней для разработки профилактических вакцин. Этот систематический обзор также подчёркивает, что всё ещё существуют значительные неопределённости в детерминантах реакции антител, особенно у людей с низким исходным уровнем антител к СГВ [11].
Для снижения перинатальной заболеваемости и смертности следует уделять больше внимания клинической практике, скринингу, повсеместному выявлению и лечению возможного инфицирования матери и ребёнка СГВ, а также профилактике антенатального инфицирования плода и новорождённого. Мониторинг циркулирующих штаммов СГВ в регионе позволит оценить стратегию профилактики инвазивных неонатальных инфекций.
Целью данного исследования явилось определение молекулярно-генетических детерминант вирулентности СГВ, выделенных у беременных и новорождённых, и мониторинг распределения типов CPS и профилей пилей штаммов СГВ в Санкт-Петербурге и Ленинградской области.
Материалы и методы
В исследовании были использованы клинические изоляты СГВ, выделенные у беременных в III триместре гестации и новорождённых в 2010–2023 гг. в НИИ АГиР им. Д.О. Отта. Клиническими материалами у женщин служили средняя порция свободно выпущенной мочи, отделяемое влагалища и/или цервикального канала и слизистой прямой кишки; у новорождённых — отделяемое задней стенки глотки, полости носа, поверхность наружного слухового прохода, кожа подмышечных впадин, меконий.
Исследование проводилось при добровольном информированном согласии пациентов и их законных представителей, протокол исследования одобрен локальным этическим комитетом НИИ АГиР им. Д.О. Отта (протокол № 114 от 14.12.2021).
Клинические материалы исследовали бактериологическим методом с использованием селективного питательного бульона (бульон Тодда–Хьюита), содержащего колистин сульфат, налидиксовую и оксолиновую кислоту, которые подавляют сопутствующую микробиоту, и на агаре Мюллера–Хинтона с добавлением 5% дефибринированной крови. Выделенные стрептококки идентифицировали с использованием САМР-теста и методом белкового профилирования MALDI-TOF («Bruker»). Для дальнейших исследований штаммы хранили при температуре –70ºC в триптиказо-соевом бульоне с добавлением 30% глицерина.
Выделение бактериальной ДНК проводили комплектом реагентов для экстракции ДНК «АмплиПрайм ДНК-сорб-АМ» (ЦНИИ Эпидемиологии Роспотребнадзора) согласно инструкции производителя.
Серотип и вариант пилей определяли при помощи полимеразной цепной реакции (ПЦР). Использовали набор «Tersus plus PCR kit» («Евроген»). Термоциклирование проводили с помощью амплификатора «Терцик» («ДНК-Технология»). Для определения типов CPS был использован метод, предложенный K. Yao и соавт. [12].
Тип пилей выявляли по методу, разработанному S. Teatero и соавт. [13]. Метод включает в себя постановку двух ПЦР. Первая реакция — мультиплексная, она содержит смесь 4 пар праймеров к генам локусов PI (Pilus islands) — PI-1, PI-1b, PI-2a, PI-2b, ампликоны которых различаются по размеру. Вторая реакция содержит пару праймеров, соответствующих началу и концу 2 генов, фланкирующих локус-профаг PI-1. Если профаг отсутствует, эти праймеры амплифицируют только фланкирующие профаг гены, что соответствует 648 парам нуклеотидов. Эту реакцию используют как контроль для PI-1-отрицательных изолятов.
Для определения гипервирулентного ST-17 использовали метод ПЦР с праймерами к гену gbs2018-ST-17. Если штамм СГВ относился к гипервирулентному ST-17, получали ампликон размером 210 п.о.
Для разделения полученных ампликонов применяли электрофорез ДНК в 2% агарозном геле. Для установления молекулярного размера ампликонов использовали маркер длин ДНК 100+ bp DNA Ladder («Евроген»). Результаты визуализировали с помощью гель-документирующей системы «Infinity» («VilberLourmat»).
Статистическая обработка данных
Для статистической обработки данных использовали программное обеспечение «R v. 4.3.0». Исследование обсервационное, в которое вошли 100% доступных случаев исследования за 2010–2011, 2016–2020 и 2021–2023 гг., поэтому мощность не проверяли. Доли пациентов с тем или иным признаком представлены как в абсолютных значениях (n/N, где n — число пациентов с признаком, N — размер группы), так и в виде относительных единиц (%) с 95% доверительным интервалом (95% ДИ), рассчитанным по методу Клоппера–Пирсона. Разницу долей оценивали при помощи точного критерия Фишера. В случае множественных сравнений применяли поправку Холма. Критический уровень, после которого отвергалась нулевая гипотеза, принят при р = 0,05.
Результаты
Для мониторинга распределения генотипов CPS и профилей пилей у СГВ, выделенных у беременных и новорождённых в Санкт-Петербурге и Ленинградской области в 2010–2023 г., исследовано 420 клинических изолятов СГВ. Мы разделили эти клинические изоляты на периоды 2010–2011, 2016–2020 и 2021–2023 гг. Периоды наблюдения были выбраны в связи с тем, что в указанные периоды была проведена сравнительная оценка факторов вирулентности СГВ и антибиотикорезистентности за 10 лет. В 2021–2023 гг. в связи с продолжением мониторинга СГВ стали накапливаться новые данные, и этот период также был взят для анализа.
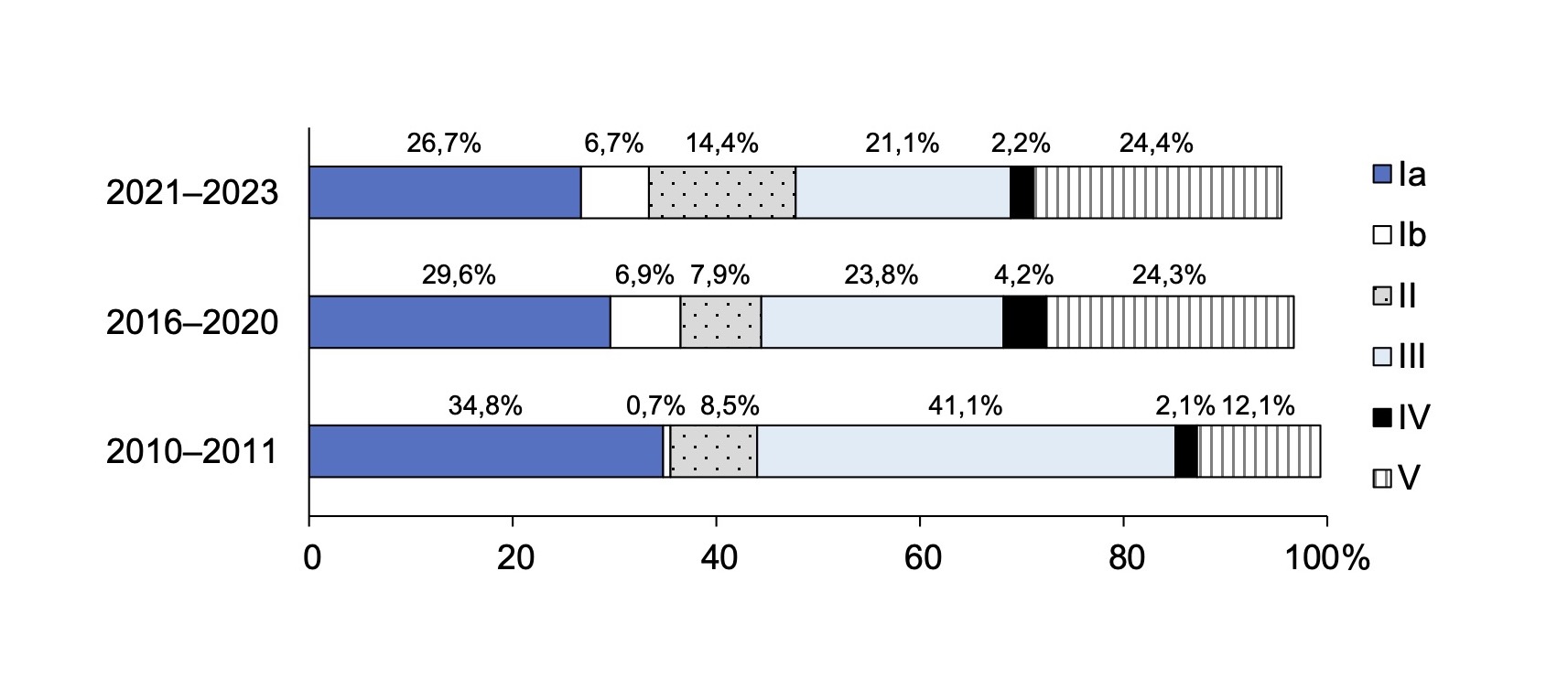
В табл. 1 представлены данные по распределению CPS у клинических изолятов СГВ, выделенных у беременных женщин и новорождённых в Санкт-Петербурге и Ленинградской области в разные периоды. В регионе во все периоды наблюдения доминировали генотипы Iа, III и V CPS СГВ, а генотипы VI, VII и IX встречались редко. На протяжении всего времени наблюдения отсутствовал генотип VIII. В течение 13 лет наблюдения частота выявления разных генотипов СГВ изменяется. Так, с 2010–2011 по 2021–2023 гг. увеличилась частота встречаемости генотипа Ib (с 0,7 до 6,7%; р = 0,015) и генотипа V (с 12,1 до 24,4%; р = 0,02), а распространённость генотипа III значимо снизилось (с 41,1 до 21,1%; р = 0,003). Следует отметить отрицательную динамику в частоте выявления генотипов Ia, Ib, III, которые включены в трёхвалентную вакцину, с 76,6 до 54,4% (табл. 1). Выявление 6 генотипов (Ia, Ib, II, II, IV, V) сохраняется на уровне более 95,0%. Такое распределение генотипов указывает на то, что шестивалентная вакцина на основе CPS была бы эффективна в нашем регионе. Эти изменения требуют пристального внимания и постоянного мониторинга, особенно при перспективе создания профилактических вакцин.
Таблица 1. Распределение CPS у клинических изолятов S. agalactiae, выделенных у беременных и новорождённых вместе в Санкт-Петербурге и Ленинградской области, n/N; % (95% ДИ)
Table 1. Distribution of capsular polysaccharides in clinical isolates of S. agalactiae isolated from pregnant women and newborns together in St. Petersburg and the Leningrad region, n/N; % (95% CI)
Генотипы | Genotype | 2010–2011 (N = 141) | 2016–2020 (N = 189) | 2021–2023 (N = 90) | Всего | Total |
Ia | 49/141; 34,8% (26,9–43,2%) | 56/189; 29,6% (23,2–36,7%) | 24/90; 26,7% (17,9–37%) | 129/420; 30,7% (26,3–35,4%) |
Ib | 1/141; 0,7% (0–3,9%) | 13/189*; 6,9% (3,7–11,5%) | 6/90*; 6,7% (2,5–13,9%) | 20/420; 4,8% (2,9–7,3%) |
II | 12/141; 8,5% (4,5–14,4%) | 15/189; 7,9% (4,5–12,8%) | 13/90; 14,4% (7,9–23,4%) | 40/420; 9,5% (6,9–12,7%) |
III | 58/141; 41,1% (32,9–49,7%) | 45/189**; 23,8% (17,9–30,5%) | 19/90**; 21,1% (13,2–31%) | 122/420; 29% (24,7–33,6%) |
IV | 3/141; 2,1% (0,4–6,1%) | 8/189; 4,2% (1,8–8,2%) | 2/90; 2,2% (0,3–7,8%) | 13/420; 3,1% (1,7–5,2%) |
V | 17/141; 12,1% (7,2–18,6%) | 46/189*; 24,3% (18,4–31,1%) | 22/90*; 24,4% (16–34,6%) | 85/420; 20,2% (16,5–24,4%) |
VI | 0/141; 0% (0–2,6%) | 2/189; 1,1% (0,1–3,8%) | 2/90; 2,2% (0,3–7,8%) | 4/420; 1% (0,3–2,4%) |
VII | 1/141; 0,7% (0–3,9%) | 2/189; 1,1% (0,1–3,8%) | 2/90; 2,2% (0,3–7,8%) | 5/420; 1,2% (0,4–2,8%) |
VIII | 0/141; 0% (0–2,6%) | 0/189; 0% (0–1,9%) | 0/90; 0% (0–4%) | 0/420; 0% (0–0,9%) |
IX | 0/141; 0% (0–2,6%) | 2/189; 1,1% (0,1–3,8%) | 0/90; 0% (0–4%) | 2/420; 0,5% (0,1–1,7%) |
Ia, Ib, III | 108/141; 76,6% (68,7–83,3%) | 114/189**; 60,3% (53–67,3%) | 49/90**; 54,4% (43,6–65%) | 271/420; 64,5% (59,7–69,1%) |
Ia, Ib, II, III, IV, V | 140/141; 99,3% (96,1–100%) | 183/189; 96,8% (93,2–98,8%) | 86/90; 95,6% (89–98,8%) | 409/420; 97,4% (95,4–98,7%) |
Примечание. Данные за 2010–2020 гг. получены и опубликованы нами ранее [14, 15]. *p < 0,05, **p < 0,05 по сравнению с данными за 2010–2011 гг.
Note. Data for 2010–2020 were obtained and published by us earlier [14, 15]. *p < 0.05, **p < 0.05 compared to the data for 2010–2011.
Эти данные более наглядно представлены на рисунке, где отражены динамика увеличения частоты обнаружения генотипов Ib, V и уменьшение частоты выявления генотипа III СГВ.
Обнаружение СГВ у беременной перед родами является прогностическим фактором колонизации новорождённых СГВ (при вертикальной передаче возбудителя). Было важно оценить частоту выявления генотипов CPS у матерей и их новорождённых. В нашем исследовании было выделено 199 пар мать–ребёнок. СГВ был обнаружен у всех матерей, колонизация новорождённых составила 52,76% (45,84–59,58%).
Наиболее часто в паре мать–ребёнок определялись генотипы III (17,0%), Ia (16,1%) и V (10,5%). Генотипы IV, VII и IX встречались в 0,5% случаев. Генотипы VI и VII были редки в нашей популяции и не были выделены в паре мать–ребёнок. Все представленные генотипы, выделенные у матери, совпадали с генотипами, выделенными у новорождённых детей (табл. 2).
Динамика частоты выявления основных CPS у S. agalactiae, выделенных у беременных и новорождённых в Санкт-Петербурге и Ленинградской области в разные периоды.
Dynamics of the frequency of detection of the main capsular polysaccharides in S. agalactiae isolated from pregnant women and newborns in St. Petersburg and the Leningrad region during different periods.
Таблица 2. Частота выявления генотипов CPS в паре мать–ребёнок в Санкт-Петербурге и Ленинградской области в 2010–2023 гг.
Table 2. Frequency of detection of genotypes of capsular polysaccharides in the mother-newborn pairs in St. Petersburg and the Leningrad region in 2010–2023
Генотипы Genotype | Пары мать–ребёнок, N = 105 Mother neonate pairs, N = 105 | |
n | % (95% ДИ | CI) | |
Ia | 32 | 16,1 (11,27–21,94) |
Ib | 3 | 1,5 (0,31–4,54) |
II | 13 | 6,53 (3,76–10,95) |
III | 34 | 17,0 (12,46–27,96) |
IV | 1 | 0,5 (0,01–3,08) |
V | 20 | 10,05 (6,53–15,08) |
VI | 0 | 0 |
VII | 1 | 0,5 (0,01–3,08) |
VIII | 0 | 0 |
IX | 1 | 0,5 (0,01–3,08) |
Изоляты СГВ, выделенные в 2021–2023 гг., были проанализированы на принадлежность к гипервирулентному ST-17. Из 90 изолятов СГВ, выделенных у беременных и новорождённых, гипервирулентный ST-17 был обнаружен у 6 (6,7%) изолятов СГВ, принадлежащих к III генотипу. У 2 детей, родившихся у этих 6 женщин, также был выделен СГВ с данным сиквенс-типом, но у них признаков СГВ-инфекции не было.
В табл. 3 представлены данные по распределению генотипов пилей у S. agalactiae, выделенных у беременных женщин и новорождённых в Санкт-Петербурге в разные периоды наблюдений.
Таблица 3. Распределение генотипов пилей у штаммов S. agalactiae, выделенных у беременных и новорождённых в Санкт-Петербурге и Ленинградской области, n/N; % (95% ДИ)
Table 3. Distribution of pili genotypes in S. agalactiae strains isolated from pregnant women and newborns in St. Petersburg and the Leningrad region, n/N; % (95% CI)
Пили | Pilus | 2010–2011 | 2016–2020 | 2021–2023 | Всего | Total |
PI-1 + PI-2a | 76/141; 53,9% (45,7–61,9%) | 110/189; 58,2% (50,8–65,3%) | 44/90; 48,9% (38,2–59,7%) | 230/420; 54,8% (49,9–59,6%) |
PI-1 + PI-2b | 20/141; 14,2% (8,9–21,1%) | 19/189; 10,1% (6,2–15,3%) | 12/90; 13,3% (7,1–22,1%) | 51/420; 12,1% (9,2–15,7%) |
PI-1b + PI-2a | 1/141; 0,7% (0–3,9%) | 4/189; 2,1% (0,6–5,3%) | 0/90; 0% (0–4%) | 5/420; 1,2% (0,4–2,8%) |
PI-1b + PI-2b | 0/141; 0% (0–2,6%) | 3/189; 1,6% (0,3–4,6%) | 0/90; 0% (0–4%) | 3/420; 0,7% (0,1–2,1%) |
PI-2a | 43/141; 30,5% (23–38,8%) | 47/189; 24,9% (18,9–31,7%) | 31/90; 34,4% (24,7–45,2%) | 90/420; 21,4% (17,6–25,7%) |
PI-2b | 1/141; 0,7% (0–3,9%) | 6/189; 3,2% (1,2–6,8%) | 3/90; 3,3% (0,7–9,4%) | 10/420; 2,4% (1,1–4,3%) |
Более половины всех распространённых в нашем регионе клинических изолятов S. agalactiae имели пили генотипа PI-1 + PI-2a, что составило 53,9% в 2010–2011 гг., 58,2% в 2016–2020 гг. и 48,9% в 2021–2023 гг., различие статистически незначимо. Следующими по распространённости были генотипы пилей PI-2a (30,5% в 2010–2011 гг., 24,9% в 2016–2020 гг. и 21,4% в 2021–2023 гг. (р > 0,05) и PI-1 + PI-2b (частота их выявления составила 12,1% за весь период наблюдения). Генотип PI-2b СГВ был одним из самых редких, что также согласуется с данными исследований, проведённых в Европе. Генотип СГВ, включающий недавно описанный локус PI-1b, как и ожидалось, встречался крайне редко.
Обсуждение
В этом исследовании мы проследили изменения генотипов CPS S. agalactiae среди беременных женщин и новорождённых детей в Санкт-Петербурге и Ленинградской области. В нашем регионе генотип СГВ Ia доминировал в 2010–2011 гг. и выявлялся в 34,8% случаев, в 2016–2020 гг. он встречался в 29,6% и в настоящее время — в 26,7%. В течение всего периода наблюдения треть (30,7%) всех клинических изолятов СГВ относилась к генотипу Iа. На втором месте по распространённости был генотип III. Однако в течение 13 лет произошли изменения в частоте выявления генотипа III СГВ, а именно значительное снижение с 41,1% в 2010–2011 гг. до 21,1% в 2021–2023 гг. (р = 0,003).Таким образом, доминирующими за весь период наблюдения генотипами остаются Ia, III и V. Эти данные совпадают с данными, полученными в других странах. Генотипы III, Ia и V были наиболее распространёнными генотипами СГВ в нескольких регионах (Европа и Северная Америка, Восточная Азия, Южная, Восточная/Центральная Африка и Австралия/Новая Зеландия) [17]. Наиболее распространённым генотипом СГВ, колонизирующим беременных во всём мире, был генотип III, встречающийся с частотой 25% (95% ДИ 23–27%), а также генотип Ia, выявляющийся у 19% (95% ДИ 17–21%) женщин [16].
В Европе и Северной Америке генотип IV встречался с частотой 4%, в Южной Африке — 3%. Генотипы VI–IX редко выявлялись в Европе (1%) [16]. В Санкт-Петербурге и Ленинградской области генотипы VI, VII и IX встречались редко (1; 1,2; 0,5% соответственно). На протяжении всего времени наблюдения генотип VIII не выявлялся ни разу.
Нужно отметить, что, по результатам нашего исследования, частота встречаемости Ib генотипа, который является одним из компонентов вакцины, увеличилась с 0,7% в 2010–2011 до 6,7% в 2021–2023 гг. (р = 0,015).
Во всем мире Ia, Ib, II–V генотипы охватывают более 99% всех случаев СГВ-инфекций, включая раннюю и позднюю неонатальную инфекцию [17]. В нашем регионе охват этих генотипов составляет (от 99 до 95,5% в разные периоды наблюдения). Эти изменения требуют пристального наблюдения за представленными генотипами при создании вакцин.
Уровень вертикальной передачи СГВ в паре мать–ребёнок в нашем исследовании составил 52,76%, и было показано совпадение молекулярно-генетических характеристик среди СГВ-положительных пар мать–ребёнок. В паре мать–ребёнок доминировали те же генотипы CPS. По данным разных авторов, частота вертикальной передачи от колонизированных СГВ матерей варьирует от 54,2% в Турции до 14,1% в Китае [18].
По данным литературы, гипервирулентные штаммы СГВ ST-17 связаны с риском развития неонатальных инвазивных инфекций. Данный сиквенс-тип СГВ был обнаружен нами у 6 женщин и 2 новорождённых. При обнаружении гипервирулентных штаммов ST-17 S. agalactiae у беременных женщин необходимо наблюдение за их новорождёнными детьми, т.к. они попадают в группу риска развития ранней и поздней инфекции и у них увеличивается риск развития менингита [19].
Основным ограничением вакцин на основе CPS является необходимость обеспечивать защиту от нескольких серотипов, поэтому стратегии мультивалентных вакцин представляют большой интерес. Трёхвалентная вакцина Novartis/GSK (Novartis/GSK GBS3), содержащая конъюгат CPS Ia/Ib/III, считается безопасной для беременных женщин, вызывает выработку высоких титров материнских антител, и антитела передаются трансплацентарно плоду [20]. К сожалению, трёхвалентная вакцина до сих пор не включает все клинически значимые генотипы СГВ и может привести к селекции невакцинных штаммов путём замены капсулы — явление, которое наблюдалось во многих популяциях высокого риска и среди штаммов ST-17 [19].
По нашим данным, эффективность трёхвалентной вакцины у беременных в 2010–2011 гг. составила бы 76,6%, в 2016–2020 гг. — 60,3%, в настоящее время её эффективность составляет лишь 54,4%. Задачу также осложняет доля бескапсульных штаммов СГВ, которая достигает 10% в некоторых популяциях. Исследование новой шестивалентной (серотипы Ia, Ib, II, III, IV и V) конъюгированной СГВ-вакцины (GBS6) [10], на долю которой приходится примерно 98% генотипов СГВ, которые распространены во всём мире, показало, что именно эти генотипы наиболее часто выявляются и в нашем регионе. Моновалентные, бивалентные и трехвалентные вакцины против генотипов Ia, Ib, II, III и V СГВ ранее изучались у небеременных и беременных женщин. Было показано, что эти вакцины безопасны и вызывают поствакцинальное увеличение антител к СГВ у новорождённых и вакцинированных женщин. Не существует лицензированных вакцин против заболеваний, вызванных СГВ [10]. Однако наличие новых генотипов и нетипируемых изолятов СГВ, а также возможность смены генотипов подтверждают необходимость постоянного наблюдения за генотипами, чтобы внести вклад в разработку универсальной вакцины [9, 11].
Важным фактором повышения вирулентности СГВ является не только капсула, но и пили. Большинство СГВ содержат PI-1 + PI-2a, и наличие этих пилей стабилизирует колонизацию [21]. Комбинация PI-1 и PI-2a преобладала среди изолятов СГВ, колонизирующих 38% беременных, PI-2a — 32%. Наибольшую долю генотипов с генами белков островков пилей составляли генотип Ia — 69% (только PI-2a) и генотип III — 85% штаммов (PI-1 и PI-2b) [22].
I. Margarit и соавт. в обширном исследовании по изучению пилей СГВ на большой коллекции клинических изолятов продемонстрировали, что все изоляты СГВ содержат по крайней мере один или комбинацию двух PI, а вакцина на основе пилей обеспечит широкую защиту [23]. Более половины всех распространённых в нашем регионе клинических изолятов S. agalactiae имели пили генотипа PI-1 + PI-2a. Следующими по распространённости были генотипы пилей PI-2a (от 24,9 до 34,4%) и PI-1 + PI-2b (12,1%). Как показывают наши исследования, распределение генотипов пилей не изменилось в наблюдаемый период. Полученные нами данные совпадают с данными, полученными в США и странах Европы [7]. Важно отметить, что вакцина, основанная на компонентах пилей, была бы эффективна в течение всего периода.
Заключение
Несмотря на плодотворные исследования последних лет, наше понимание двойной роли СГВ как комменсала и патогена пронизано множеством пробелов в знаниях. Более фундаментальные исследования, раскрывающие молекулярную основу факторов вирулентности и реакции хозяина на СГВ, необходимы для разработки новых методов профилактики, которые могут быть эффективными в предотвращении СГВ инфекций у новорождённых.
Об авторах
Кира Валентиновна Шалепо
Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта
Автор, ответственный за переписку.
Email: 2474151@mail.ru
ORCID iD: 0000-0002-3002-3874
к.б.н., с.н.с. отдела медицинской микробиологии
Россия, Санкт-ПетербургТатьяна Алексеевна Хуснутдинова
Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта
Email: 2474151@mail.ru
ORCID iD: 0000-0002-2742-2655
к.м.н., с.н.с. отдела медицинской микробиологии
Россия, Санкт-ПетербургОльга Викторовна Будиловская
Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта
Email: 2474151@mail.ru
ORCID iD: 0000-0001-7673-6274
к.м.н., с.н.с. отдела медицинской микробиологии
Россия, Санкт-ПетербургАнна Александровна Крысанова
Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта
Email: 2474151@mail.ru
ORCID iD: 0000-0003-4798-1881
к.м.н., с.н.с. отдела медицинской микробиологии
Россия, Санкт-ПетербургКирилл Викторович Сапожников
Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта
Email: 2474151@mail.ru
ORCID iD: 0000-0002-2476-7666
к.м.н., специалист отдела репродуктологии
Россия, Санкт-ПетербургАлевтина Михайловна Савичева
Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта
Email: 2474151@mail.ru
ORCID iD: 0000-0003-3870-5930
д.м.н., профессор, зав. отделом медицинской микробиологии
Россия, Санкт-ПетербургИгорь Юрьевич Коган
Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта
Email: 2474151@mail.ru
ORCID iD: 0000-0002-7351-6900
д.м.н., профессор, чл.-корр. РАН, директор
Россия, Санкт-ПетербургСписок литературы
- Russell N.J., Seale A.C., O’Driscoll M., et al. Maternal colonization with group B Streptococcus and serotype distribution worldwide: systematic review and meta-analyses. Clin. Infect. Dis. 2017;65(Suppl. 2):S100–11. doi: https://doi.org/10.1093/cid/cix658
- Хван В.О., Шипицина Е.В., Зациорская С.Л. и др. Частота и факторы риска колонизации беременных женщин стрептококками группы В. Журнал акушерства и женских болезней. 2017;66(6):44–58. Khvan V.O., Shipitsyna E.V., Zatsiorskaya S.L., et al. Frequency and risk factors of colonization of pregnant women with group B streptococci. Journal of Obstetrics and Woman Disease. 2017;66(6):44–58. doi: https://doi.org/10.17816/JOWD66644-58 EDN: https://elibrary.ru/knjtfe
- Verani J.R., McGee L., Schrag S.J. Prevention of perinatal group B streptococcal disease — revised guidelines from CDC, 2010. MMWR Recomm. Rep. 2010;59(RR-10):1–36.
- Rosini R., Margarit I. Biofilm formation by Streptococcus agalactiae: influence of environmental conditions and implicated virulence factors. Front. Cell. Infect. Microbiol. 2015;5:6. DOI: https://doi.org/10.3389/fcimb.2015.00006
- Le Doare K., O’Driscoll M., Turner K., et al. Intrapartum antibiotic chemoprophylaxis policies for the prevention of group B streptococcal disease worldwide: systematic review. Clin. Infect. Dis. 2017;65(Suppl. 2):S143–51. doi: https://doi.org/10.1093/cid/cix654
- Jones N., Bohnsack J.F., Takahashi S., et al. Multilocus sequence typing system for group B streptococcus. J. Clin. Microbiol. 2003;41(6):2530–6. doi: https://doi.org/10.1128/jcm.41.6.2530-2536.2003
- Russell N.J., Seale A.C., O’Sullivan C., et al. Risk of early-onset neonatal group B streptococcal disease with maternal colonization worldwide: systematic review and meta-analyses. Clin. Infect. Dis. 2017;65(Suppl. 2):S152–9. doi: https://doi.org/10.1093/cid/cix655
- Margarit I., Rinaudo C.D., Galeotti C.L., et al. Preventing bacterial infections with pilus-based vaccines: the group B streptococcus paradigm. J. Infect. Dis. 2009;199(1):108–15. doi: https://doi.org/10.1086/595564
- Madhi S.A., Dangor Z., Heath P.T., et al. Considerations for a phase-III trial to evaluate a group B Streptococcus polysaccharide-protein conjugate vaccine in pregnant women for the prevention of early- and late-onset invasive disease in young-infants. Vaccine. 2013;31(Suppl. 4):D52–7. doi: https://doi.org/10.1016/j.vaccine.2013.02.029
- Absalon J., Segall N., Block S.L., et al. Safety and immunogenicity of a novel hexavalent group B streptococcus conjugate vaccine in healthy, non-pregnant adults: a phase 1/2, randomised, placebo-controlled, observer-blinded, dose-escalation trial. Lancet Infect. Dis. 2021;21(2):263–74. doi: https://doi.org/10.1016/s1473-3099(20)30478-3
- Bjerkhaug A.U., Ramalingham S., Mboizi R., et al. The immunogenicity and safety of Group B Streptococcal maternal vaccines: a systematic review. Vaccine. 2024;42(2):84–98. doi: https://doi.org/10.1016/j.vaccine.2023.11.056
- Yao K., Poulsen K., Maione D., et al. Capsular gene typing of Streptococcus agalactiae compared to serotyping by latex agglutination. J. Clin. Microbiol. 2013;51(2):503–7. doi: https://doi.org/10.1128/jcm.02417-12
- Teatero S., Neemuchwala A., Yang K., et al. Genetic evidence for a novel variant of the pilus Island 1 backbone protein in group B Streptococcus. J. Med. Microbiol. 2017;66(10):1409–15. DOI: https://doi.org/10.1099/jmm.0.000588
- Колоусова К.А., Шипицына Е.В., Шалепо К.В., Савичева А.М. Факторы вирулентности и патогенности штаммов Streptococcus agalactiae, выделенных у беременных и новорождённых. Журнал акушерства и женских болезней. 2021;70(5):15–22. Kolousova K.A., Shipitsyna E.V., Shalepo K.V., Savicheva A.M. Virulence and pathogenicity factors of S. agalactiae strains isolated from pregnant women and newborns. Journal of Obstetrics and Woman Disease. 2021;70(5):15–22. doi: https://doi.org/10.17816/JOWD75671 EDN: https://elibrary.ru/oateln
- Shipitsyna E., Shalepo K., Zatsiorskaya S., Krysanova A., et al. Significant shifts in the distribution of vaccine capsular polysaccharide types and rates of antimicrobial resistance of perinatal group B streptococci within the last decade in St. Petersburg, Russia. European Journal of Clinical Microbiology & Infectious Diseases. 2020;39(8):1487–93. doi: https://doi.org/10.1007/s10096-020-03864-1 EDN: https://elibrary.ru/xrupas
- Bianchi-Jassir F., Paul P., To K.N., et al. Systematic review of Group B Streptococcal capsular types, sequence types and surface proteins as potential vaccine candidates. Vaccine. 2020;38(43):6682–94. doi: https://doi.org/10.1016/j.vaccine.2020.08.052
- Nanduri S.A., Petit S., Smelser C., et al. Epidemiology of invasive early-onset and late-onset group B Streptococcal disease in the United States, 2006 to 2015: multistate Laboratory and Population-Based Surveillance. JAMA Pediatr. 2019; 173(3):224–33. doi: https://doi.org/10.1001/jamapediatrics.2018.4826
- Li S., Wen G., Cao X., et al. Molecular characteristics of Streptococcus agalactiae in a mother-baby prospective cohort study: Implication for vaccine development and insights into vertical transmission. Vaccine. 2018;36(15):1941–8. doi: https://doi.org/10.1016/j.vaccine.2018.02.109
- Brokaw A., Furuta A., Dacanay M., et al. Waldorf bacterial and host determinants of group B streptococcal vaginal colonization and ascending infection in pregnancy. Front. Cell. Infect. Microbiol. 2021;11:720789. doi: https://doi.org/10.3389/fcimb.2021.720789
- Swamy G.K., Metz T.D., Edwards K.M., et al. Safety and immunogenicity of an investigational maternal trivalent group B streptococcus vaccine in pregnant women and their infants: results from a randomized placebo-controlled phase II trial. Vaccine. 2020;38(44):6930–40. doi: https://doi.org/10.1016/j.vaccine.2020.08.056
- Liu Y., Liu J. Group B streptococcus: virulence factors and pathogenic mechanism. Microorganisms. 2022;10(12):2483. doi: https://doi.org/10.3390/microorganisms10122483
- Rinaudo C.D., Rosini R., Galeotti C.L., et al. Specific involvement of pilus type 2a in biofilm formation in group B Streptococcus. PLoS One. 2010;5(2):e9216. doi: https://doi.org/10.1371/journal.pone.0009216
- Margarit I., Rinaudo C.D., Galeotti C.L., et al. Preventing bacterial infections with pilus-based vaccines: the group B streptococcus paradigm. J. Infect. Dis. 2009;199(1):108–15. doi: https://doi.org/10.1086/595564
Дополнительные файлы