Молекулярно-генетическая характеристика полноразмерного генома вируса гепатита В у HBsAg-негативных доноров крови в Уральском федеральном округе
- Авторы: Останкова Ю.В.1, Серикова Е.Н.1, Семенов А.В.2, Зуева Е.Б.1, Валутите Д.Э.1, Щемелев А.Н.1, Зурочка В.А.3,4, Тотолян А.А.1,5
-
Учреждения:
- Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии имени Пастера
- Государственный научный центр вирусологии и биотехнологии «Вектор»
- Институт иммунологии и физиологии Уральского отделения Российской академии наук
- Южно-Уральский государственный университет (национальный исследовательский университет)
- Первый Санкт-Петербургский государственный медицинский университет имени академика И.П. Павлова
- Выпуск: Том 99, № 6 (2022)
- Страницы: 637-650
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://microbiol.crie.ru/jour/article/view/1356
- DOI: https://doi.org/10.36233/0372-9311-325
- ID: 1356
Цитировать
Аннотация
Актуальность. По оценкам Всемирной организации здравоохранения, на конец 2019 г. более чем у 296 млн человек в мире зарегистрирован хронический вирусный гепатит В (ВГВ). Распространённость HBsAg-негативной, скрытой формы течения заболевания у доноров крови варьирует в зависимости от региона мира и чувствительности используемых методов анализа. Поскольку генетическое разнообразие вирусов демонстрирует пространственно-временные вариации, а генетический профиль изолятов в ключевых группах, потенциально способных становиться источником распространения патогена, важен для прогнозирования эпидемиологической ситуации, представляется значимым определить циркулирующие среди доноров крови в регионах России генотипы ВГВ.
Цель работы — молекулярно-генетическая характеристика геномов ВГВ, выявленных у HBsAg-негативных доноров крови в Уральском федеральном округе.
Материалы и методы. Материалом исследования служили 1400 образцов плазмы, полученных от HBsAg-негативных доноров крови Уральского федерального округа. Исследование включало определение HBsAg, антител анти-HBs IgG, анти-HBcore IgG, ДНК ВГВ. Для всех выявленных образцов проводили секвенирование и анализ нуклеотидных последовательностей полных геномов ВГВ.
Результаты. Распространённость ДНК ВГВ составила 4,93%, в том числе 4 (0,28%) случая ложного скрытого гепатита В. Среди анти-HBcore IgG-позитивных образцов ДНК ВГВ обнаружили в 18,08% случаев, в то время как у лиц с выявленной ДНК ВГВ анти-HBcore IgG — в 46,38%. У 8,69% изолятов обнаружены одновременно антитела анти-HBs IgG и ДНК вируса при отсутствии анти-HBcore IgG. На основании филогенетического анализа показано, что у HBsAg-негативных доноров крови представлены субгенотипы ВГВ в следующих соотношениях: D3 — 53,62%, D2 — 21,74%, D1 — 18,84%, С2 — 5,8%. Показана высокая вариабельность регионов S, C, P генома вируса в обследованной группе. Во всех выявленных нами случаях HBsAg-негативного хронического ВГВ у доноров крови были представлены вирусы, по крайней мере, с одной аминокислотной заменой в положениях, мутации в которых действуют как ускользающие от вакцины. В регионе обратной транскриптазы гена P в 3 (4,35%) случаях определены мутации устойчивости вируса к лекарственным препаратам: ламивудину, телбивудину, энтекавиру. В регионах preCore/Core выявлены мутации, способствующие прогрессированию заболевания печени.
Заключение. Скрытый, HBsAg-негативный хронический ВГВ представляет собой угрозу передачи ВГВ при переливании крови и её компонентов за счёт крайне низкой вирусной нагрузки, не позволяющей определить вирус с помощью рутинно используемых диагностических наборов. Ситуацию может усугубить выявленное нами обилие и разнообразие аминокислотных замен вируса, включающих мутации иммунологического избегания, мутации фармакорезистентности и мутации, способствующие прогрессированию развития заболевания.
Полный текст
Введение
Вирус гепатита В (ВГВ) — ДНК-содержащий гемоконтактный патоген, способный вызывать как острое, так и хроническое заболевание печени, приводящее к развитию цирроза и гепатоцеллюлярной карциномы (ГЦК). По оценкам Всемирной организации здравоохранения, на конец 2019 г. более чем у 296 млн человек в мире зарегистрирован хронический вирусный гепатит В (ХВГВ), смертность от связанных с инфекцией ВГВ случаев за год превысила 820 тыс. человек, однако осведомлены о своем заболевании были только 10,5% инфицированных1.
Частично двуцепочечный кольцевой геном вируса протяжённостью приблизительно 3200 нуклеотидов (нт) представлен генами S, P, C и X, кодирующими, за счёт перекрывающихся открытых рамок считывания, 7 белков.
Благодаря наличию в жизненном цикле РНК-стадии и отсутствию 3’-5’-экзонуклеазной активности обратной транскриптазы, что лишает вирус возможности корректировки генома, а также высокой скорости изменчивости, ВГВ характеризуется значительной генетической гетерогенностью [1]. Классифицируют ВГВ на основе дивергенции нуклеотидных последовательностей полного генома. В настоящее время описаны 9 генотипов (A–I), расхождение которых превышает 8%, и почти 50 субгенотипов, отличающихся друг от друга на 4,0–7,5% [2, 3]. Высокая степень генетической изменчивости позволяет вирусу реагировать на эндогенное и экзогенное селективное давление путём активной модификации структуры своего генома, что приводит к большому количеству естественно возникающих мутаций, часть из которых имеет клиническое значение. Так, в области гена S нередко выявляют аминокислотные замены в положениях 123, 126, 129, 130, 133, 144, 145 и 181, приводящие к ускользанию от иммунного ответа и/или к неэффективности диагностических тестов на HBsAg, а мутации в гене P, частично пересекающемся с геном S, способствуют устойчивости вируса к лекарственной терапии [4, 5]. Для региона гена С описаны мутации в промоторе T1753C, A1762T/G1764A, а также F24Y, E64D, E77Q, A80I/T/V, L116I, E180A, ассоциированные с прогрессированием заболевания печения и ГЦК [6].
Характеристика генотипических и мутационных профилей ВГВ в ключевых потенциально способствующих распространению вируса группах населения эпидемиологически значима для оценки моделей, путей передачи ВГВ, а также внедрения в популяцию импортированных штаммов [7]. Одной из таких ключевых групп являются доноры крови. Переливание крови и её продуктов играет важную роль в терапии тяжёлых состояний различного генеза, ежегодно спасая миллионы жизней во всем мире, однако трансфузиологические манипуляции при отсутствии достаточного контроля безопасности материала могут становиться источником инфицирования реципиентов гемоконтактными патогенами, включая вирус иммунодефицита человека (ВИЧ), ВГB и вирус гепатита C (ВГС).
В России, как и во многих странах, на протяжении многих лет основным диагностическим инструментом для выявления острой или хронической инфекции было определение поверхностного антигена ВГВ (HBsAg) серологическими методами; в случае получения сомнительных результатов по HBsAg дополнительно определяют антитела к ядерному антигену анти-HBcore IgG. В настоящее время в протокол обследования доноров входят молекулярно-биологические исследования для идентификации ДНК вируса, однако при этом допускается проведение анализа в минипуле (не более чем из 6 образцов) при чувствительности используемых наборов реагентов 100 МЕ/мл2.
Несмотря на принятые меры в области инфекционной безопасности донорства крови, остаточный риск трансфузионной передачи ВГВ сохраняется3. Связано это, помимо случаев серонегативного окна после недавнего заражения, с двумя особенностями ВГВ. Во-первых, в то время как для заражения ВИЧ и ВГС необходима высокая вирусная нагрузка патогенов, инфекционная доза ВГВ составляет 16 копий (3 МЕ/мл), независимо от объёма переливаемой плазмы/компонентов крови [8]. Во-вторых, естественной формой течения ХВГВ является так называемый скрытый ВГВ (скВГВ), определяемый наличием способной к репликации ДНК вируса в тканях печени (эписомальной ковалентно замкнутой кольцевой ДНК) и/или в крови при отрицательном результате теста на HBsAg. Серопозитивный вариант скВГВ сопровождается наличием иных маркеров ХВГВ, в первую очередь антителами анти-HBcore, а при серонегативном могут полностью отсутствовать любые маркеры. Кроме того, преобладающая в большинстве таких случаев крайне низкая вирусная нагрузка усложняет задачу выявления ДНК ВГВ методом полимеразной цепной реакции (ПЦР) [9]. В условиях переливания крови желательно применять модификации ПЦР с чувствительностью 10 МЕ/мл и ниже, проводя индивидуальное тестирование образцов. Анализ с использованием минипулов, т.е. смеси 6–10 донаций, что нередко применяется для удешевления скрининга, приводит к снижению чувствительности в соответствии с коэффициентом разбавления, не позволяя выявлять случаи с низкой вирусной нагрузкой. При математическом моделировании рассчитанная оценка остаточного риска ВГВ варьирует от < 1 до 1,4 на 1 млн донаций в странах с низкой эндемичностью ВГВ и от 16 до > 100 в странах с высокой эндемичностью [10].
Исследования распространённости скВГВ среди доноров крови долгое время были немногочисленны, однако в последние годы появляется всё больше публикаций, посвящённых этой проблеме. Встречаемость этой формы ХВГВ среди доноров крови в разных странах варьирует в зависимости от представленности HBsAg в географическом регионе. Так, среди доноров крови в Аргентине ВГВ был выявлен только в 0,06% образцов, из них только 4 образца были HBsAg-негативными. Напротив, в Лаосской Народно-Демократической Республике и Нигерии распространённость скВГВ составила 10,9 и 17% соответственно [11, 12]. В то же время зарегистрированная распространённость скВГВ среди доноров крови нередко колеблется в пределах одного и того же региона, а результаты разных исследовательских коллективов противоречивы. Например, в Иране встречаемость HBsAg у населения и у доноров крови составляет 2,6 и 0,4%, соответственно, при этом распространённость скВГВ среди доноров превышает 4% [13–15]. Таким образом, данные в целом варьируют в зависимости не только от региона, но и от методов определения вируса, включая разнообразие коммерческих наборов для выявления HBsAg и ДНК ВГВ.
Поскольку генетическое разнообразие вирусов демонстрирует пространственно-временные вариации, а генетический профиль изолятов в ключевых группах, потенциально способных становиться источником распространения патогена, важен для прогнозирования эпидемиологической ситуации, представляется значимым определить циркулирующие в настоящее время генотипы ВГВ среди регулярных доноров крови в регионах Российской Федерации.
Целью нашей работы было дать молекулярно-генетическую характеристику геномов ВГВ, выявленных у HBsAg-негативных доноров крови в Уральском федеральном округе.
Материалы и методы
В работе были использованы 1400 образцов плазмы донорской крови, полученных в 2020 г. от HBsAg-негативных регулярных доноров крови Уральского федерального округа. Все обследованные дали письменное информированное согласие на участие в исследовании. На проведение данного исследования было получено одобрение локального этического комитета Санкт-Петербургского НИИ эпидемиологии и микробиологии им. Пастера (протоколы № 67 от 22.02.2017 и № 97 от 29.01.2020). Непосредственно в медицинских учреждениях, осуществлявших сбор и банкирование крови и её элементов, образец от каждой донации исследовали на маркеры 4 гемотрансмиссивных инфекций: ВИЧ (антиген р24 ВИЧ-1, антитела к ВИЧ-1/2), ВГВ (HBsAg, ДНК ВГВ в минипулах), ВГC (антитела к ВГС, РНК ВГС в минипулах), сифилис (антитела класса М и G к бледной трепонеме). В Санкт-Петербургском НИИ эпидемиологии и микробиологии им. Пастера исследование поступившей плазмы на наличие серологических маркеров ХВГВ методом иммуноферментного анализа заключалось в качественном определении HBsAg, антител анти-HBs IgG, анти-HBcore IgG. Анализы проводили в 2 повторах с использованием коммерческих наборов «ДС-ИФА-HBsAg», «ДС-ИФА-АНТИ-HBsAg», «ДС-ИФА-АНТИ-HBc» (НПО «Диагностические системы») и «Вектогеп B-HBs-антиген», «ВектоHBsAg-антитела», «ГепаБест анти-HBc-IgG» (АО «Вектор-Бест») согласно инструкциям производителя. Для определения HBsAg использовали наборы реагентов с чувствительностью 0,05 и 0,01 МЕ/мл.
Экстракцию ДНК ВГВ осуществляли с использованием коммерческого набора «РИБО-преп» (ЦНИИ Эпидемиологии Роспотребнадзора). Предварительно для всех образцов проводили концентрирование вирусных частиц ультрацентрифугированием плазмы крови в течение 1 ч при 24 000g и 4°С.
Для первичного выявления ВГВ методом ПЦР с гибридизационно-флуоресцентной детекцией в режиме «реального времени» применяли коммерческий диагностический набор реагентов «АмплиСенс® HBV-FL» (ЦНИИ Эпидемиологии Роспотребнадзора) согласно инструкции. Чувствительность набора реагентов составляет 50 МЕ/мл. Дальнейшее определение ДНК ВГВ проводили с использованием разработанной в Санкт-Петербургском НИИ эпидемиологии и микробиологии им. Пастера методики, позволяющей выявлять ДНК ВГВ в биологическом материале при низкой вирусной нагрузке (чувствительность составляет 5 МЕ/мл), в том числе при HBsAg-негативном ХВГВ [16]. Для всех выявленных образцов проводили секвенирование и последующий анализ нуклеотидных последовательностей полных геномов ВГВ, как описано ранее [17].
Первичный анализ полученных в ходе секвенирования фрагментов осуществляли с помощью программы NCBI Blast в сравнении с нуклеотидными последовательностями, представленными в международной базе данных GenBank. Выравнивание нуклеотидных последовательностей проводили в программе MEGA11, используя алгоритм ClustalW [18]. Для построения филогенетических деревьев и последующего филогенетического анализа рассматривали расстояния между последовательностями методом присоединения соседей, позволяющим оптимизацию дерева в соответствии с критерием «сбалансированной минимальной эволюции» (neighbor-joining), для оценки достоверности построенных деревьев проведён бутстреп (bootstrap) для 1000 повторов.
Серологический подтип ВГВ определяли на основе аминокислотной последовательности HBsAg.
Полученные последовательности ВГВ также были проанализированы для определения их генотипов и оценки возможной лекарственной устойчивости и мутаций, ускользающих от иммунитета, с использованием 3 онлайн-инструментов базы данных Geno2Pheno HBV4, программы HBVseq5 из базы данных HIV Stanford, инструмента HIV-GRADE HBV6.
Статистическую обработку данных производили с помощью пакета программ «MS Excel», «Prizm 5.0» («GraphPad Software Inc.»). При оценке статистической погрешности использовали «точный» интервал Клоппера–Пирсона. Результаты представлены с указанием 95% доверительного интервала (ДИ). Для оценки достоверности различий численных данных, полученных при парных сравнениях, использовали, в зависимости от характеристик выборок, точный критерий Фишера или критерий χ2 с поправкой Йетса. В качестве порога достоверности отличий было определено значение вероятности p < 0,05.
Результаты
Возраст доноров крови в группе варьировал от 18 лет до 61 года и в среднем составил 33,5 ± 8,7 года. Количество мужчин в обследуемой группе преобладало по сравнению с женщинами — 66,85 и 33,14% соответственно.
Распространённость серологических маркеров в группе составила 72,71% (95% ДИ 70,30–75,03%). Не выявлено различий в общей распространённости маркеров ВГВ у мужчин (73,72%; 95% ДИ 70,77–76,51%) и женщин (70,69%; 95% ДИ 66,32–74,8%). Результат анализа распространённости и распределения исследованных маркеров ВГВ в обследованной группе представлен в табл. 1.
Таблица 1. Распространённость и распределение серологических маркеров ВГВ в обследованной группе, n (%; 95% ДИ) / Table 1. Prevalence and distribution of the hepatitis B serological markers in the examined group, n (%; 95% CI)
Выявленные серологические маркеры в плазме крови Detected serological markers in blood plasma | Численность в группе Number in the group (n = 1400) | Численность в группе среди мужчин Number in the group among men (n = 936) | Численность в группе среди женщин Number in the group among women (n = 464) |
Распространённость серологических маркеров | Prevalence of the hepatitis B serological markers | |||
HBs IgG+ | 947 (67,64; 65,12–70,09) | 631 (67,41; 64,31–70,41) | 316 (68,1; 63,65–72,32) |
HBcore IgG+ | 172 (12,29; 10,61–14,12) | 137 (14,64; 12,43–17,07) | 40 (8,62; 6,23–11,55) |
Серопозитивные | Seropositive | 1018 (72,71; 70,3–75,03) | 690 (73,72; 70,77–76,51) | 328 (70,69; 66,32–74,8) |
Серонегативные | Seronegative | 382 (27,29; 24,97–29,7) | 246 (26,28; 23,49–29,23) | 136 (29,31; 25,2–33,68) |
Распределение серологических маркеров | Distribution of serological markers | |||
HBcore IgG+, HBs IgG+ | 101 (7,21; 5,91–8,79) | 73 (7,8; 6,16–9,71) | 28 (6,03; 4,05–8,6) |
HBcore IgG+ изолированные | isolated | 71 (5,07; 3,98–6,35) | 59 (6,3; 4,83–8,06) | 12 (2,59; 1,34–4,47) |
HBs IgG+ изолированные | isolated | 846 (60,43; 57,81–63,00) | 558 (59,62; 56,39–62,78) | 288 (62,07; 57,48–66,5) |
Таким образом, серологические маркеры ХВГВ в целом представлены у мужчин и женщин в равной степени, однако антитела анти-HBcore IgG чаще выявляли у мужчин по сравнению с женщинами (χ2 = 10,166; p = 0,0014; df (число степеней свободы) = 1). При оценке распределения маркеров изолированные антитела анти-HBcore IgG также чаще выявляли у мужчин, чем у женщин (χ2 = 8,904; p = 0,0028; df = 1).
В пределах серопозитивной группы мужчин (67,78%; 95% ДИ 64,81–70,64%) больше, чем женщин (32,22%; 95% ДИ 29,36–35,19%). Результат анализа распространённости и распределения исследованных маркеров ВГВ в группе серопозитивных лиц представлен в табл. 2.
Таблица 2. Распространённость и распределение серологических маркеров ВГВ среди серопозитивных лиц, n (%; 95% ДИ) / Table 2. Prevalence and distribution of the hepatitis B serological markers among seropositive individuals, n (%; 95% CI)
Выявленные серологические маркеры в плазме крови Detected serological markers in blood plasma | Численность в серопозитивной группе Number in the seropositive group (n = 1018) | Численность в серопозитивной группе среди мужчин Number in the seropositive group among men (n = 690) | Численность в серопозитивной группе среди женщин Number in the seropositive group among women (n = 328) |
Распространённость серологических маркеров | Prevalence of the hepatitis B serological markers | |||
HBs IgG+ | 947 (93,03; 91,28–94,51) | 631 (91,45; 89,11–93,43) | 316 (96,34; 93,7–98,1) |
HBcore IgG+ | 172 (16,9; 14,64–19,34) | 137 (19,86; 16,94–23,03) | 40 (12,19; 8,86–16,23) |
Распределение серологических маркеров | Distribution of serological markers | |||
HBcore IgG+, HBs IgG+ | 101 (9,92; 8,15–11,92) | 73 (10,58; 8,38–13,12) | 28 (8,54; 5,75–12,10) |
HBcore IgG+ изолированные | isolated | 71 (6,97; 5,49–8,72) | 59 (8,55; 6,57–10,89) | 12 (3,66; 1,9–6,3) |
HBs IgG+ изолированные | isolated | 846 (83,1; 80,66–85,36) | 558 (80,87; 77,73–83,74) | 288 (87,8; 83,77–91,14) |
При оценке распространённости серологических маркеров по возрастным группам выявлено, что среди ВГВ-серопозитивных лиц 9,14% (95% ДИ 7,44–11,07%) — люди в возрасте 18–22 лет, 55,89% (95% ДИ 52,78–58,97%) — 23–40 лет и 34,97% (95% ДИ 32,04–37,99%) — старше 40 лет.
При использовании молекулярно-биологических методов ДНК ВГВ выявлена у 4,93% (95% ДИ 3,85–6,20%) доноров крови. Среди анти-HBcore IgG-позитивных образцов ДНК ВГВ обнаружили в 18,08% (95% ДИ 12,71–24,55%) образцов, в то время как у лиц с выявленной ДНК ВГВ анти-HBcore IgG — в 46,38% (95% ДИ 34,28–58,8%). Определены 8,69% (95% ДИ 3,26–17,97%) изолятов, у которых обнаруживали одновременно антитела анти-HBs IgG и ДНК вируса при отсутствии анти-HBcore IgG. Подчеркнём, что, несмотря на значимое преобладание мужчин в группе доноров крови и среди лиц с выявленной ДНК ВГВ (75,36%; 95% ДИ 63,51–84,94%), представленность скВГВ среди мужчин (5,56%; 95% ДИ 4,18–7,22%) преобладала по сравнению с женщинами (3,66%; 95% ДИ 2,15–5,8%) незначительно, достоверных отличий не установлено (p = 0,1488).
Вирусная нагрузка в большинстве образцов (94,2%) составила менее 50 МЕ/мл, однако в 4 случаях достигала 105 МЕ/мл.
Нуклеотидные последовательности полных геномов выявленных изолятов ВГВ депонированы в международную базу данных GenBank под номерами OP153940–OP154008.
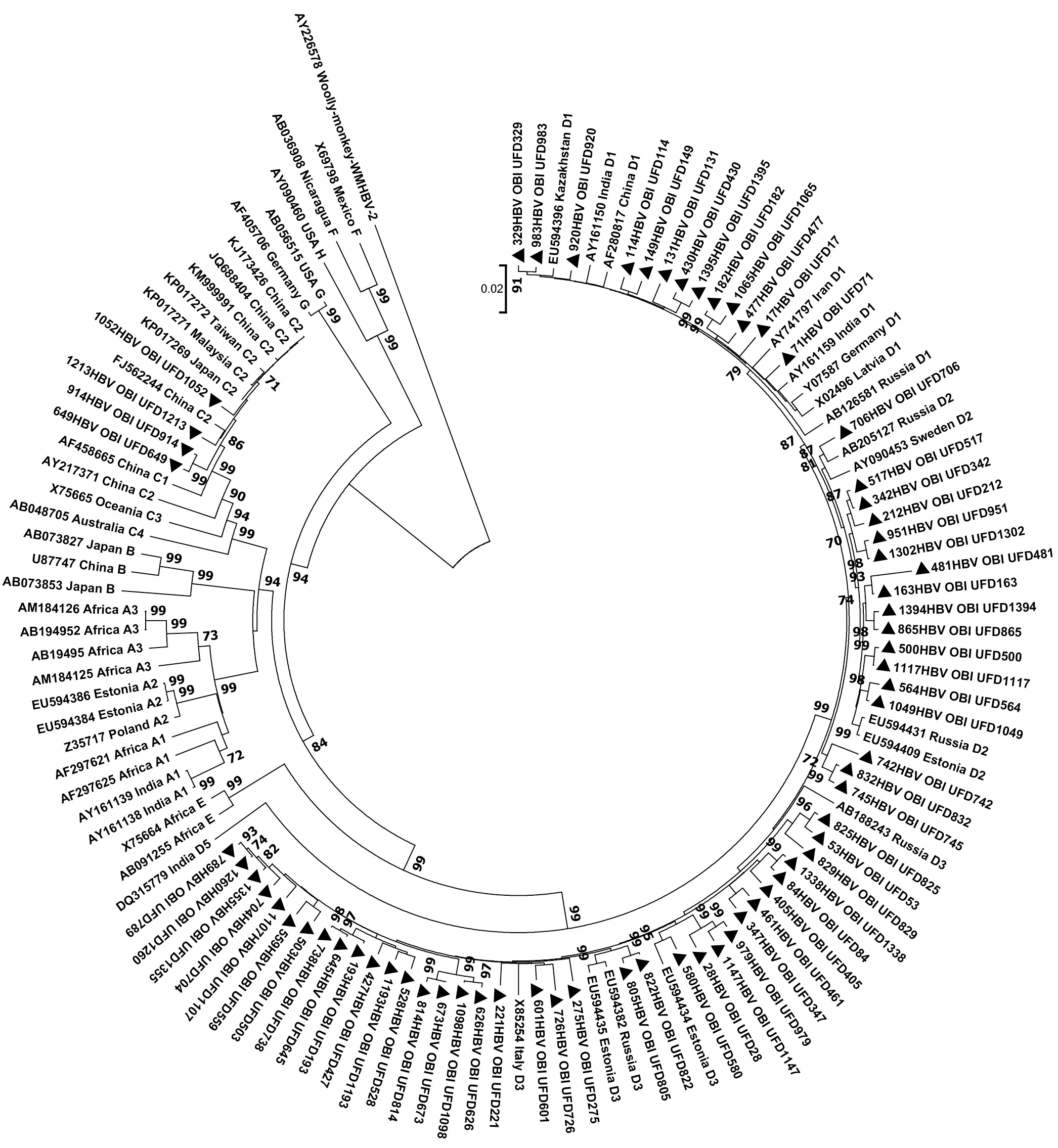
На основании филогенетического анализа 69 изолятов показано, что в обследованной группе преобладал ВГВ генотипа D (94,2%; 95% ДИ 85,82–98,4%), в 4 случаях выявлен генотип С (5,8%; 95% ДИ 1,60–14,18%). При этом среди пациентов с ВГВ генотипа D наиболее высокая частота встречаемости определена для субгенотипа D3 (56,92%) по сравнению с субгенотипами D2 (23,08%) и D1 (20%). Таким образом, среди 69 образцов у HBsAg-негативных доноров крови представлены субгенотипы ВГВ в следующих соотношениях: D3 — 53,62%, D2 — 21,74%, D1 — 18,84%, С2 — 5,8% (рисунок).
Филогенетический анализ нуклеотидных последовательностей полных геномов ВГВ, выделенных от доноров крови в сравнении с представленными в международной базе данных GenBank референсными последовательностями. Референсные последовательности обозначены кодами GenBank с указанием генотипа и региона происхождения образца. Как внешняя группа использована нуклеотидная последовательность ВГВ шерстистой обезьяны AY226578. Исследованные в настоящей работе образцы обозначены чёрными треугольниками. Для построения филогенетического дерева использовали алгоритм присоединения соседей (neighbor-joining). Даны значения bootstrap ≥ 60. / Phylogenetic analysis of the HBV complete genomic nucleotide sequences from blood donors compared to reference sequences from the GenBank international database. The reference sequences have the assigned GenBank codes showing the genotype and the region of the sample. Nucleotide sequence AY226578 of woolly monkey HBV was used as an out-group. The studied samples are marked with black triangles. The phylogenetic tree was constructed using the neighbor-joining method. Bootstrap values ≥ 60 are used.
При определении серологического подтипа обнаруженных изолятов преобладал серотип ayw2 (73,91%; 95% ДИ 61,94–83,75%), в меньшей степени представлены серотипы ayw3 (14,49%; 95% ДИ 7,18–25,14%), adw3 и adr — по 5,8% (95% ДИ 1,60–14,18%). При этом серотип ayw2 установлен для всех изолятов субгенотипа D1 и для большинства D2 и D3, ayw3 также указан для D2 и D3, adw3 определён только для ВГВ субгенотипа D2, adr для С2.
Несмотря на то что в большинстве случаев нуклеотидные последовательности ВГВ при скрытой форме ХВГВ не имеют отличий от таковых при HBsAg-позитивном заболевании и определяются как «дикий тип», в обследуемой группе доноров выявлен ряд естественных полиморфных вариантов вируса в регионах генома всех изолятов, в том числе аминокислотные замены показаны для 100% образцов ВГВ в регионах RT, SHB, MHB, LHB и Core, а также для 71,01% в регионе preCore.
Для изучения мутаций, влияющих на антигенность HBsAg, проанализирован регион главной гидрофильной области (Major Hydrophilic Region — MHR) и регион детерминанты «а», представляющей собой кластер основных эпитопов B-клеток, расположенных между 124 и 147 (или 149) аминокислотными остатками. Показано наличие аминокислотных замен в 22 позициях из 144, что составило 15,28% (95% ДИ 9,83–22,21%). Выявили следующие полиморфные варианты: Y100S/L, Q101R/H, G102R, L109Q/I, I110L, G112E, T113S, T114S, T118V/A, P120S, K122R, T125M, T127P, A128V, N131T, S132Y, F134Y, A159G, Y161F, V168A. Во всех изолятах ВГВ генотипа C в указанном регионе определены замены, не обнаруженные среди изолятов генотипа D: T126I, K160R.
В регионе обратной транскриптазы гена P также выявлен ряд полиморфных вариантов: A7V, E11G, H12L, I16T, A21S, A38G/E, R41G, Q48E, Y54H/N/D, V63I/C/G, N71K, L72R, N76T/G, S85C/L, F88S, Y89*/L, H90S, L91I, H94D, A97G, H100D, S105C, Y111N, S117Y, N118T, F122L, H124Y/N/H, H126R, T128I/N/T/A, M129L, Q130P, D134N, Y135S, N139D, L145M, K154Q, L164M, R167G, L180M, T184A, I187L, M204V, S213T, V214A, H216Q, L229F, A223S, N248H, C256S, Y257H, D263E/A, I266V/R, Q267H/L, E271D, V278I, I282V, L293H, F300L, M309K, S317A/F/S, K318R, A329T, N337T. При этом у большинства обследуемых (21,74%; 95% ДИ 23,71–33,31%) показаны по 7 мутаций в RT-регионе, у 15,94% (95% ДИ 8,24–26,74%) — по 6 мутаций, у 11,59% (95% ДИ 5,14–21,57%) — по 10 и более мутаций, у 11,59% (95% ДИ 5,14–21,57%) — по 8 мутаций, у 10,14% (95% ДИ 4,18–19,79%) — по 3 и 4 мутации, у 8,7% (95% ДИ 3,26–17,97%) — по 5 мутаций, у 7,25% (95% ДИ 2,39–16,11%) — по 9 мутаций. В 3 случаях (4,35%; 95% ДИ 0,91–12,18%) были определены мутации устойчивости вируса к лекарственным препаратам (табл. 3).
Таблица 3. Мутации лекарственной устойчивости, выявленные в обследуемой группе / Table 3. Drug resistance mutations identified in the study group
Изолят Isolate | Генотип Subgenotype | Мутация Mutation | Описание Description |
HBV_OBI_UFD53 | D1 | M204V | Резистентность к ламивудину, телбивудину, частичная резистентность к энтекавиру Resistance to lamivudine, telbivudine, partial resistance to entecavir |
HBV_OBI_UFD1147 | D2 | L180M | Ограниченная чувствительность к ламивудину Limited sensitivity to lamivudine |
T184A, L180M | Компенсаторная мутация при резистентности к энтекавиру Compensatory mutation in entecavir resistance | ||
HBV_OBI_UFD829 | D2 | L180M, M204V | Резистентность к ламивудину Resistance to lamivudine |
M204V | Резистентность к телбивудину Resistance to telbivudine | ||
T184A, L180M, M204V | Резистентность к энтекавиру Resistance to entecavir |
При анализе preCore-региона выявляли полиморфные варианты W28L/S, G29D/A. Частота встречаемости W28L/S составила 13,04% (95% ДИ 6,14–23,32%), G29D/A — 23,19% (95% ДИ 13,87–34,91%), 2 мутаций одновременно — 5,8% (95% ДИ 1,60–14,18%).
Непосредственно в регионе Core определены 39 позиций, в которых происходили аминокислотные замены: T12S, S21T/H/A/Q, F24Y, V27I, D29Q, A34T, E40D/Q, A41P, P45H, L55I, E64D, M66L/R, T67N/S, A69V/S, N74G/V, E77D, P79Q, A80I/T, N87S, N92H, I97F/L, I105V, T109S, E113Q/D, L116V/I, P130A, A131T, P135Q, N136D, T142L, L143I, T147A, V149I, R151P, D153*, R154*, S157T, Q179K, S183P.
Обсуждение
В 2016–2017 гг. в России зарегистрировано 2643 случая острого ВГВ (ОВГВ) — 0,915 на 100 тыс. населения, что отражает снижение заболеваемости за последние 5 лет в 1,6 раза. Распределение частоты заболеваемости в субъектах страны неравномерно, варьирует от 0–0,54 до 0,86–3,79 на 100 тыс. населения. Однако продолжает регистрироваться достаточно высокая заболеваемость впервые выявленным ХВГВ — приблизительно 21,045 случая на 100 тыс. населения с учётом больных ХВГВ и пациентов, которых ранее обозначали как «носители ВГВ». Такое противоречие в заболеваемости ОВГВ и ХВГВ связано, по всей видимости, с несколькими факторами. Прежде всего, инфицирование ВГВ преимущественно происходит бессимптомно, т.е. выявленные случаи острого течения заболевания составляют лишь некий процент от реального уровня частоты заражения. Второй причиной остается сравнительно низкая информированность населения и ограниченная доступность сложных молекулярно-генетических методов диагностики, в результате чего новые случаи ХВГВ выявляют либо случайно, например, при общей диспансеризации, либо при обращении к врачам пациентов с выраженными клиническими симптомами серьёзных стадий заболевания. Очевидно, что такие обнаруженные новые случаи фактически не являются новыми, а также составляют лишь некоторую долю от истинно больных ХВГВ. Уральский федеральный округ относится к регионам с самой высокой заболеваемостью ОВГВ — 0,86–3,79 на 100 тыс. населения и с крайне вариабельной заболеваемостью ХВГВ: от 0,26–7,66 в Курганской, Свердловской и Тюменской областях до 11,63–61,72 в Ямало-Ненецком автономном округе [19]. В связи с вышесказанным Уральский федеральный округ был выбран в качестве одного из первых регионов для пилотного исследования распространённости скВГВ среди доноров крови в России.
Отсутствие HBsAg в обследуемой группе соответствует информации, полученной от медицинских учреждений, предоставивших биологический материал. Высокий уровень анти-HBs IgG связан, по всей видимости, с вакцинацией против вируса. Выявленные случаи сочетания анти-HBs IgG и анти-HBcore IgG свидетельствуют о том, что 7,21% доноров сохраняли определяемые уровни нейтрализующих антител после заражения и естественного выздоровления. Преобладание мужчин среди серопозитивных лиц связано, видимо, с общим превалированием мужчин в обследуемой группе, что подтверждает сходство распространённости маркеров ХВГВ среди мужчин и женщин. Более низкая встречаемость анти-HBcore IgG у женщин по сравнению с мужчинами может свидетельствовать о сравнительно менее рисковом поведении представительниц этой когорты, а значит, и меньшей вероятности инфицирования.
Общеизвестно, что распространённость ВГВ оценивают по встречаемости HBsAg и, соответственно, выделяют географические регионы с высоким (> 8%), умеренным (2–7%) и низким (< 2%) уровнями распространённости инфекции среди населения. Россия в целом относится к странам с умеренной распространённостью. Однако такой метод не позволяет учитывать распространённость скрытой, HBsAg-негативной формы заболевания. Выявление в рамках нашего исследования 4,93% доноров ДНК ВГВ свидетельствует о недостаточности применяемых в настоящее время методов для скрининга доноров крови на маркеры ВГВ. Отсутствие достоверных отличий в частоте встречаемости ДНК ВГВ у мужчин и женщин не позволяет рассматривать мужской пол как фактор риска для развития скВГВ, несмотря на то что беспорядочные половые связи и иные варианты рискованного поведения в большей степени характерны для мужского пола. Ранее, оценивая распространённость HBsAg-негативного ХВГВ у доноров крови в Казахстане, мы также отмечали отсутствие достоверных отличий и лишь некоторую тенденцию к более частому инфицированию мужчин (10,1%) по сравнению с женщинами (6,9%) [20]. Напротив, у доноров крови в Гвинейской Республике встречаемость ДНК ВГВ у мужчин (18,61%) достоверно превышала таковую у женщин — 10,5% (χ2 = 27,285; p < 0,0001; df = 1) [21]. Можно предположить, что в наличии или отсутствии отличий могут играть роль как распространённость патогена в регионе, так и разница в особенностях поведения мужчин и женщин в России, Казахстане и Гвинее.
Отметим, что, с одной стороны, выявление только 18,08% случаев ДНК ВГВ среди всех положительных по анти-HBcore IgG доноров свидетельствует об избыточности указанного серологического маркера при диагностике. С другой стороны, только у 46,38% ДНК ВГВ-позитивных лиц обнаруживали анти-HBcore IgG, что, в свою очередь, демонстрирует недостаточность тестирования на анти-HBcore IgG для обнаружения всех доноров со скВГВ. Отдельного внимания заслуживают случаи выявления ДНК ВГВ у доноров с сочетанием антител анти-HBs IgG и анти-HBcore IgG, а также у лиц только с анти-HBs IgG. Ранее такое явление описывали преимущественно у больных c иммуносупрессией различного генеза, однако обнаруживали также и у иммунокомпетентных доноров крови. Так, среди HBsAg-негативных доноров крови с ДНК ВГВ в Китае 85% были реактивными в отношении анти-HBcore, 36,2% — анти-HBc и анти-HBs, 11,3% не имели серологических маркеров [22]. Ввиду того, что такой серологический профиль у лиц с HBsAg-негативной формой ХВГВ более распространён в странах Азии (13%), чем в Европе (2%), высказано предположение о его взаимосвязи с недостаточным охватом вакцинацией [10].
Растущая чувствительность ПЦР-методов, направленная на выявление ВГВ при крайне низкой вирусной нагрузке, потенциально способна приводить к появлению ложноположительных ответов. Из-за расхождения результатов анализа между серологическими и высокочувствительными молекулярно-генетическими тестами при скВГВ представляется затруднительным различать истинные и ложноположительные случаи обнаружения ДНК вируса. В связи с вышесказанным секвенирование нуклеотидных последовательностей всех выявленных изолятов является убедительным способом подтверждения HBsAg-негативного ХВГВ.
Генотипический профиль ВГВ в обследуемой группе имеет несколько особенностей. Так, ранее для Уральского федерального округа описывали только генотип D, что схоже с полученными нами результатами, в то время как для России в целом характерно превалирование генотипа D, но также распространённость генотипа А субгенотипа А2 и генотипа С субгенотипа С1 [23]. Однако в то время, как для центральной и северо-западной части страны характерен ВГВ субгенотипа D2, в настоящем исследовании ведущую роль играет субгенотип D3, тогда как D2 незначительно превышает по частоте встречаемости D1. Авторы считают, что такое распределение субгенотипов генотипа D обусловлено близким соседством с Казахстаном и значительным количеством мигрантов из указанного региона, встречаемость в котором ВГВ D3 и D1 крайне высока [24]. Кроме того, известно, что преобладание ВГВ D3 типично в группах пациентов, сообщавших о рискованном сексуальном поведении, тогда как множественность вариантов вируса описана для когорт, представленных людьми, считающими, что инфицирование произошло во время медицинских манипуляций [25]. Полученные результаты в целом могут служить дополнительным свидетельством изменения эпидемиологического профиля ВГВ в России за счёт трудовой миграции из стран Средней Азии. Разнообразие геновариантов вируса в пределах субгенотипов указывает на множественность независимых источников инфицирования выявленных случаев генотипа D в обследованной группе. Особого внимания заслуживают 4 изолята субгенотипа C2, практически не представленного на территории нашей страны, выделенные от мужчин в возрасте 25–30 лет, проживающих в одном городе и не являющихся родственниками. Для лучшей дифференциации полученных изолятов мы выбрали в международной базе данных GenBank 8 полных геномов ВГВ субгенотипа С2, наибольшее сходство с которыми было показано для наших образцов. Однако при филогенетическом анализе выявленные нами изоляты не образовали монофилетической клады, связанной с какой-либо референсной последовательностью. В связи с вышесказанным, несмотря на анамнестические данные доноров крови, авторы предполагают как минимум 2 независимых случая завоза в регион указанного субгенотипа.
Как известно, антигенную специфичность характеризуют серотипы, определение которых нередко осуществляют параллельно с генотипированием, поскольку, по некоторым данным, клиническое течение ХВГВ может быть связано с генотипом и серотипом вируса [26]. В России серотипы ayw2 и ayw3 типичны для изолятов генотипа D, что в целом согласуется с полученными нами результатами. Однако 4 случая серотипа adw3 изолятов D2 могут быть связаны с мутациями детерминанты «а», третичная структура которой способна определять антигенную специфичность [27]. В большинстве случаев ХВГВ, выявленных нами в группе доноров, вирусная нагрузка крайне низка и только в указанных образцах достигала 105 МЕ/мл, что позволило предположить ложный скВГВ, характеризующийся достаточно высокой вирусной нагрузкой и модифицированным HBsAg, отсутствие которого при тестировании связано с неэффективностью диагностических наборов.
В качестве профилактики заражения ВГВ доступна безопасная и эффективная вакцина, обеспечивающая 98–100% защиты от вируса, предотвращающая развитие осложнений, включая хроническое заболевание и первичный рак печени. Однако некоторые мутации, возникающие в геноме вируса как естественным образом, так и под селективным действием внешних факторов, могут приводить к избеганию терапевтических, профилактических и диагностических мероприятий. Основной белок оболочки ВГВ состоит из N-конца (положения аминокислот 1–99), MHR (положения аминокислот 100–169) и С-конца (положения аминокислот 170–226). Главный гидрофильный регион включает 2 петли, связанные дисульфидными мостиками между cys124–cys137 и cys139–cys147, и является мишенью антител, индуцированных иммунизацией и используемых в диагностических анализах [28]. Разрушение мостиков за счёт возникающих мутаций приводит к изменению конформации белка и, как следствие, к невозможности нейтрализации вируса вакцинными антителами, а также к упомянутой нами выше неэффективности диагностических наборов из-за неспособности антител распознать модифицированный эпитоп [5]. Таким образом, в некоторых случаях профилактическое применение вакцин или иммуноглобулинов может оказаться неэффективным.
Все выявленные в настоящей работе изоляты несли аминокислотные замены в MHR, включая мутации, ассоциированные с HBsAg-негативным ХВГВ, а также ранее описанные как escape-мутации, или мутации вакцинного избегания [29]. Кроме того, некоторые из обнаруженных мутаций S-региона ассоциированы с прогрессированием заболевания печени. Например, согласно данным N. Thi Cam Huong и соавт., риск развития ГКЦ составил 3,38 при инфицировании вирусом с полиморфизмом P120S [30]. Особого внимания заслуживает тот факт, что во всех выявленных нами случаях скВГВ у доноров крови были представлены вирусы по крайней мере с 1 аминокислотной заменой в положениях 120, 126 и 131, мутации в которых действуют как ускользающие от вакцины. Данное обстоятельство, очевидно, может представлять опасность в связи с возможностью передачи патогена вакцинированным лицам. Кроме того, циркуляция в группе доноров крови изолятов с escape-мутациями является проблемой с точки зрения повышенного риска реактивации ВГВ у пациентов с ослабленным иммунитетом, что имеет особое значение при переливании крови и её компонентов [31].
В связи с вышесказанным вариабельность участка обратной транскриптазы гена P не удивительна; с другой стороны, аминокислотные замены в этом домене также могут приводить к низким уровням ДНК ВГВ и HBsAg. Выявленные мутации фармакорезистентности (L180M, M204V) и компенсаторная мутация T184A описаны у пациентов с коинфекцией ВИЧ + ВГВ и относятся к наиболее распространённым среди получающих антиретровирусную терапию лиц в европейском многоцентровом исследовании [32]. Обнаружение 3 случаев скВГВ, сочетающих с мутациями ускользания мутации фармакорезистентности, представляет очевидную угрозу инфицирования реципиентов устойчивым к терапии вирусом, обнаружение которого затруднено без использования сложных высокочувствительных молекулярно-биологических методов.
В нашей работе мутации в preCore-регионе были выявлены в 71% случаев, в то время как любые изменения в последовательности этого фрагмента потенциально могут служить маркерами прогрессирования заболевания. Так, полиморфизм позиций 28 и 29, обнаруженный нами, достоверно ассоциирован с развитием цирроза печени и ГЦК. Известно также, что стоп-кодон в положении 28 (W28*) способен негативно влиять на синтез HBeAg, отвечая более чем за 90% случаев дефектной секреции указанного белка [6]. В настоящем исследовании мы не определили стоп-кодоны, и можно предположить, что W28L и W28S являются переходным «этапом» к появлению мутации W28*.
Среди общего разнообразия полиморфных вариантов в регионе Core выявлены ассоциированные с развитием заболевания печени мутации (например, F24Y, E40D/Q, E77D, A80I/T), локализованные, как известно, в районе эпитопов Т-клеток (F24Y, E40D/Q) и В-клеток (E77D, A80I/T, L116V/I) [33]. Модификации аминокислотной последовательности между позициями 113 и 143 влияют на антигенность и стабильность вируса. Теоретически мутации в основных иммунных эпитопах способны нарушить иммунный ответ, что приводит к персистирующей инфекции и, вероятно, может являться одной из причин развития скВГВ у обследованных доноров крови, а также разнообразия выявляемых у больных полиморфных вариантов во всех регионах генома вируса [34]. Полученные нами результаты согласуются с исследованиями M. Wang и соавт., определившими значительно большую вариабельность регионов генома S, включая MHR, и P, включая регион обратной транскриптазы, вируса при скВГВ по сравнению с HBsAg-позитивной формой течения заболевания [35].
СкВГВ представляет собой угрозу передачи ВГВ при переливании крови и её компонентов, ситуацию могут усугубить выявленные нами обилие и разнообразие аминокислотных замен вируса, включающих мутации иммунологического избегания, мутации фармакорезистентности и мутации, способствующие прогрессированию развития заболевания, цирроза и ГЦК. Следует также помнить, что значительную долю реципиентов составляют новорождённые и дети, в то время как при инфицировании ВГВ до 5 лет вероятность хронизации достигает 90%. Изучение характеристик полноразмерного генома ВГВ среди доноров крови из различных регионов будет способствовать пониманию ситуации с частотой встречаемости скВГВ среди доноров и значения HBsAg-негативного ХВГВ для распространения патогена в популяции.
Заключение
Высокая частота встречаемости скВГВ среди доноров крови свидетельствует не только о широком распространении HBsAg-негативной формы заболевания в популяции, но и о недостаточности общепринятых методов анализа и/или чувствительности диагностических тестов для выявления ХВГВ, требуя внимания и эффективных мер для обеспечения безопасного переливания крови. Выявленная гипервариабельность генома вируса убеждает в необходимости изучения отличительных черт патогена и иммунного ответа хозяина при скрытом течении ВГВ. Использование молекулярной филогенетики может способствовать пониманию эпидемиологии инфекционного процесса, выявлению особенностей распространения и роли «завозных» генотипов ВГВ в циркуляции вируса в регионе.
1 ВОЗ. Гепатит B. Основные факты. URL: https://www.who.int/ru/news-room/fact-sheets/detail/hepatitis-b
2 Приказ Министерства здравоохранения Российской Федерации от 28.10.2020 № 1166н «Об утверждении порядка прохождения донорами медицинского обследования и перечня медицинских противопоказаний (временных и постоянных) для сдачи крови и (или) ее компонентов и сроков отвода, которому подлежит лицо при наличии временных медицинских показаний, от донорства крови и (или) ее компонентов». URL: http://publication.pravo.gov.ru/Document/View/0001202011260032
3 WHO. Global hepatitis report 2017: executive summary; 2017. URL: https://www.who.int/publications/i/item/global-hepatitis-report-2017
4 URL: https://hbv.geno2pheno.org
5 URL: https://hivdb.stanford.edu/HBV/HBVseq/development/HBVseq.html
6 URL: https://www.hiv-grade.de/cms/grade/explanations/hbv-tool
Об авторах
Юлия Владимировна Останкова
Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии имени Пастера
Автор, ответственный за переписку.
Email: shenna1@yandex.ru
ORCID iD: 0000-0003-2270-8897
к.б.н., зав. лаб. иммунологии и вирусологии ВИЧ-инфекции, с.н.с. лаб. молекулярной иммунологии
Россия, Санкт-ПетербургЕлена Николаевна Серикова
Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии имени Пастера
Email: shenna1@yandex.ru
ORCID iD: 0000-0002-0547-3945
н.с. лаб. иммунологии и вирусологии ВИЧ-инфекции
Россия, Санкт-ПетербургАлександр Владимирович Семенов
Государственный научный центр вирусологии и биотехнологии «Вектор»
Email: shenna1@yandex.ru
ORCID iD: 0000-0003-3223-8219
д.б.н., директор Екатеринбургского НИИ вирусных инфекций
Россия, ЕкатеринбургЕлена Борисовна Зуева
Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии имени Пастера
Email: shenna1@yandex.ru
ORCID iD: 0000-0002-0579-110X
к.б.н., биолог отделения ВИЧ-инфекции и СПИД ассоциированных заболеваний
Россия, Санкт-ПетербургДиана Эдуардовна Валутите
Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии имени Пастера
Email: shenna1@yandex.ru
ORCID iD: 0000-0002-0931-102X
врач клинической лабораторной диагностики отделения ВИЧ-инфекции и СПИД-ассоциированных заболеваний
Россия, Санкт-ПетербургАлександр Николаевич Щемелев
Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии имени Пастера
Email: shenna1@yandex.ru
ORCID iD: 0000-0002-3139-3674
м.н.с. лаб. иммунологии и вирусологии ВИЧ-инфекции
Россия, Санкт-ПетербургВладимир Александрович Зурочка
Институт иммунологии и физиологии Уральского отделения Российской академии наук; Южно-Уральский государственный университет (национальный исследовательский университет)
Email: shenna1@yandex.ru
ORCID iD: 0000-0001-8930-3742
д.м.н., с.н.с. лаб. иммунологии воспаления, с.н.с. лаб. иммунобиотехнологии Научно-образовательного центра Российско-китайского центра системной патологии
Россия, Екатеринбург; ЧелябинскАрег Артёмович Тотолян
Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии имени Пастера; Первый Санкт-Петербургский государственный медицинский университет имени академика И.П. Павлова
Email: shenna1@yandex.ru
ORCID iD: 0000-0003-4571-8799
д.м.н., профессор, академик РАН, зав. лаб. молекулярной иммунологии, директор, зав. каф. иммунологии
Россия, Санкт-Петербург; Санкт-ПетербургСписок литературы
- Lin Y.Y., Liu C., Chien W.H., Wu L.L., Tao Y., Wu D., et al. New insights into the evolutionary rate of hepatitis B virus at different biological scales. J. Virol. 2015; 89(7): 3512–22. https://doi.org/10.1128/JVI.03131-14
- Kao J.H. Molecular Epidemiology of Hepatitis B Virus. Korean J. Intern. Med. 2011; 26(3): 255–61. https://doi.org/10.3904/kjim.2011.26.3.255
- Lin C.L., Kao J.H. Hepatitis B virus genotypes and variants. Cold Spring Harb. Perspect. Med. 2015; 5(5): a021436. https://doi.org/10.1101/cshperspect.a021436
- Ye Q., Shang S.Q., Li W. A new vaccine escape mutant of hepatitis B virus causes occult infection. Hum. Vaccin. Immunother. 2015; 11(2): 407–10. https://doi.org/10.4161/21645515.2014.994461
- Xue Y., Wang M.J., Yang Z.T., Yu D.M., Han Y., Huang D., et al. Clinical features and viral quasispecies characteristics associated with infection by the hepatitis B virus G145R immune escape mutant. Emerg. Microbes. Infect. 2017; 6(3): e15. https://doi.org/10.1038/emi.2017.2
- Yll M., Cortese M.F., Guerrero-Murillo M., Orriols G., Gregori J., Casillas R., et al. Conservation and variability of hepatitis B core at different chronic hepatitis stages. World J. Gastroenterol. 2020; 26(20): 2584–98. https://doi.org/10.3748/wjg.v26.i20.2584
- Mixson-Hayden T., Lee D., Ganova-Raeva L., Drobeniuc J., Stauffer W.M., Teshale E., et al. Hepatitis B virus and hepatitis C virus infections in United States-bound refugees from Asia and Africa. Am. J. Trop. Med. Hyg. 2014; 90(6): 1014–20. https://doi.org/10.4269/ajtmh.14-0068
- Candotti D., Assennato S.M., Laperche S., Allain J.P., Levicnik-Stezinar S. Multiple HBV transfusion transmissions from undetected occult infections: revising the minimal infectious dose. Gut. 2019; 68(2): 313–21. https://doi.org/10.1136/gutjnl-2018-316490
- Raimondo G., Locarnini S., Pollicino T., Levrero M., Zoulim F., Lok A.S. Update of the statements on biology and clinical impact of occult hepatitis B virus infection. J. Hepatol. 2019; 71(2): 397–408. https://doi.org/10.1016/j.jhep.2019.03.034
- Candotti D., Laperche S. Hepatitis B virus blood screening: need for reappraisal of blood safety measures? Front. Med. (Lausanne). 2018; 5: 29. https://doi.org/10.3389/fmed.2018.00029
- Pisano M.B., Blanco S., Carrizo H., Ré V.E., Gallego S. Hepatitis B virus infection in blood donors in Argentina: prevalence of infection, genotype distribution and frequency of occult HBV infection. Arch. Virol. 2016; 161; (10): 2813–17. https://doi.org/10.1007/s00705-016-2960-2
- Jutavijittum P., Andernach I.E., Yousukh A., Samountry B., Samountry K., Thammavong T., et al. Occult hepatitis B infections among blood donors in Lao PDR. Vox Sang. 2014; 106(1): 31–7. https://doi.org/10.1111/vox.12073
- Alavian S.M. Occult hepatitis B virus infection among hemodialysis patients. Hepat. Mon. 2012; 12(4): 242–3. https://doi.org/10.5812/hepatmon.869
- Smolle E., Zohrer E., Bettermann K., Haybaeck J. Viral hepatitis induces hepatocellular cancer: What can we learn from epidemiology comparing Iran and worldwide findings? Hepat. Mon. 2012; 12(10 HCC): e7879. https://doi.org/10.5812/hepatmon.7879
- Vaezjalali M., Rashidpour S., Rezaee H., Hajibeigi B., Zeidi M., Gachkar L., et al. Hepatitis B viral DNA among HBs antigen negative healthy blood donors. Hepat. Mon. 2013; 13(3): e6590. https://doi.org/10.5812/hepatmon.6590
- Серикова Е.Н., Семенов А.В., Останкова Ю.В., Тотолян А.А. Метод выявления вируса гепатита В в плазме крови при низкой вирусной нагрузке с использованием ПЦР в режиме реального времени. Клиническая лабораторная диагностика. 2021; 66(1): 59–64. https://doi.org/10.18821/0869-2084-2021-66-1-59-64
- Останкова Ю.В., Семенов А.В., Тотолян Арег А. Выявление вируса гепатита В в плазме крови при низкой вирусной нагрузке. Клиническая лабораторная диагностика. 2019; 64(10): 635–40. https://doi.org/10.18821/0869-2084-2019-64-10-635-640
- Tamura K., Stecher G., Kumar S. MEGA11: Molecular Evolutionary Genetics Analysis version 11. Mol. Biol. Evol. 2021; 38(7): 3022–7. https://doi.org/10.1093/molbev/msab120
- Покровский В.И., Тотолян А.А., ред. Вирусные гепатиты в Российской Федерации. Аналитический обзор. 11 выпуск. СПб.; 2018.
- Останкова Ю.В., Семенов А.В., Буркитбаев Ж.К., Савчук Т.Н., Тотолян А.А. Результаты генотипирования вируса гепатита В у HBsAg-негативных доноров крови в г. Астана, Казахстан. Инфекция и иммунитет. 2017; 7(4): 383–92. https://doi.org/10.15789/2220-7619-2017-4-383-392
- Бумбали С., Балде T.Л., Семенов А.В., Останкова Ю.В., Серикова Е.Н., Найденова Е.В. и др. Распространенность маркеров вирусного гепатита В среди доноров крови в Гвинейской Республике. Вопросы вирусологии. 2022; 67(1): 59–68. https://doi.org/10.36233/0507-4088-92
- Lin H., Zhao H., Tang X., Hu W., Jiang N., Zhu S., et al. Serological Patterns and Molecular Characterization of Occult Hepatitis B Virus Infection among Blood Donors. Hepat. Mon. 2016; 16(10): e40492. https://doi.org/10.5812/hepatmon.40492
- Tallo T., Tefanova V., Priimägi L., Schmidt J., Katargina O., Michailov M., et al. D2: major subgenotype of hepatitis B virus in Russia and the Baltic region. J. Gen. Virol. 2008; 89(Pt. 8): 1829–39. https://doi.org/10.1099/vir.0.83660-0
- Шевцов А.Б., Филипенко М.Л., Киянбекова Л.С., Кравченко А.П., Омралина А.Е., Абеев А.Б. и др. Генотипы вируса гепатита В, циркулирующие на территории г. Астана. Биотехнология. Теория и практика. 2011; (4): 14–23.
- Sarkar N., Pal A., Das D., Saha D., Biswas A., Bandopadhayay B., et al. Virological Characteristics of acute hepatitis B in eastern India: critical differences with chronic infection. PLoS One. 2015; 10(11): e0141741. https://doi.org/10.1371/journal.pone.0141741
- Безуглова Л.В., Мануйлов В.А., Осипова Л.П., Мосина Я.Д., Порываева В.А., Агафонова О.А. и др. Результаты испытаний реагентов для иммуноферментного определения субтипа HBsAg и генотипа вируса гепатита B в образцах плазмы крови человека. Молекулярная генетика, микробиология и вирусология. 2020; 38(4): 188–95. https://doi.org/10.17116/molgen202038041188
- Moradi A., Zhand S., Ghaemi A., Javid N., Tabarraei A. Mutations in the S gene region of hepatitis B virus genotype D in Golestan Province-Iran. Virus Genes. 2012; 44(3): 382–7. https://doi.org/10.1007/s11262-012-0715-z
- Tang Y., Liu X., Lu X., He Q., Li G., Zou Y. Occult hepatitis B virus infection in maintenance hemodialysis patients: prevalence and mutations in "a" determinant. Int. J. Med. Sci. 2020; 17(15): 2299–305. https://doi.org/10.7150/ijms.49540
- Araújo S.D.R., Malheiros A.P., Sarmento V.P., Nunes H.M., Freitas P.E.B. Molecular investigation of occult hepatitis B virus infection in a reference center in Northern Brazil. Braz. J. Infect. Dis. 2022; 26(3): 102367. https://doi.org/10.1016/j.bjid.2022.102367
- Thi Cam Huong N., Trung N.Q., Luong B.A., Tram D.B., Vu H.A., Bui H.H., et al. Mutations in the HBV PreS/S gene related to hepatocellular carcinoma in Vietnamese chronic HBV-infected patients. PLoS One. 2022; 17(4): e0266134. https://doi.org/10.1371/journal.pone.0266134
- Colagrossi L., Hermans L.E., Salpini R., Di Carlo D., Pas S.D., Alvarez M., et al. Immune-escape mutations and stop-codons in HBsAg develop in a large proportion of patients with chronic HBV infection exposed to anti-HBV drugs in Europe. BMC Infect. Dis. 2018; 18(1): 251. https://doi.org/10.1186/s12879-018-3161-2
- Hermans L.E., Svicher V., Pas S.D., Salpini R., Alvarez M., Ben Ari Z., et al. Combined analysis of the prevalence of drug-resistant hepatitis B virus in antiviral therapy-experienced patients in Europe (CAPRE). J. Infect. Dis. 2016; 213(1): 39–48. https://doi.org/10.1093/infdis/jiv363
- Al-Qahtani A.A., Al-Anazi M.R., Nazir N., Abdo A.A., Sanai F.M., Al-Hamoudi W.K., et al. The correlation between hepatitis B virus precore/core mutations and the progression of severe liver disease. Front. Cell. Infect. Microbiol. 2018; 8: 355. https://doi.org/10.3389/fcimb.2018.00355
- Sanaei N., Hashemi S.M.A., Dehno S.Z.S., Asl M.M., Moini M., Malek-Hosseini S.A., et al. Precore/core mutations of hepatitis B virus genotype D arising in different states of infection. Clin. Exp. Hepatol. 2022; 8(1): 21–8. https://doi.org/10.5114/ceh.2022.114253
- Wang M., Xu R., Huang J., Liao Q., Tang X., Shan Z., et al. Molecular characteristics of the full-length genome of occult hepatitis B virus from blood donors in China. Sci. Rep. 2022; 12(1): 8194. https://doi.org/10.1038/s41598-022-12288-0
Дополнительные файлы